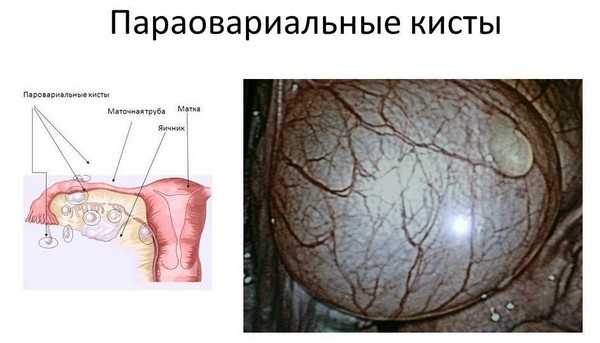
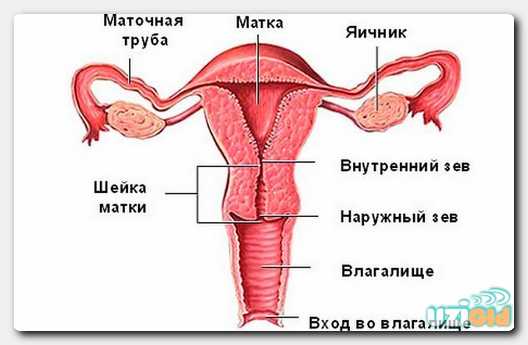
Мкб 10 поликистоз яичников
СПКЯ - это... Что такое СПКЯ?
Синдром поликистозных яичников (СПКЯ, известный также как синдром Штейна-Левенталя) — полиэндокринный синдром, сопровождающийся нарушениями функции яичников (отсутствием или нерегулярностью овуляции, повышенной секрецией андрогенов и эстрогенов), поджелудочной железы (гиперсекреция инсулина), коры надпочечников (гиперсекреция надпочечниковых андрогенов), гипоталамуса и гипофиза.
Номенклатура
Другие названия для этого синдрома следующие:
- болезнь поликистозных яичников (некорректно, поскольку это состояние характеризуется не как болезнь, отдельная нозологическая форма, а как клинический синдром, причины которого могут быть различны);
- функциональная яичниковая гиперандрогения (или функциональный яичниковый гиперандрогенизм);
- гиперандрогенная хроническая ановуляция;
- яичниковый дисметаболический синдром;
- синдром поликистоза яичников;
- поликистоз яичников.
Определения
Существуют два наиболее употребительных в клинической практике определения синдрома поликистозных яичников.
Первое определение выработано в 1990 году консенсусом экспертной комиссии, сформированной Американским Национальным институтом здравоохранения (NIH). Согласно этому определению, пациентке должен быть поставлен диагноз поликистоза яичников, если у неё одновременно присутствуют:
- Симптомы избыточной активности или избыточной секреции андрогенов (клинические и/или биохимические);
- Олигоовуляция или ановуляция
и если при этом исключены другие причины, могущие вызывать поликистоз яичников.
Второе определение сформулировано в 2003 году консенсусом европейских экспертов, сформированным в Роттердаме. По этому определению, диагноз ставится, если у пациентки присутствуют одновременно любые два из трёх следующих признаков:
- Симптомы избыточной активности или избыточной секреции андрогенов (клинические или биохимические);
- Олигоовуляция или ановуляция;
- Поликистозные яичники при ультразвуковом исследовании органов брюшной полости
и если при этом исключены другие причины, могущие вызывать поликистоз яичников.
Роттердамское определение значительно шире и включает в группу страдающих этим синдромом значительно больше пациенток. В частности, оно включает в себя и пациенток без клинических или биохимических признаков избытка андрогенов (поскольку обязательными являются любые два из трёх признаков, а не все три), в то время как в американском определении избыточная секреция или избыточная активность андрогенов является обязательным условием для диагноза поликистоза яичников. Критики Роттердамского определения утверждают, что находки, полученные при изучении пациенток с избытком андрогенов, не обязательно могут быть экстраполированы на пациенток без симптомов избытка андрогенов.
Симптомы
Общие симптомы поликистоза яичников следующие:
- Олигоменорея, аменорея — нерегулярные, редкие менструации или полное отсутствие менструаций; те менструации, которые всё же происходят, могут быть патологически скудными или, напротив, чрезмерно обильными, а также болезненными;
- Бесплодие, обычно являющееся результатом хронической ановуляции или олигоовуляции (полного отсутствия овуляций либо овуляция происходит не в каждом цикле);
- Повышенные уровни в крови андрогенов (мужских гормонов), в особенности свободных фракций тестостерона, андростендиона и дегидроэпиандростерона сульфата, что вызывает гирсутизм и иногда маскулинизацию;
- Центральное ожирение — «паукообразное» или «в форме яблока» ожирение по мужскому типу, при котором основная масса жировой ткани концентрируется внизу живота и в брюшной полости;
- Андрогенная алопеция (существенное облысение или выпадение волос по мужскому типу с залысинами по бокам лба, выше линии лба, на макушке, происходящее из-за нарушения гормонального баланса);
- Угревая сыпь, жирная кожа, себорея;
- Акантоз (тёмные пигментные пятна на коже, от светло-бежевого до тёмно-коричневого или чёрного);
- Акрохордоны (кожные складки) — мелкие складки и морщинки кожи;
- Стрии (растяжки) на коже живота, обычно как последствие быстрой прибавки массы тела;
- Длительные периоды симптомов, напоминающих симптомы предменструального синдрома (отёки, колебания настроения, боль внизу живота, в пояснице, боли или набухание молочных желёз);
- Ночные апноэ — остановки дыхания во сне, приводящие к частым ночным пробуждениям больной;
- Депрессия, дисфория (раздражительность, нервозность, агрессивность), нередко сонливость, вялость, апатия, жалобы на «туман в голове».
- Множественные кисты яичников. Сонографически они могут выглядеть как «жемчужное ожерелье», скопление белесых пузырьков или «косточки фрукта», рассеянные по всей ткани яичников;
- Увеличенные размеры яичников, обычно от 1.5 до 3 раз больше, чем в норме, являющиеся результатом множественных мелких кист;
- Утолщённая, гладкая, жемчужно-белая наружная поверхность (капсула) яичников;
- Утолщённый, гиперплазированный эндометрий матки как следствие хронического избытка эстрогенов, не сбалансированного адекватными прогестероновыми влияниями;
- Хроническая боль внизу живота или в пояснице, в тазовой области, вероятно вследствие сдавления органов малого таза увеличенными яичниками или вследствие гиперсекреции простагландинов в яичниках и эндометрии; точная причина хронической боли при поликистозе яичников неизвестна;
- Повышенный уровень ЛГ или повышенное соотношение ЛГ/ФСГ: при измерении на 3-й день менструального цикла соотношение ЛГ/ФСГ оказывается больше 1:1;
- Пониженный уровень глобулина, связывающего половые стероиды;
- Гиперинсулинемия (повышенный уровень инсулина в крови натощак), нарушение толерантности к глюкозе, признаки инсулинорезистентности тканей при тестировании по методу сахарной кривой.
Риски для здоровья и осложнения
Женщины, страдающие поликистозом яичников, подвержены повышенному риску развития следующих осложнений:
Данные ряда исследователей указывают на то, что женщины с поликистозом яичников имеют повышенный риск выкидыша или преждевременных родов, невынашивания беременности. Кроме того, многие женщины с этим синдромом не могут зачать или имеют трудности с зачатием вследствие нерегулярности менструального цикла и отсутствия или редко происходящих овуляций. Однако при правильном лечении эти женщины могут нормально зачать, выносить и родить здорового ребёнка.
Эпидемиология
Хотя при ультразвуковом обследовании брюшной полости яичники, выглядящие как поликистозные, обнаруживаются у до 20 % женщин репродуктивного возраста (в том числе и не предъявляющих никаких жалоб), лишь у 5-10 % женщин репродуктивного возраста обнаруживаются клинические признаки, позволяющие ставить диагноз синдрома поликистозных яичников. Синдром поликистозных яичников одинаково распространён в разных этнических группах. Он является наиболее частым гормональным расстройством у женщин детородного возраста и одной из ведущих причин женского бесплодия.
Этиология и патогенез
Точные причины развития синдрома неизвестны, однако большое значение придается патологическому снижению инсулин-чувствительности периферических тканей, прежде всего жировой и мышечной ткани (развитию их инсулинорезистентности) при сохранении инсулин-чувствительности ткани яичников. Возможна также ситуация патологически повышенной инсулин-чувствительности ткани яичников при сохранении нормальной чувствительности к инсулину периферических тканей.
В первом случае, как следствие инсулинорезистентности организма, возникает компенсаторная гиперсекреция инсулина, приводящая к развитию гиперинсулинемии. А патологически повышенный уровень инсулина в крови приводит к гиперстимуляции яичников и повышению секреции яичниками андрогенов и эстрогенов и нарушению овуляции, поскольку яичники сохраняют нормальную чувствительность к инсулину.
Во втором случае уровень инсулина в крови нормален, однако реакция яичников на стимуляцию нормальным уровнем инсулина патологически повышена, что приводит к тому же самому результату — гиперсекреции яичниками андрогенов и эстрогенов и нарушению овуляции.
Патологическая инсулинорезистентность тканей, гиперинсулинемия и гиперсекреция инсулина при поликистозе яичников часто (но не всегда) бывают следствием ожирения или избыточной массы тела. Вместе с тем эти явления и сами могут приводить к ожирению, так как эффектами инсулина являются повышение аппетита, повышение отложения жира и уменьшение его мобилизации.
В патогенезе поликистоза яичников придают значение также нарушениям регулирующих гипоталамо-гипофизарных влияний: избыточной секреции ЛГ, аномально повышенному соотношению ЛГ/ФСГ, повышенному «опиоидергическому» [1] [2] и пониженному дофаминергическому [3] [4] [5] тонусу в системе гипоталамус-гипофиз. Состояние может отягощаться и труднее поддаваться лечению при наличии сопутствующей гиперпролактинемии, субклинической или клинически выраженной недостаточности щитовидной железы. Такие сочетания встречаются у этих женщин значительно чаще, чем в общей популяции, что может говорить о полиэндокринной или полиэтиологической природе синдрома Штейна-Левенталя.
Некоторые исследователи придают значение повышенному уровню простагландинов и других медиаторов воспаления в текальной ткани яичников и в фолликулярной жидкости у больных поликистозом яичников и считают, что в патогенезе синдрома поликистозных яичников может играть роль возникающее по невыясненным пока причинам «холодное», асептическое воспаление ткани яичников, перенесённые воспалительные заболевания женской половой сферы или аутоиммунные механизмы. Известно, что введение простагландина E1 в яичник или в питающий его сосуд вызывает у лабораторных крыс значительное повышение секреции андрогенов и эстрогенов тека-тканью яичника.
Лечение
История
Исторически самые первые попытки лечения синдрома поликистозных яичников состояли в оперативном вмешательстве — декапсуляции яичников или их частичной резекции с удалением наиболее пораженных кистозом участков ткани, или иссечении овариального ложа (ovarian wedge resection), или в аккуратном применении диатермии (нагревания) яичников. В ряде случаев такие операции приводили к успеху и позволяли восстановить фертильность женщины, а также добиться резкого снижения секреции андрогенов яичниками, нормализации менструального цикла и др. Однако оперативное вмешательство не всегда возможно, и не всегда приводило к успеху. Кроме того, возможны осложнения, например, формирование спаек. Поэтому специалисты искали консервативные, нехирургические методы лечения поликистоза яичников.
Традиционное консервативное лечение состояло в назначении антиандрогенов, эстрогенов, прогестинов с антиандрогенной активностью или их комбинации (например, в виде противозачаточных таблеток типа Диане-35). Такое лечение обычно позволяло нормализовать менструальный цикл, но обладало недостаточной эффективностью в отношении кожных проявлений (угри, сальность кожи, андроген-зависимая алопеция), не позволяло восстановить овуляцию и фертильность, и не устраняло сами причины поликистоза яичников (нарушения инсулиновой секреции и инсулин-чувствительности тканей, функции оси гипоталамус-гипофиз и др.). Более того, лечение эстрогенами, прогестинами и антиандрогенами часто сопровождалось дальнейшим увеличением веса пациенток, усугублением имеющихся проблем с углеводным обменом и щитовидной железой, гиперпролактинемией, депрессией.
Следующая попытка усовершенствовать методы лечения синдрома поликистозных яичников была предпринята с появлением в арсенале врачей антиэстрогенных препаратов — клостилбегита (кломифена цитрата) и тамоксифена. Применение кломифенцитрата или тамоксифена в середине цикла позволяло в примерно 30 % случаев успешно индуцировать овуляцию, восстановить фертильность женщин и добиться стабильного овуляторного менструального цикла без применения экзогенных гормонов (эстрогенов, прогестинов и антиандрогенов). Однако эффективность клостилбегита и тамоксифена в отношении остальных симптомов поликистоза яичников, в частности, проявлений гиперандрогении, оказалась ограниченной. Эффективность комбинированной терапии (эстрогены и прогестины либо антиандрогены по циклу, клостилбегит или тамоксифен в середине цикла) оказалась выше, но тоже недостаточной.
Попытки улучшить эффективность лечения женщин с синдромом поликистоза яичников путём коррекции достоверно имеющихся или предполагаемых сопутствующих эндокринных нарушений (коррекция сопутствуюшей гиперпролактинемии бромокриптином, сопутствующей субклинической недостаточности щитовидной железы назначением тиреоидных гормонов, подавление гиперсекреции андрогенов надпочечниками с помощью назначения небольших доз дексаметазона) оказались отчасти успешными, но успех был индивидуален и недостаточно постоянен и предсказуем.
Реальные сдвиги в эффективности лечения поликистоза яичников произошли тогда, когда удалось глубже проникнуть в понимание патогенеза поликистоза яичников и когда стали придавать основное, первостепенное значение в развитии этого состояния гиперсекреции инсулина и патологической инсулинорезистентности тканей при сохранной инсулинчувствительности яичников. С этого времени для лечения поликистоза яичников стали широко применять в качестве препаратов первой линии препараты, нормализующие чувствительность тканей к инсулину и понижающие секрецию инсулина — метформин, глитазоны (пиоглитазон, розиглитазон). Такой подход оказался очень успешным — у 80 % женщин с поликистозом яичников на монотерапии метформином или одним из глитазонов спонтанно восстанавливалась овуляция, нормализовывался менструальный цикл, снижалась секреция андрогенов яичниками и исчезали либо уменьшались симптомы гиперандрогении, снижался вес тела, нормализовывался углеводный обмен, улучшалось психическое состояние. Большинство этих женщин затем смогли выносить и родить здоровых детей.
Ещё более высокий процент успеха, превышающий 90 %, дала комбинированная терапия — сочетание метформина или глитазонов с уже ранее известными методами (эстрогенами, антиандрогенами и прогестинами, и/или с антиэстрогенами в середине цикла и/или, возможно, коррекцией сопутствующих нарушений секреции пролактина, гормонов щитовидной железы, надпочечниковых андрогенов). Введение в практику гинекологов-эндокринологов такого комбинированного подхода к лечению поликистоза яичников позволило почти полностью исключить, кроме редких полирезистентных случаев, необходимость в хирургическом вмешательстве по поводу поликистоза яичников, а также сделать значительно более редкой необходимость в индукции овуляции с помощью гонадотропинов и в искусственном оплодотворении женщин с поликистозом яичников.
Современное состояние вопроса
На сегодняшний день препаратами первой линии при лечении поликистоза яичников являются метформин и глитазоны (пиоглитазон, розиглитазон). К ним могут быть присоединены, при необходимости, антиандрогенные препараты (спиронолактон, ципротерона ацетат), эстрогены (этинилэстрадиол в виде отдельного препарата или в противозачаточных таблетках), прогестины, малые дозы дексаметазона (0.5-1 мг в вечернее время для подавления секреции надпочечниковых андрогенов).
Необходимы меры по нормализации массы тела: диета, физическая активность.
При наличии сопутствующей гиперпролактинемии показана её коррекция с помощью назначения бромокриптина. При выявлении субклинической, а тем более клинически выраженной недостаточности щитовидной железы она подлежит коррекции с помощью назначения экзогенного L-тироксина.
При необходимости индуцировать овуляцию, если она не восстанавливается спонтанно на фоне терапии метформином или глитазонами, женщине могут быть назначены клостилбегит или тамоксифен в середине цикла.
В случае резистентности ко всем применяемым методам лечения показана хирургическая операция (лазерная или диатермокоагуляция яичников либо их декапсуляция, частичная резекция).
Примечания
- ↑ Fruzzetti F., Bersi C., Parrini D., Ricci C., Genazzani AR. PMID: 12009347
- ↑ Fulghesu AM, Ciampelli M, Guido M, Murgia F, Caruso A, Mancuso S, Lanzone A. PMID: 9472963
- ↑ Gogokhiia NA, Natmeladze KM, Mikaberidze KhL. PMID: 16148382
- ↑ Hernandez I, Parra A, Mendez I, Cabrera V, Cravioto MC, Mercado M, Diaz-Sanchez V, Larrea F. PMID: 10880731
- ↑ Zironi C, Pantaleoni M, Zizzo G, Coletta F, Velardo A. PMID: 1685015
Библиография (на английском)
- Ehrmann DA. Polycystic ovary syndrome. N Engl J Med 2005;352:1223-36. PMID 15788499.
Ссылки (на английском)
Медицинская информация
Группы поддержки для пациенток
Wikimedia Foundation. 2010.
dic.academic.ru
Синдром поликистозных яичников
Синдром поликистозных яичников (СПКЯ, известный также как синдром Штейна—Левенталя) - полиэндокринный синдром, сопровождающийся нарушениями функции яичников (отсутствием или нерегулярностью овуляции, повышенной секрецией андрогенов и эстрогенов), поджелудочной железы (гиперсекреция инсулина), коры надпочечников (гиперсекреция надпочечниковых андрогенов), гипоталамуса и гипофиза.
Частота встречаемости.
Хотя при ультразвуковом обследовании брюшной полости яичники, выглядящие как поликистозные, обнаруживаются у 20 % женщин репродуктивного возраста (в том числе и не предъявляющих никаких жалоб), лишь у 5-10 % женщин репродуктивного возраста обнаруживаются клинические признаки, позволяющие ставить диагноз синдрома поликистозных яичников. Он является наиболее частым гормональным расстройством у женщин детородного возраста и одной из ведущих причин женского бесплодия.
Основные симптомы поликистоза яичников следующие:
- Олигоменорея, аменорея - нерегулярные, редкие менструации или полное отсутствие менструаций; те менструации, которые всё же происходят, могут быть патологически скудными или, напротив, чрезмерно обильными, а также болезненными;
- Бесплодие, обычно являющееся результатом хронической ановуляции или олигоовуляции (полного отсутствия овуляций либо овуляция происходит не в каждом цикле);
- Повышенные уровни в крови андрогенов (мужских гормонов), в особенности свободных фракций тестостерона, андростендиона и дегидроэпиандростерона сульфата, что вызывает гирсутизм и иногда маскулинизацию;
- Центральное ожирение — «паукообразное» или «в форме яблока» ожирение по мужскому типу, при котором основная масса жировой ткани концентрируется внизу живота и в брюшной полости;
- Андрогенная алопеция (существенное облысение или выпадение волос по мужскому типу с залысинами по бокам лба, на макушке, происходящее из-за нарушения гормонального баланса);
- Угревая сыпь, жирная кожа, себорея;
- Акантоз (тёмные пигментные пятна на коже, от светло-бежевого до тёмно-коричневого или чёрного);
- Появление стрий (полос растяжения) на коже живота, бёдер, ягодиц, в результате быстрой прибавки массы тела на фоне гормонального дисбаланса;
- Длительные периоды симптомов, напоминающих симптомы предменструального синдрома (отёки, колебания настроения, боль внизу живота, в пояснице, боли или набухание молочных желёз);
- Множественные кисты яичников. Сонографически они могут выглядеть как «жемчужное ожерелье», скопление белёсых пузырьков или «косточки фрукта», рассеянные по всей ткани яичников;
- Увеличение размеров яичников в 1,5—3 раза за счёт возникновения множества мелких кист;
- Утолщённая, гладкая, жемчужно-белая наружная поверхность (капсула) яичников;
- Утолщённый, гиперплазированный эндометрий матки — результат длительного избытка эстрогенов, не сбалансированного адекватными прогестероновыми влияниями;
- Повышенный уровень ЛГ или повышенное соотношение ЛГ/ФСГ: при измерении на 3-й день менструального цикла соотношение ЛГ/ФСГ оказывается больше 1:1;
- Пониженный уровень глобулина, связывающего половые стероиды;
- Гиперинсулинемия (повышенный уровень инсулина в крови), нарушение толерантности к глюкозе, признаки инсулинорезистентности тканей при проведении глюкоза толерантного теста.
Причины возникновения склерополикистоза яичников.
Точные причины развития синдрома неизвестны, однако большое значение придается патологическому снижению инсулин-чувствительности периферических тканей, прежде всего жировой и мышечной ткани (развитию их инсулинорезистентности) при сохранении инсулин-чувствительности ткани яичников. Возможна также ситуация патологически повышенной инсулин-чувствительности ткани яичников при сохранении нормальной чувствительности к инсулину периферических тканей.
В первом случае, как следствие инсулинорезистентности организма, возникает компенсаторная гиперсекреция инсулина, приводящая к развитию гиперинсулинемии. А патологически повышенный уровень инсулина в крови приводит к гиперстимуляции яичников и повышению секреции яичниками андрогенов и эстрогенов и нарушению овуляции, поскольку яичники сохраняют нормальную чувствительность к инсулину.
Во втором случае уровень инсулина в крови нормален, однако реакция яичников на стимуляцию нормальным уровнем инсулина патологически повышена, что приводит к тому же самому результату — гиперсекреции яичниками андрогенов и эстрогенов и нарушению овуляции.
Патологическая инсулинорезистентность тканей, гиперинсулинемия и гиперсекреция инсулина при поликистозе яичников часто (но не всегда) бывают следствием ожирения или избыточной массы тела. Вместе с тем эти явления и сами могут приводить к ожирению, так как эффектами инсулина являются повышение аппетита, повышение отложения жира и уменьшение его мобилизации.
В патогенезе поликистоза яичников придают значение также нарушениям регулирующих гипоталамо-гипофизарных влияний: избыточной секреции ЛГ, аномально повышенному соотношению ЛГ/ФСГ. Состояние может отягощаться и труднее поддаваться лечению при наличии сопутствующей гиперпролактинемии, субклинической или клинически выраженной недостаточности щитовидной железы. Такие сочетания встречаются у этих женщин значительно чаще, чем в общей популяции, что может говорить о полиэндокринной или полиэтиологической природе синдрома Штейна-Левенталя.
Диагностика СПКЯ.
Диагностика склерополикистоза основана на:
- Сборе жалоб у пациентки, общего осмотра, гинекологического осмотра.
- Проведении ультразвукового гинекологического исследования.
- Исследовании уровня гормонов крови.
При проведении лапароскопии достигаются высокие диагностические возможности. Этот метод предполагает осмотр органов малого таза с помощью миниатюрной видеокамеры. Этот аппарат вводится с помощью прокола брюшной стенки в брюшную полость. Благодаря этому методу возможно оценить вид яичников и получить образец ткани яичника для последующего гистологического (тканевого) исследования.
Современный подход в лечении склерополикистоза яичников.
На сегодняшний день препаратами первой линии при лечении поликистоза яичников являются метформин и глитазоны (пиоглитазон, розиглитазон). К ним могут быть присоединены, при необходимости, антиандрогенные препараты (спиронолактон, ципротерона ацетат), эстрогены (этинилэстрадиол в виде отдельного препарата или в противозачаточных таблетках), прогестины, малые дозы дексаметазона (0.5-1 мг в вечернее время для подавления секреции надпочечниковых андрогенов).
Необходимы меры по нормализации массы тела: диета, физическая активность.
При наличии сопутствующей гиперпролактинемии показана её коррекция с помощью назначения бромокриптина. При выявлении субклинической, а тем более клинически выраженной недостаточности щитовидной железы она подлежит коррекции с помощью назначения экзогенного L-тироксина.
Такой подход оказался очень успешным— у 80 % женщин с поликистозом яичников на монотерапии метформином или одним из глитазонов спонтанно восстанавливалась овуляция, нормализовывался менструальный цикл, снижалась секреция андрогенов яичниками и исчезали либо уменьшались симптомы гиперандрогении, снижалась масса тела, нормализовывался углеводный обмен, улучшалось психическое состояние. Большинство этих женщин затем смогли выносить и родить здоровых детей.
При необходимости индуцировать овуляцию, если она не восстанавливается спонтанно на фоне терапии метформином или глитазонами, женщине могут быть назначены клостилбегит или тамоксифен в середине цикла.
В случае резистентности ко всем применяемым методам лечения показана хирургическая операция (лазерная или диатермокоагуляция яичников либо их декапсуляция, частичная резекция).
vrt.alyansklinik.ru
Синдром поликистозных яичников - Международный диагностический консенсус (2003 г.)
КомментарииОпубликовано в журнале: CONSILIUM-MEDICUM »» Том 06/N 9/2004
Международный диагностический консенсус (2003 г.) и современная идеология терапии
Д.Е.ШилинРоссийская медицинская академия последипломного образования МЗ и СР РФ, Москва
Введение
В 2005 г. исполнится 70 лет с момента первой зарубежной публикации о патологии, которая впоследствии получила название синдрома Штейна–Левенталя, по фамилиям авторов – чикагских гинекологов [1]. За это время эпонимическое обозначение синдрома сменилось на клинико-патогенетическое – синдром поликистозных яичников (СПКЯ), а представление медиков об этом эндокринном заболевании (Е28.2 по МКБ-10) трансформировалось из разряда редкой патологии в категорию чрезвычайно распространенной и поэтому – социально-значимой. Так, к концу ХХ века в крупных независимых исследованиях, выполненных в разных странах, получены достаточно однородные эпидемиологические сведения, указывающие на широкую распространенность СПКЯ среди женщин фертильного возраста – порядка 5% (3–10%) в популяции. Более того, на смену ранее бытовавшему клиническому пониманию данного состояния как частой патологии исключительно репродуктивного плана к началу третьего тысячелетия пришло новое осмысление СПКЯ как глобальной проблемы соматического здоровья – эндокринно-метаболического статуса, сердечно-сосудистого и онкологического риска.
Вместе с тем за столь длительное время резко обозначились существенные различия в клиническом, диагностическом и классификационном толковании СПКЯ среди представителей разных специальностей, научных течений и школ, географических частей света. По этой причине и подходы к лечению одной и той же пациентки, предпринимавшиеся на приемах разных врачей, могли принципиально отличаться, а это делало невозможным достигать высокой результативности назначаемой терапии, правильно оценивать и точно сравнивать ее истинную эффективность. Единственная (до недавнего времени) согласованная попытка сближения точек зрения на диагностику СПКЯ была предпринята в 1990 г. на Международной конференции US NIH (Национального института здоровья; г. Бетесда, США) [2]. На основании, скорее, практического опыта экспертов, чем на доказательной базе контролируемых клинических испытаний, которые в то время не пользовались особой популярностью, были утверждены следующие диагностические критерии: клинические или биохимические признаки гиперандрогении, хроническая ановуляция и исключение других известных нарушений (табл. 1).
С той поры минуло почти 15 лет, и благодаря новым достижениям в изучении патогенеза СПКЯ и совершенствованию диагностических технологий стало очевидным, что назрела крайняя необходимость жесткой ревизии дефиниции синдрома, критериев постановки данного диагноза, а также уточнения роли и места выявления инсулинорезистентности в практике обследования каждой пациентки с проявлениями гиперандрогении и менструальной дисфункции [5]. Самым значимым и неоспоримым фактом, послужившим основой для неизбежного пересмотра диагностических критериев, стало общее признание того, что синдром реально включает в себя намного более широкий спектр жалоб, симптомов и лабораторно-инструментальных признаков овариальной дисфункции, чем казалось раньше [6].
Консенсус о критериях диагноза СПКЯ (пересмотр 2003 г.)
Назревшая проблема была вынесена на рассмотрение специального Международного симпозиума объединенной рабочей группы ESHRE/ASRM (Европейского общества репродукции и эмбриологии человека и Американского общества репродуктивной медицины) [3]. Симпозиум состоялся 1–3 мая 2003 г. в Роттердаме (Нидерланды) под председательством B.Tarlatzis (Греция) и B.Fauser (Нидерланды). В нем приняли участие 27 ведущих экспертов Научный комитет: Chang (США), Azziz (США), Legro (США), Dewailly (Франция), Franks (Великобритания), Tarlatzis (Греция), Fauser (Нидерланды). Участники дискуссии: Balen (Великобритания), Bouchard (Франция), Dahlgren (Швеция), Devoto (Чили), Diamanti (Греция), Dunaif (США), Filicori (Италия), Homburg (Израиль), Ibanez (Испания), Laven (Нидерланды), Magoffin (США), Nestler (США), Norman (Австралия), Pasquali (Италия), Pugeat (Франция), Strauss (США), Tan (Канада), Taylor (США), Wild (США), Wild (Великобритания). из 12 стран с четырех континентов планеты.
Как и ранее, в заключительном документе Роттердамского консенсуса было закреплено положение, что СПКЯ остается диагнозом, требующим исключения других известных нарушений, которые проявляются универсальными клиническими признаками гиперандрогении, а поэтому могут имитировать и протекать “под маской” СПКЯ (см. далее). В то время как сам СПКЯ представляет собой синдром овариальной дисфункции (нерегулярные месячные, стойкая ановуляция, бесплодие), к специфическим проявлениям которой относятся не только гиперандрогения, но и “поликистозная” морфология яичников (см. табл. 1). Тем самым впервые была достигнута договоренность о необходимости придания ультразвуковой оценке размеров и структуры ткани яичников статуса равноправного диагностического критерия.
Согласно консенсусу наличие хотя бы двух из трех утвержденных критериев позволяет после исключения иных состояний верифицировать диагноз СПКЯ. Таким образом, с одной стороны, в плане обследования СПКЯ остается синдромом (комплексом симптомов), идентификация которого невозможна и недопустима на основании изолированного наличия любого единственного диагностического критерия (одиночно от остальных двух). С другой стороны, простой анализ попарного сочетания современных критериев позволяет сделать принципиальный вывод о необходимости расширенного толкования термина СПКЯ. Это связано с дополнительным включением в его дефиницию новых клинических форм, а именно: в отсутствие другой гиперандрогенной патологии диагноз СПКЯ допустимо выставлять не только при классическим течении (полной триаде признаков), но и при наличии одного из трех неполных (неклассических) клинико-инструментальных дуэтов. К ним отнесены:
- 1) сочетание гиперандрогении с морфологическими признаками овариального поликистоза, но на фоне регулярных по ритму менструаций и ановуляторных по незрелости фолликулов (т.е. на фоне “ановуляторных циклов”. – Прим. авт.);
2) сочетание менструальной дисфункции с ультразвуковыми (УЗ) – признаками овариального поликистоза, но в отсутствие гиперандрогении (в отечественной литературе – так называемая безгирсутная форма СПКЯ. – Прим. авт.);
3) сочетание менструальной дисфункции с гиперандрогенией, но в отсутствие явной УЗ-картины овариального поликистоза.
По нашему мнению, подобная констатация такого выраженного клинического полиморфизма СПКЯ вполне объяснима. Он отражает не столько реальное многообразие и частоту нетипичных (неполных, стертых) “портретов” патологии, сколько его клиническую эволюцию (стадийность) у пациенток разного возраста и национальности с различной генетической предрасположенностью и фенотипической индивидуальностью. Объединение названных четырех форм патологии в общий синдром на этапе постановки диагноза позволяет чаще применять современные терапевтические технологии: причем не только на этапе лечения, но и для профилактики СПКЯ; у все более широкого круга пациенток, в том числе у самых молодых, даже на стадии полового созревания.
Диагностические критерии для клинических испытаний и семейных исследований
Предполагается, что названные критерии диагностики для клинической практики, возможно, не будут столь пригодными для клинических испытаний, направленных на оценку исходов СПКЯ. Поэтому при планировании клинической апробации фармакологических препаратов для медикаментозной индукции овуляции, средств для коррекции гирсутизма или метаболических нарушений рекомендуется на этапе включения в исследование придерживаться принципа стратификации (формирования групп испытаний) по ведущему признаку, идентифицирующему СПКЯ, – соответственно, по наличию ановуляции, степени патологического роста терминальных волос или инсулинорезистентности.
Изучение семейно наследуемых случаев СПКЯ важно для понимания широкого фенотипического спектра столь гетерогенной патологии, а также для выявления генов предрасположенности к ней. В подобных исследованиях будет оправданно более узкое толкование диагноза для выявления пораженных членов семей – по изолированному наличию только овариального поликистоза или гиперандрогенемии как таковой.
Исключение сходных состояний
Перечень заболеваний, протекающих с клинической симптоматикой, напоминающей СПКЯ и по этой причине требующих исключения для постановки данного диагноза, представлен в табл. 2. Хотя круг перечисленных состояний достаточно большой, их суммарный вклад в структуру случаев гиперандрогенной ановуляции по распространенности существенно уступает СПКЯ. Тем не менее этиологическое своеобразие этих заболеваний требует дифференцированной патогенетической терапии, во многом отличающейся от таковой при СПКЯ.
В связи с этим участники симпозиума при разработке консенсуса пришли к согласованному решению о необходимости рутинного (обязательного) исследования ряда гормональных параметров, по нормальным концентрациям которых в сыворотке крови у пациентки с 2–3 клиническими критериями, подозрительными на наличие СПКЯ, можно исключить иные варианты патологии и окончательно идентифицировать СПКЯ как таковой (см. табл. 2). В их число включены 17-гидроксипрогестерон, тиреотропный гормон, пролактин, кортизол. Кроме того, крайне важной представляется особая клиническая настороженность во избежание опасности диагностической ошибки, связанной с пропуском достаточно редких, но наиболее грозных и потенциально фатальных болезней надпочечников или яичников (гиперкортицизм, вирилизирующая опухоль).
Гиперандрогения
С практической точки зрения наиболее простым и надежным способом установления гиперандрогении является клиническое выявление ее признаков путем полуколичественной (балльной) оценки гирсутизма (патологического оволосения в андрогензависимых участках лица, туловища и конечностей по шкале Ферримэна и Голлвея) с учетом наличия простых угрей (acne vulgaris) и/или облысения по мужскому типу (андрогенной алопеции). В этих случаях лабораторная верификация избытка андрогенов в крови (моче) не нужна.
В редких случаях для идентификации “безгирсутной” формы СПКЯ оправданно дополнительное гормональное исследование, направленное на установление повышенного содержания мужских половых гормонов в сыворотке крови (бессимптомной гиперандрогенемии). Уточняется, что в подобной ситуации наиболее информативным служит расчетный метод оценки индекса свободного тестостерона как результата деления стократной величины уровня общего тестостерона на уровень глобулина, связывающего половые гормоны (ТЭСГ). Особо подчеркивается, что при гиперандрогенных состояниях прямое определение содержания свободного тестостерона, как и определение концентрации общего тестостерона и андростендиона, в современной практике не рекомендуется (по лабораторно-техническим или патофизиологическим причинам).
Измерение уровня дегидроэпиандростерона-сульфата если и упоминается, то в редких случаях, и предлагается лишь для идентификации асимптоматической гиперандрогенемии, но только не для дифференциальной диагностики (!) СПКЯ с первично-надпочечниковой патологией (адреногенитальным синдромом).
Изучение ренальной экскреции мочевых метаболитов андрогенов (суммарных 17-кетостероидов и их фракций) вообще не обсуждается, на наш взгляд, ввиду их крайне низкой информативности и неудовлетворительной воспроизводимости.
Лютеинизирующий гормон
Две трети пациенток с СПКЯ имеют абсолютное повышение содержания лютеинизирующего гормона (ЛГ) в циркуляции за счет избыточной амплитуды и/или учащения выбросов этого гормона в системный кровоток, и до 95% пациенток – относительное повышение ЛГ в сравнении с нормально низким уровнем фолликулостимулирующего гормона (ФСГ), судя по так называемому гонадотропному индексу (ЛГ/ФСГ>2). Оценка данного маркера-индикатора предлагается в качестве необязательного вторичного критерия в диагностически неясных случаях, особенно у худых пациенток с аменореей, а также с исследовательской целью в научных проектах.
Поликистозные яичники
Авторы консенсуса 2003 г. в отличие от разработчиков предыдущего документа четко заявили, что морфологическая (сонографическая) верификация овариального поликистоза должна приниматься во внимание в качестве одного из возможных критериев диагноза СПКЯ. Но интерпретация данного критерия возможна только в совокупности с клинической оценкой репродуктивного статуса пациентки (менструально-овуляторной дисфункции яичников) и/или клинических (реже – лабораторных) признаков гиперандрогении. По этой причине окончательное заключение о СПКЯ может формулироваться только клиницистом, тогда как УЗ-описание подозрительной морфологии без учета анамнестических и клинико-лабораторных данных не дает права для постановки данного диагноза и тем более для назначения любого лечебного вмешательства.
Наряду с кратким упоминанием специфических эхо-признаков в тексте основного консенсуса [3] дополнительно было подготовлено и опубликовано детализированное руководство для специалистов УЗ-диагностики [4]. Его основные положения суммированы в табл. 3. Для клиницистов, оценивающих эти инструментальные признаки, крайне важно назначать УЗ-исследование малого таза на 3–5-й день менструального цикла (синхронно с гормональным обследованием), а также понимать главное требование, предъявляемое к его протоколу, обязательное измерение в максимальном сечении всех трех линейных размеров каждого яичника. Только эти результаты позволяют по простой формуле максимально точно устанавливать реальное увеличение их объема [7]. И наоборот, чем меньшее количество размеров органа представлено в протоколе УЗ-исследования, тем более трудоемкой становится технология расчета объема, либо резко падает точность результата (табл. 4).
Инсулинорезистентность
Снижение чувствительности периферических тканей к инсулину в среднем на 50% выявляется при СПКЯ как минимум в 2–3 раза чаще, чем в общей популяции. Причем этот феномен носит универсальный характер и присущ данной патологии независимо от наличия и степени выраженности ожирения – как тучным, так и худым пациенткам любого возраста. Возраст и величина избытка массы тела определяют только распространенность и интенсивность инсулинорезистентности на уровне печени, жировой и мышечной ткани. Рефрактерность к инсулину этих клеток влечет за собой компенсаторное увеличение продукции гормона поджелудочной железой – гиперинсулинемию, которая запускает массу неблагоприятных дисметаболических нарушений (со стороны углеводного и липидного обмена). Но чувствительность к инсулину в андрогенпродуцирующих структурах яичников и надпочечников при этом не страдает, а в ответ на гиперинсулинизм выработка мужских половых гормонов только возрастает, что усугубляет клинику гиперандрогении.
Заслугой консенсуса 2003 г. в отличие от предыдущей версии является то, что впервые заявляется как патофизиологическая, так и клиническая роль инсулинорезистентности (см. далее). Но с учетом известных сложностей в лабораторной идентификации этого состояния по прямым параметрам продукции инсулина на современном этапе практическая диагностика нарушений углеводного обмена рекомендуется только при наличии дополнительных факторов метаболического риска – пациенткам с СПКЯ, имеющим ожирение и/или отягощенную наследственность по сахарному диабету типа 2 [3]. Поскольку к моменту выработки консенсуса по СПКЯ экспертная группа гинекологов-эндокринологов располагала рекомендациями диабетологов по диагностике метаболического синдрома, разработанными до этого в 1997–2001 гг. [8–10], было предложено всем остальным пациенткам данные исследования пока не проводить.
Вместе с тем следует отметить, что состоявшийся всего лишь через полгода после симпозиума в Роттердаме Первый Всемирный конгресс по инсулинорезистентности (21–22 ноября 2003 г.; Лос-Анджелес, США) рассмотрел рекомендации Американской ассоциации клинических эндокринологов [11, 12], согласно которым при СПКЯ независимо от других факторов клинико-анамнестического риска и без проведения гормонального анализа инсулинорезистентность может быть установлена по наличию хотя бы 2 из 4 суррогатных признаков – по повышению уровня триглицеридов, снижению уровня холестерина липопротеидов высокой плотности артериальной гипертензии, гипергликемии натощак или через 2 ч после углеводной нагрузки (табл. 5).
Резюме
Подводя черту под обзором вновь представленных в консенсусе 2003 г. критериев СПКЯ, можно констатировать, что за счет внедрения в алгоритм обследования пациенток с гиперандрогенным бесплодием метода УЗ-исследования малого таза и изъятия из этого арсенала ряда неинформативных гормональных параметров, в целом диагностика СПКЯ стала более доступной, менее инвазивной, более дешевой и более точной. Настолько точной, насколько это необходимо для грамотного выбора современной рациональной тактики лечения.
Современная идеология терапии СПКЯ
Индивидуальная тактика ведения конкретной пациентки с СПКЯ нередко зависит не только от установленного нозологического варианта патологии, но и от текущей жизненной ситуации в семье, где проводится планирование беременности. С учетом этого терапию СПКЯ условно можно разделить на 2 группы: базовую – когда длительно исполняется комплексная реабилитационная программа и планомерная подготовка молодой женщины к беременности, и ситуационную – когда по желанию пациентки неотложно решается вопрос о восстановлении фертильности.
Базовая терапия
Арсенал помощи пациенткам с СПКЯ представлен ныне большой фармакотерапевтической группой мощных лекарственных средств, оказывающих специфические и принципиально отличные воздействия на разные патогенетические звенья (рис. 1). Индивидуальный комплекс мероприятий разрабатывается с учетом наличия или отсутствия указаний на инсулинорезистентность, образа пищевого поведения и вредных привычек. Базовая терапия предусматривает два основных сценария лечения: а) для худых без гиперинсулинизма – антиандрогенные (рис. 2) ± эстроген-гестагенные препараты; б) для имеющих избыточную массу тела – сенситайзеры инсулина в сочетании с мероприятиями по нормализации массы тела.
Наиболее ощутимым и значимым следствием открытия роли инсулинорезистентности в формировании СПКЯ стала новая терапевтическая технология с применением лекарственных препаратов, повышающих чувствительность инсулиновых рецепторов. Следует сразу оговориться, что группа метформина и глитазонов показана хотя и абсолютному большинству пациенток, но не всем. Совершенно очевидно, что для отбора на терапию инсулинсенсибилизирующими препаратами явное преимущество имеют только лица, удовлетворяющие критериям периферической рефрактерности к гормону.
С момента публикации в 1994 г. статьи коллектива авторов из Венесуэлы и США Velazquez EM, Mendoza S, Hamer T, Sosa F, Glueck CJ. Metformin therapy in polycystic ovary syndrome reduces hyperinsulinemia, insulin resistance, hyperandrogenemia, and systolic blood pressure, while facilitating normal menses and pregnancy. Metabolism. 1994; 43 (5): 647–54. о первом опыте применения метформина при СПКЯ прошло 10 лет. За эти годы опубликовано еще около двухсот работ по данному вопросу. В большинстве из них представлены сведения об испытаниях нерандомизированных, неконтролируемых и, как правило, малочисленных по включенным в опытные выборки пациенткам. Такой уровень научного анализа не удовлетворяет современным жестким требованиям доказательной медицины. Поэтому исключительный интерес представляют публикации систематизированных аналитических обзоров и итоги метаанализа по сводным данным из сопоставимых по дизайну испытаний [13–15]. Подобные работы появились лишь в течение последнего года, и их обсуждение важно как для текущей практики, так и на перспективу. В табл. 6 приводим сводные данные наиболее очевидных и систематически воспроизводимых эффектов метформина при СПКЯ.
Таблица 1. Диагностические критерии СПКЯ и сходных состояний
| Состояния и критерии их диагностики СПКЯ |
| Критерии Первой Международной конференции US NIH (Национального института здоровья США; 1990 г.) [2] при наличии обоих следующих критериев:
при отсутствии других причин (гиперпролактинемии, тиреоидной патологии, поздней формы адреногенитального синдрома, синдрома гиперкортицизма) Критерии по консенсусу Симпозиума рабочей группы ESHRE/ASRM(Европейского общества репродукции и эмбриологии человека и Американского общества репродуктивной медицины; 2003 г.) [3] при наличии любых двух критериев из трех следующих:
|
| Поликистозные яичники (по данным УЗ-исследования [4])
|
Таблица 2. Дифференциальный диагноз СПКЯ от других причин гиперандрогении [2, 3]
| СПКЯ– это диагноз исключения других эндокринопатий | |
| Гиперандрогенные состояния | Главные “маркеры” |
| 1. Идиопатический гирсутизм | Rt + “мужской анамнез” а |
| 2. Неклассический вариант ВДКН | 17-оксипрогестерон б |
| 3. Гиперпролактинемический гипогонадизм | ПРЛ |
| 4. Первичный гипотиреоз | ТТГ |
| 5. Вирилизирующие опухоли | Клиника в + “объем” Н/Я г |
| 6. Тотальный гиперкортицизм | Клиника д + кортизол |
Примечание. а – родственники-мужчины с ранним началом облысения (андрогенной алопеции) и/или с семейным типом избыточного оволосения по мужской линии; б – дискриминационный порог выше 2–3 мкг/л (6,9–10,4 нМоль/л); в – вирилизация наружных половых органов и гортани (клиторомегалия, ларингомегалия, барифония); г – при визуализации надпочечников и яичников;
д – “кушингоидизация” внешности с перераспределением жира по верхнему типу + стероидные стрии, плетора, геморрагии, остеопороз.
medi.ru
Поликистоз яичников
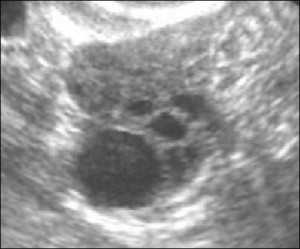
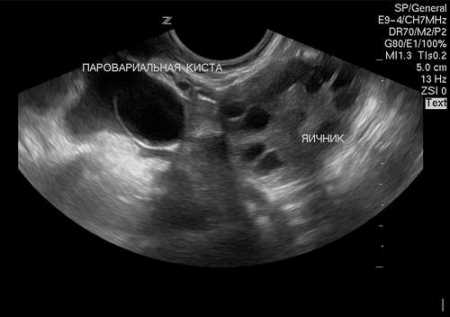
Поликистоз (УЗ-признаки)
Как известно, регуляция менструального цикла осуществляется сложным взаимодействием гормонов гипоталамуса, гипофиза, яичников, щитовидной железы. При нарушении баланса хотя бы одного вида гормонов нарушается работа яичников и менструальный цикл.
Поликистоз яичников (ПЯ) — одно из гормональных заболеваний, приводящее к тому, что в организме не происходит овуляция (выход яйцеклетки из яичника) и развивается бесплодие. Поликистоз яичников характеризуется нарушением менструального цикла, избыточным оволосением и ожирением (вследствие гормонального дисбаланса) и образованием множественных кист на яичниках, увеличения их размеров, уплотнением оболочки. Первым признаком поликистоза яичников в подростковом возрасте может быть аменорея (отсутствие месячных), нерегулярные или обильные месячные, однако, в полной мере поликистоз проявляется в более зрелом возрасте, когда женщина не может забеременеть или выносить ребенка.
Этиология
При поликистозе яичников в организме вырабатывается избыточное количество андрогена, что приводит к нарушению соотношения мужских и женских половых гормонов, т.е. гормональному дисбалансу. В этом случае овуляция происходит реже, чем положено (олигоовуляция), или не происходит вообще (ановуляция). Прекращение овуляции приводит к нарушению или прекращению менструации.
Точные причины поликистоза яичников науке неизвестны, но исследования показывают, что ПЯ может быть связан с избытком инсулина — гормона, вырабатываемого поджелудочной железой. Инсулин регулирует потребление клетками глюкозы (сахара), первичного источника энергии организма. Избыток инсулина каким-то образом стимулирует выработку андрогена яичниками. Кроме того, немалую роль в развитии поликистоза яичников играет наследственность и генетические факторы.
Предрасполагающими факторами считаются:
- сопутствующие гинекологические заболевания
- избыточный вес
- сахарный диабет
- тяжелые инфекционные заболевания, в том числе в анамнезе
- заболевания сердечно-сосудистой системы
- наследственная предрасположенность
- хронические стрессы, переутомления и др.
Распространенность
Поликистоз яичников — самое распространенное гормональное заболевание среди женщин детородного возраста, от которого страдает 5-10% женского населения планеты. Ранняя диагностика и лечение поликистоза яичников помогает уменьшить риск развития долговременных осложнений, в том числе диабета и сердечных заболеваний.
Клиническая картина
Поликистоз яичниковклинически проявляется в виде нарушений менструального цикла (чаще задержки), избыточное оволосение на теле, увеличение всех размеров яичников, у половины больных — избыточный вес. Критерием диагностирования поликистоза яичников является выявление как минимум двух из следующих симптомов:
Нерегулярная менструация или ее отсутствие. Это самый распространенный и верный признак ПЯ. Под нерегулярной менструацией подразумевают нарушения менструального цикла, промежуток между двумя менструациями более 35 дней или же менструация реже восьми раз в год. Поликистоз яичников начинается в период полового созревания, часто с началом менструации.
Избыток гормона андрогена. Повышенный уровень содержания в организме мужского гормона андрогена может привести к появлению таких физических симптомов, как избыточное оволосение на лице, груди, в паховой области, на спине, руках и ногах, угревая сыпь (акне) и облысение по мужскому типу (алопеция). Тем не менее, далеко не у всех женщин с ПЯ появляются физическим симптомы повышенного уровня андрогена.
Клиническая картина поликстоза яичников характерна и для некоторых других заболеваний, в том числе:
* Гипотиреоз. В этом случае понижается активность щитовидной железы, что может привести к отсутствию менструации (аменорее).
* Гиперпролактинемия. При гиперпролактинемии гипофиз вырабатывает слишком большое количество гормона пролактина, стимулирующего выработку грудного молока и подавляющего овуляцию.
* Некоторые опухоли. Опухоль яичников или надпочечников может быть причиной повышения уровня андрогена.
Прежде чем диагностировать поликистоз яичников, врач исключает вероятность этих заболеваний.
Многие женщины с ПЯ страдают ожирением. Распределение жировых отложений влияет на тяжесть симптомов поликистоза яичников. По результатам одного из исследований, в организме женщин, у которых избыточный вес сосредоточен в центральной части туловища, уровень андрогена, сахара и липидов выше, чем в организме тех, у которых лишний вес сосредоточен на конечностях.
Также с поликистозом яичников связаны такие заболевания как:
* Бесплодие
* Акантокератодермия — потемнение кожи на затылке, в подмышечных впадинах, с внутренней стороны бедер, в паху или под молочными железами
* Синдром хронической тазовой боли
Диагностика
УЗИ позволяет обнаружить поликистоз яичников. Яичники увеличены в размерах, содержат множественные кисты, нет ДФ, капсула яичников уплотнена (гипертекоз). Однако, не всем женщинам с кистами яичников ставят диагноз «поликистоз яичников» и наоборот — при ПЯ кисты могут выглядеть нормальными. Поэтому ПЯ диагностируют не только на основе результатов УЗИ, но и при наличии других симптомов — нарушения менструального цикла и гормонального дисбаланса.
При исследовании крови на гормоны обнаруживается избыток андрогенов, пролактина, дисбаланс ФСГ\ЛГ и другие нарушения. Могут быть понижены гормоны Т3 и Т4 (щитовидной железы).
Внешние признаки женщины: акне, усиленный волосяной покров, сальность кожи и волос, ожирение косвенно указывают на поликистоз.
Нарушение менструального цикла: длительные задержки, отсутствие месячных.
Лечение
Лечение может проводиться с помощью лекарственных препаратов или хирургическим методом. Гормональные средства, стимулирующие овуляцию, назначаются исключительно врачом, заранее разработавшим индивидуальную схему лечения. Если медикаментозный метод не принес желаемых результатов, то прибегают к оперативному вмешательству.
В настоящее время лечение поликистоза наиболее часто проводят методом лапараскопии, благодаря щадящему проведению операции у пациенток не возникает спаек и других послеоперационных осложнений, которые нередко бывают при других способах хирургического вмешательства. Однако, после лапараскопии необходима гормональная терапия для получения стойкого положительного результата.
Поделись статьей!
Еще статьи на эту тему
Теги: бесплодие, гормон, менструация, овуляция, ожирение, плод
Рубрика: Акушерство и Гинекология
medpractik.ru