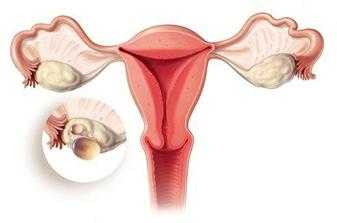
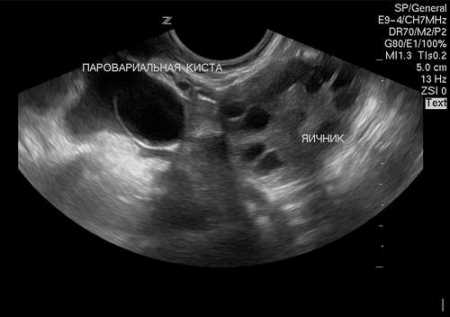
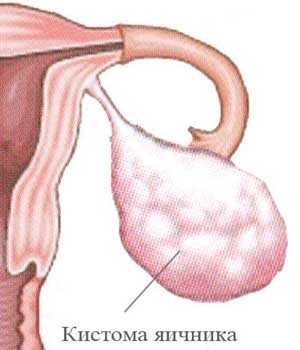
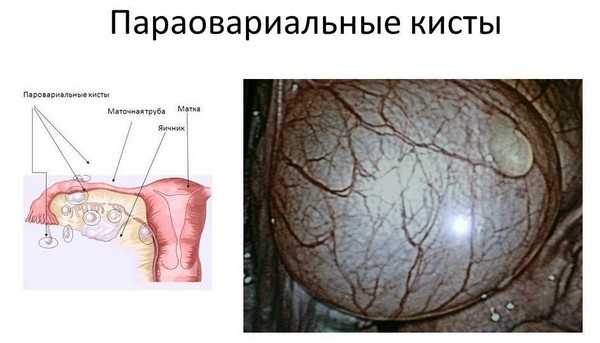
Пограничные опухоли яичников
Пограничные опухоли яичников
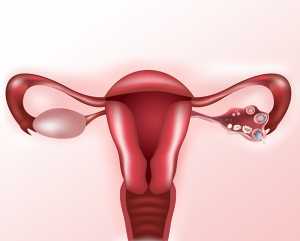
В яичниках встречаются доброкачественные, злокачественные и пограничные опухоли. Доброкачественные опухоли обычно не трансформируются в злокачественные, но могут вызывать боли и перекруты сосудов яичника, а в некоторых случаях могут протекать вообще без симптомов.
Злокачественные опухоли часто ведут себя агрессивно, быстро прогрессируют и дают метастазы. Они требуют комплексного лечения – радикальных операций и химиотерапии до и (или) после операции. Пограничные опухоли среди новообразований яичников занимают особое место – само название хорошо описывает суть этого заболевания, они имеют некоторые черты и злокачественных, и доброкачественных опухолей. Технически они не относятся к доброкачественным и сопровождаются частыми рецидивами при выборе органосохраняющего лечения, но еще и не являются злокачественными и не требуют химиотерапии. Пограничные опухоли коварны тем, что поражают чаще молодых женщин 30–45 лет, очень часто еще не успевших реализовать свою репродуктивную функцию.
Зачастую при пограничных опухолях специфические симптомы не наблюдаются, что осложняет их диагностику. Как правило, они выявляются впервые по данным гистологии удаленной кисты, когда хирург-гинеколог выполняет операцию по поводу предположительно доброкачественных кист яичников. Если киста выглядит подозрительно на предмет злокачественности, всегда требуется выполнение экспресс-гистологии во время операции, и при подтверждении диагноза в операционную вызывается онкогинеколог, который выполняет лапароскопическое удаление сальника и дополнительные биопсии. Такая тактика помогает пациенткам избежать второй операции и повторного наркоза.Факты и риски
Приблизительно 10% пограничных опухолей яичников перерождаются в злокачественные новообразования при рецидиве. Это означает, что опухоль, которая по данным гистологического исследования ранее являлась пограничной, через некоторое время возвращается, но уже как злокачественная. К сожалению, даже самые современные диагностические технологии (такие как УЗИ, КТ, МРТ, онкомаркеры) не позволяют поставить диагноз «пограничная опухоль» со 100% точностью до операции. Внешне пограничные новообразования могут выглядеть и как доброкачественные, и как злокачественные, и только интраоперационная или послеоперационная гистология смогут точно определить диагноз. Также нет специфических симптомов, по которым врач мог бы поставить диагноз опухоли яичника, если только опухоли не становятся очень крупными и не оказывают давление на соседние органы, что происходит в случае пограничных опухолей крайне редко.Хирургическое лечение в ЕМС
Понимая, что каждая десятая пациентка погибнет от рецидива пограничной опухоли, врачи сегодня с гораздо большей настороженностью относятся к каждому случаю этого заболевания. Молодым женщинам мы проводим органосохраняющие операции, чтобы пациентки в дальнейшем были готовы к деторождению и сохранили гормональную функцию. Такие методы лечения не ухудшают прогноз заболевания для жизни женщины, но сопряжены с более высокими рисками рецидивов – до 40–50%. Такие рецидивы требуют повторной и, нередко, не единственной операции. Однако в подавляющем большинстве случаев, даже при необходимости расширения объема операции, такие вмешательства должны проводиться лапароскопически – это мировой стандарт, которому мы следуем в Европейском медицинском центре. К сожалению, этого нельзя сказать про большинство онкологических учреждений России, где лапароскопия в таких случаях не проводится. Полостные же операции при пограничных опухолях – скорее, исключение, чем правило.Если у пациентки еще не было беременности и родов, мы в ЕМС рекомендуем органосохраняющие операции, и даже если возник рецидив, и мы вынуждены проводить повторные лапароскопические операции, обычно есть возможность сохранения части яичника для последующей стимуляции овуляции врачом-репродуктологом в протоколе ЭКО. Мы получаем яйцеклетки для криоконсервации (заморозки) и дальнейшего их оплодотворения перед возможным наступлением следующего (второго, третьего и т.д.) рецидива, который уже может потребовать полного удаления оставшегося яичника. Таким образом, матка при этом заболевании у молодых женщин практически никогда не удаляется даже при распространенных формах пограничных опухолей. Такие пациентки уже через несколько месяцев после операции могут беременеть и самостоятельно вынашивать своего биологически родного ребенка.Частые ошибки
Многие клиники в России предлагают проведение химиотерапии в рамках лечения пограничных опухолей яичников после хирургической операции. Это принципиально неверно, потому что данные образования в действительности не отвечают на химиотерапию. Все, что получают женщины от такого лечения, – токсическое воздействие терапии в виде нейропатии (онемения кистей, стоп, снижения слуха и т.д.) и поражения костного мозга. Также доказано, что вероятность рецидивов от химиотерапии не снижается, поэтому все, что требуется в рамках правильного лечения, – это во время операции при подозрительном образовании на яичнике провести гистологическую диагностику, и если она покажет, что перед нами пограничная опухоль, лапароскопически провести необходимые манипуляции для определения стадии и исключения распространения опухоли за пределы яичника.Мы в ЕМС не предлагаем нашим пациенткам с пограничными опухолями химиотерапию и не проводим радикальные операции по поводу пограничных опухолей, когда удаляются оба яичника вместе с придатками и маткой, если речь идет о молодых женщинах с еще функционирующими яичниками.
Европейский Медицинский Центр +7 (495) 933-66-55. КРУГЛОСУТОЧНО
emc-group.livejournal.com
Пограничные опухоли яичников: современный взгляд на проблему
Пограничные опухоли яичников: современный взгляд
на проблему
И.Ю. Давыдова, В.В. Кузнецов, А.И. Карселадзе, Л.А. Мещерякова
ФГБУ«РОНЦ им. Н.Н. Блохина» РАМН, Москва
Контакты: Ирина Юрьевна Давыдова davydova06@mail.ru
В статье изложены общие положения по проблеме диагностики, лечения и прогноза пограничных опухолей яичников, основанные на современных литературных данных. Правильно установленный диагноз позволит выполнить адекватный и в то же время органосохраняющий объем хирургического вмешательства, благодаря которому будут сохранены репродуктивная и эндокринная функции. Обсуждены вопросы нецелесообразности химиотерапии, по-прежнему применяемой в некоторых лечебных учреждениях пациенткам с пограничными опухолями яичников.
Ключевые слова: пограничные опухоли яичников, серозные пограничные опухоли, инвазивные импланты, неинвазивные импланты
Borderline ovarian tumors: а modern view of the problem
I.Yu. Davydova, V.V. Kuznetsov, A.I. Karseladze, L.A. Meshcheryakova
N.N. Blokhin Russian Cancer Research Center, Russian Academy of Medical Sciences, Moscow
To paper describes the general provisions of the diagnosis, treatment, and prognosis of borderline ovarian tumors, which are based on current literature data. Their correct diagnosis will be able to perform adequate and at the same time organ-sparing surgery volume that will be responsible for preserving reproductive and endocrine functions. Whether chemotherapy used as usual in patients with borderline ovarian tumors in some healthcare facilities is unadvisable is discussed.
Key words: borderline ovarian tumors, serous borderline tumors, invasive implants, noninvasive implants
Пограничные опухоли яичников (ПОЯ) были впервые выделены в отдельную нозологическую группу ВОЗ и FIGO в начале 70-х годов XX столетия. Этиология их неизвестна, однако к факторам, влияющим на возникновение ПОЯ, можно отнести: прием оральных контрацептивов, менархе, возраст первой беременности и первых родов, менструальную функцию, курение, семейный анамнез рака яичников.
Пограничные опухоли составляют 15—20 % всех эпителиальных новообразований яичников у женщин более молодого возраста по сравнению с больными раком яичников (в среднем на 10 лет). В последнее время число пациенток с ПОЯ увеличилось. Это объясняется прежде всего совершенствованием диагностики. Однако, по мнению ряда авторов, для развития ПОЯ отсутствует протективный эффект применяемых оральных контрацептивов [1]. В отличие от рака яичников ПОЯ диагностируют в основном на начальных стадиях заболевания.
Отличительной особенностью ПОЯ является наличие пролиферации эпителиальных структур без деструктивной стромальной инвазии. Морфологически этому типу опухоли присущи некоторые признаки злокачественности: пролиферация эпителия, формирование многослойных солидных структур, увеличение числа митозов, ядерная атипия.
Классификация ПОЯ соответствует таковой при раке яичников (FIGO). Важным достоверным прогностическим фактором является тип имплантов ПОЯ (инвазивный или неинвазивный).
Патогномоничных признаков заболевания нет, точный диагноз устанавливается только после гистологического исследования удаленной опухоли. Несмотря на противоречивость мнений авторов относительно стадирования, многие клиницисты рекомендуют выполнять полноценное хирургическое стадирование при удалении первичной опухоли: биопсию тазовой брюшины, мочевого пузыря, стенок таза, дугласова пространства, а также латеральных каналов брюшинной полости, диафрагмы, висцеральной брюшины тонкой и толстой кишки, брыжейки, подвздошных и поясничных лимфатических узлов. Также необходимо выполнять резекцию большого сальника [2].
Морфологически установить ПОЯ исследованием замороженных срезов удается только опытным специалистам, правильный диагноз, по данным разных авторов, устанавливается только в 58—86 % случаев. С другой стороны, ни одним из существующих лабораторных и инструментальных методов исследований однозначно диагностировать ПОЯ невозможно. Таким образом, только тщательное гистологическое исследование удаленной опухоли опытным морфологом по-
зволит диагностировать ПОЯ и выбрать адекватную тактику лечения.
В целом прогноз при ПОЯ хороший. У 60 % больных встречается I стадия заболевания на этапе первичного обследования. Проведение послеоперационной химиотерапии нецелесообразно. То же можно сказать и о повторной операции после нерадикально выполненного вмешательства: если целью является только стадирование, то, скорее всего, выполнять повторное хирургическое вмешательство не следует [2, 3]. Адекватное стадирование может оказаться полезным только для определения прогноза заболевания. Так, в исследовании M. Romeo et al. было показано, что рецидивы ПОЯ при I стадии возникали только у больных, которым не проводилось полноценного хирургического стадирования [4]. Приблизительно 95 % всех ПОЯ диплоидны, что подтверждается хорошим прогнозом. В случаях, когда опухоль анеуплоидна, вероятность развития рецидива заболевания возрастает. Некоторые авторы считают, что подходы к лечению анеуплоидных ПОЯ должны быть такими же, как и при высокодиф-ференцированной аденокарциноме яичников. Несмотря на то что гиперэкспрессия HER-2 и позитивный ген ТР53 всегда ассоциируются с худшим прогнозом при злокачественных новообразованиях, при ПОЯ такой закономерности не наблюдается.
Рецидивы при I стадии ПОЯ происходят в 15 % наблюдений, хотя это не влияет на 5-летнюю выживаемость, которая соответствует 100 %. Что касается 10-летней выживаемости, то она снижается до 90— 95 % в зависимости от гистологических особенностей опухоли. При II—IV стадиях ПОЯ зависимость прямо пропорциональная — с повышением стадии заболевания прогноз становится хуже. Кроме того, факторами, влияющими на выживаемость, считаются возраст больных и наличие инвазивных имплантов. В опубликованных результатах исследований показано, что у пациентов с неинвазивными имплантами рецидивы встречались в 20 % случаев, летальные исходы — в 7 %. Если рецидив был представлен пограничной опухолью, то в среднем он диагностировался через 3 года от начала заболевания. В случаях, когда рецидивная опухоль представляла собой инвазивный рак яичников, в основном ее обнаруживали через 8 лет от начала заболевания. Уровень СА-125 не превышал нормальных значений у 65 % пациентов с рецидивом д. ПОЯ. Летальные исходы встречались только в случаях, = когда рецидивная опухоль представляла собой инва-^ зивную карциному. Основываясь на исследованиях ^ D.M. Gershenson et al., у пациенток с инвазивными ® имплантами частота рецидивов была высокой и соот-as ветствовала 31—45 %, у большинства больных рецидив = возникал приблизительно через 2 года от начала заболевания. При радикальных операциях без остаточной опухоли безрецидивный период был достоверно боль-
ше по сравнению с операциями с макроскопически определяемой остаточной опухолью. Платиносодер-жащая химиотерапия, проводимая после операции, достоверно ухудшала безрецидивную выживаемость. Однако авторы исследования считают, что столь неожиданные результаты могут быть связаны с возможными статистическими погрешностями.
D.M. Gershenson et al. пришли к выводу, что существенные для злокачественных опухолей яичников прогностические факторы и общепринятые факторы прогноза для пограничных опухолей на самом деле никакого прогностического значения в отношении ПОЯ не имеют. К ним авторы отнесли возраст, стадию заболевания, объем операции, послеоперационную химиотерапию, наличие неинвазивных имплантов и даже некоторое количество инвазивных имплантов. Достоверного влияния гистологического типа ПОЯ, муцинозного или серозного, также отмечено не было. Муцинозные ПОЯ в большинстве случаев наблюдались в I стадии заболевания и практически никогда не сочетались с имплантами [5].
Поскольку в целом прогноз при ПОЯ хороший и заболевание встречается в основном у женщин репродуктивного возраста, закономерным требованием к лечению больных ПОЯ является выполнение орга-носохраняющих операций. Частота рецидивов при резекции яичника или цистэктомии более чем в 2 раза (58 %) выше, чем при аднексэктомии (23 %). Выполнять резекцию контрлатерального яичника следует только тогда, когда он изменен и подозрителен в отношении опухоли. По данным различных исследований, после органосохраняющих операций больные, желающие сохранить фертильность, способны беременеть и рожать здоровых детей. Так, в одном исследовании наблюдалось 256 беременностей, у 206 больных, пытавшихся забеременеть, доля наступивших беременностей составила 48 % [5].
Больным, находящимся в менопаузе, рекомендуется выполнять экстирпацию матки с придатками. Удаление большого сальника всегда должно сопровождать органосохраняющий или полный объем хирургического вмешательства. При распространенной форме ПОЯ по возможности необходимо удалять все видимые опухолевые образования — только такой объем позволит достигнуть хороших результатов.
Поскольку немаловажным аспектом с точки зрения прогноза является тип имплантов, то всегда следует уточнять их характер у морфологов.
Дискуссии о целесообразности химиотерапии ведутся на протяжении нескольких десятков лет. В лечении ПОЯ применялись различные режимы химиотерапии, и ни один из них не показал значимых результатов. Некоторые авторы рекомендуют применять платино-содержащие режимы у пациенток с инвазивными им-
плантами, так как их наличие прогностически неблагоприятно.
Таким образом, мы считаем, что в целом больным ПОЯ химиотерапию проводить не следует. Если присутствуют неинвазивные импланты, то химиотерапия
нецелесообразна, а при инвазивных имплантах вопрос остается открытым. Ни одно из рандомизированных исследований не показало преимущества проведения химиотерапии пациенткам с инвазивны-ми имплантами.
1. Sklrnisdottir I., Garmo H., Wilander E., Holmberg L. Borderline ovarian tumors
in Sweden 1960—2005: trends in incidence and age at diagnosis compared to ovarian cancer. Int J Cancer 2008;123(8):1897-901.
2. Lin P.S., Gershenson D.M., Bevers M.W. et al. The current status of surgical staging of ovarian serous borderline tumors. Cancer 1999;85(4):905-11.
ЛИТЕРАТУРА
3. Cadron I., Leunen K., Van Gorp T. et al. Management of borderline ovarian neoplasms. J Clin Oncol 2007;25(20): 2928-37.
4. Romeo M., Pons F., Barretina P., Radua J. Incomplete staging surgery as a major predictor of relapse of borderline ovarian tumor. World J Surg Oncol 2013;11:13.
5. Gershenson D.M., Silva E.G., Levy L. et al. Ovarian serous borderline tumors with invasive peritoneal implants. Cancer 1998;82(6):1096-103.
6. Swanton A, Bankhead C.R., Kehoe S. Pregnancy rates after conservative treatment for borderline ovarian tumours: a systematic review. Eur J Obstet Gynecol Reprod Biol 2007;135(1):3-7.
cyberleninka.ru
ЛЕЧЕНИЕ ПОГРАНИЧНЫХ ЭПИТЕЛИАЛЬНЫХ ОПУХОЛЕЙ ЯИЧНИКОВ
Пограничные эпителиальные опухоли яичников – также называются эпителиальные опухоли с низким потенциалом злокачественности (НЗП) или атипичными пролиферирующими.
При УЗИ или КТ данные опухоли неотличимы от инвазивного эпителиального рака яичников. Для того чтобы провести различие между данными опухолями, необходима биопсия. Обычно биоптат забирается во время операции.
Операции при опухолях с низким потенциалом злокачественности (НПЗ) проводятся так же, как и при инвазивном раке яичников.
Цель хирургического лечения: удаление опухоли и определение ее стадии.
У женщин, которые больше не хотят иметь детей, также удаляется матка, маточные трубы и яичники.
Интраоперационное стадирование проводится для определения выхода опухоли за пределы яичников или малого таза.
При этом удаляется сальник и часть лимфатических узлов, и проводятся смывы с поверхности брюшной полости и таза. Если пациентка в будущем планирует беременность, то удаляется только яичник с опухолью и маточная труба на стороне поражения. В редких случаях проводится удаление одной лишь опухоли.
Для определения распространенности опухоли необходимо установить ее стадию.
Если опухоль находится в пределах яичника, то назначается динамическое наблюдение без последующего лечения. Специалисты рекомендует проводить обследование каждые 6 месяцев в течение первых 5 лет после постановки диагноза.
Химиотерапия и лучевая терапия в случае опухоли, не выходящей за границы яичника, как исходное лечение обычно не назначаются.
Если на момент диагностики опухоль уже распространилась за пределы яичника, то хирург старается удалить максимально возможный объем опухоли (проводит циторедукцию).
Послеоперационное лечение зависит от наличия инвазии.
Опасность раковых опухолей заключается в их способности проникать в другие ткани.
Инвазия - это процесс, в ходе которого клетки одного типа проникает в органы или ткани, которым они не принадлежат.
При распространении опухолей с НПЗ на оболочке брюшной полости (брюшине) и на поверхности органов малого таза и брюшной полости образуются скопления опухолевых клеток. Чаще всего данные скопления является неинвазивными, то есть не прорастают в брюшину или другие органы. Если опухолевые клетки проникают в брюшину или внутренние органы, то опухоль называется инвазивной.
После проведения циторедуктивной операции пациентки с неинвазивными скоплениями опухолевых клеток обычно наблюдаются без дополнительного лечения.
При наличии инвазии может потребоваться химиотерапия. Схема и режим химиотерапии не отличаются от таковых при инвазивном раке яичников.
Нередко в случае опухолей с НПЗ рекомендуется динамическое наблюдение, поскольку данные новообразования растут очень медленно. Даже если они распространяются, то редко приводят к летальному исходу.
Если после исходного хирургического удаления отмечается рецидив опухоли, то возможно проведение второй циторедуктивной операции.
При рецидивирующих опухолях с НПЗ также используется химиотерапия и, редко, лучевое лечение.
ichilov.net
Пограничные опухоли яичников
Пограничные эпителиальные опухоли имею низкую потенциальную злокачественность. Большинство заболевших женщин пременопаузального возраста. Для диплоидных типов данных опухолей прогноз удовлетворительный, при анеуплоидных и полиплоидных опухолях – прогноз неблагоприятный, клиническое течение сходно с раком яичников.
Лечение пограничных опухолей яичников хирургическое в объеме экстирпации матки с придатками и оментэктомией, как при раке яичников.
Клиника рака яичников
Клиника рака яичников многообразна и зависит от гистологического типа опухоли. Преобладают эпителиальные карциномы (80%), которые не имеет ярко выраженной клинической картины. Характерны симптомы, связанные непосредственно с растущей опухолью: натяжение связок яичника и развитие в связи с этим болевого синдрома, увеличение живота в объеме, изменение его конфигурации, выпячивание опухоли.
При перекручивании “ножки” опухоли, нарушении трофики опухоли, разрыве капсулы развиваются симптомы “острого” живота и внутрибрюшного кровотечения.
При давлении опухоли на мочевой пузырь и прямую кишку появляются дизурические расстройства и нарушение акта дефекации.
Прорастание опухоли капсулы яичника приводит к быстрой диссеминации по брюшине, поражению большого сальника. Внутрибрюшинные опухолевые конгломераты врастают в петли тонкого кишечника и толстую кишку, приводя к развитию частичной или полной кишечной непроходимости.
У большей половины больных развивается асцит, что приводит к быстрому увеличению живота в объеме, чувству распирания, одышке, появлению отеков нижних конечностей. Распространение опухоли на плевру приводит к болевому синдрому в грудной клетке, а развитие гидроторакса сопровождается дыхательной недостаточностью.
По мере роста опухоли и увеличения ее массы развивается как опухолевая интоксикация, так и интоксикация, связанная с местным нарушением трофики и нарушениями функции кишечника и мочевыделительной системы. Интоксикационный синдром, а также потеря белка с асцитом, наряду с усиленным катаболизмом белков, приводит к похудению больных и потере массы тела.
У 30-35 % больных эпителиальным раком яичников могут наблюдаться маточные кровотечения, связанные с нарушением функции яичников.
При опухолях стромы полового тяжа развиваются симптомы феминизации и дефеминизации (вирильный синдром) из-за продукции эстрогенов или андрогенов.
Гранулезостромальноклеточная опухоль, текома продуцируют эстрогенные гормоны, что может приводить у девочек к преждевременному половому созреванию, увеличению молочных желез, появлению вторичных половых признаков. В репродуктивном возрасте характерно нарушение менструального цикла, гиперполименорея, менометроррагии. У женщин в пременопаузе увеличивается возраст наступления менопаузального периода. У женщин менопаузального периода возобновляются циклические кровотечения, метроррагии. Пожилые женщины выглядят моложе своих лет, отмечают повышение либидо.
Андробластома сопровождается продукцией андрогенов, в связи с чем в клиническом течении преобладают признаки дефеминизации и вирилизации: развивается гипоменструальный синдром и аменорея, отмечается снижение либидо, рост волос по мужскому типу, грубеет голос, меняются черты лица и весь облик женщины.
Диагностика рака яичников
Диагностика включает морфологическую верификацию опухоли, определение местной распространенности опухолевого процесса, выявление отдаленных метастазов и оценку функционального состояния органов и систем пациентки.
На первом этапе применяется ректовагинальный осмотр и УЗИ органов малого таза. На втором этапе используются методы углубленной диагностики:
1. Цитологический исследование биопсийного материала, полученного при пункции тонкой иглой заднего свода влагалища, плевральной полости, опухолевых конгломератов, лимфоузлов.
2. Ультразвуковой метод позволяет дифференцировать солидные опухоли с жидкостными включениями, визуализировать кистозные образования, не пальпируемые при ректовагинальном исследовании, проводить пункцию метастатических забрюшинных лимфоузлов.
3. Рентгенологические методы при раке яичников используются для исследования органов грудной клетки, желудка, кишечника и других органов брюшной полости и малого таза с целью определения распространенности процесса.
4. Раздельное диагностическое выскабливание матки с гистологическим исследованием при кровянистых выделениях из влагалища.
5. Диагностическая лапароскопия позволяет определить объем поражения и получить материал для морфологического исследования.
6. Для диагностики эпителиальных опухолей используют опухолевые маркеры – раково-эмбриональный антиген и опухолево-специфический антиген СА-125, которые также применяют для определения наступления ремиссии или рецидива. Больным до 30 лет необходимо определять бета-хорионический гонадотропин и альфа-фетопротеин.
Лечебная тактика
После установления стадии заболевания и верификации диагноза проводится специальное лечение. Хирургическое лечение является обязательным в большинстве случаев и первым этапом комбинированного и комплексного лечения больных раком яичников.
Диспансеризация
В течение первых двух лет после завершения специального лечения больная проходит контрольное обследование каждые 3 месяца, третий год – 1 раз в 4 месяца, в последующем – 1 раз в год пожизненно.
Больная направляется на МРЭК в установленные сроки для решения вопроса о трудоспособности и установления группы инвалидности в зависимости от стадии и прогноза заболевания.
Прогноз. Рак яичников является самой агрессивной онкогинекологической опухолью. Пятилетняя выживаемость больных раком яичников III стадии колеблется в пределах 15-20 %, а при IV стадии снижается до 5 % и менее. Наиболее важным прогностическим фактором после циторедуктивных операций при распространенном раке яичников является объем оставшихся опухолевых масс. Отдаленные результаты при I стадии составляют 72-80 %, при II стадии – 46-78 %.
Советы врачу-общей практики:
7. При жалобах на боли внизу живота, в пояснично-крестцовой области, кровотечениях из влагалища и гормональных нарушениях направить больную к гинекологу для углубленного обследования.
8. При выявлении любых образований и процессов в яичниках направить больную в специализированное онкологическое учреждение.
9. Больных с факторами риска направлять для углубленного обследования в специализированное учреждение.
Советы пациенту
После проведенного специального лечения больному необходимо выполнять рекомендации онколога:
· Проходить контрольный осмотр в установленные сроки.
· Нормализовать образ жизни, распорядок дня, режим питания.
Всем женщинам проходить ежегодно профилактические обследования с обязательным гинекологическим осмотром.
Рак влагалища
Заболеваемость
Первичный рак влагалища встречается редко, составляя 1-2 % по отношению ко всем злокачественным опухолям женских половых органов, его распространенность существенно ниже 1 случая на 100 000 женщин. Рак влагалища встречается в любом возрасте, но чаще болеют женщины после 50 лет.
Этиология и факторы риска
В этиопатогенезе рака влагалища можно выделить несколько ведущих факторов, коррелирующих с возрастом, иммуносупрессией, экзогенными инфекциями.
Основной причиной развития первичного рака влагалища у женщин молодого возраста может быть признана папилломавирусная и герпесвирусная инфекция, вызывающая многофокусное поражение слизистой верхних отделов влагалища и шейки матки. У больных раком влагалища определяются как вирусы папилломы человека высокого онкогенного риска, более характерные для рака шейки матки, так и мутации гена p 53, которые чаще диагностируются при раке вульвы.
В пожилом возрасте на первое место выходят гормональные нарушения, инволютивные и дистрофические процессы в постменопаузальном периоде.
Доказана роль облучения в патогенезе рака влагалища. Относительный риск развития рака влагалища после сочетанного лучевого лечения по поводу рака шейки матки в 300 раз больше, чем в общей популяции.
cyberpedia.su