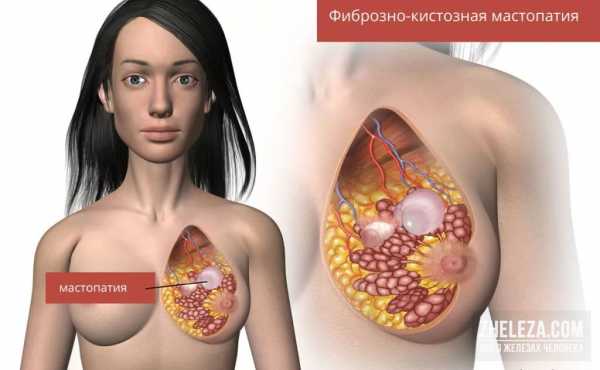
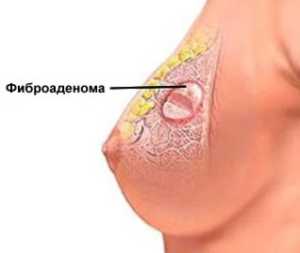
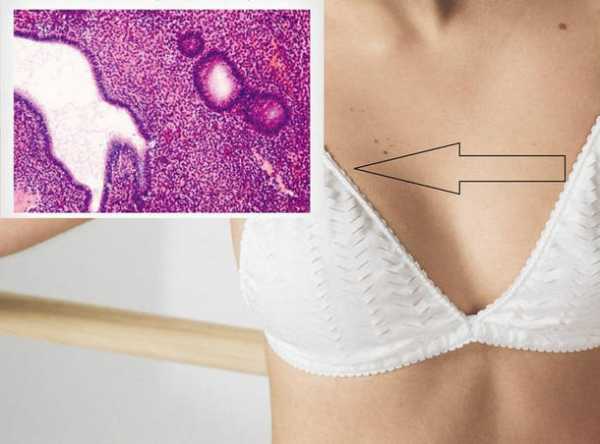
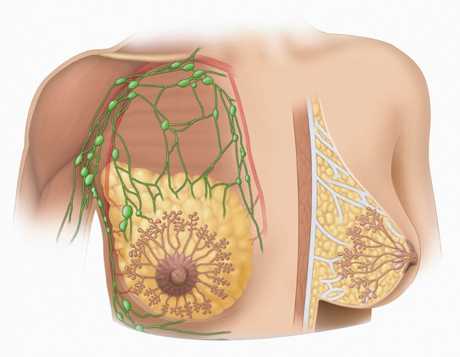
Гистофизиология молочной железы нейроэндокринная регуляция лактации
Нейроэндокринная регуляция лактации
Во время кормления ребёнка раздражение чувствительных нервных окончаний соска молочной железы при сосании передаётся в ЦНС по восходящим путям (рис. 20–19) до содержащих активин нейронов ядра одиночного пути (nucleus tractus solitarii) и далее — до крупноклеточной части супраоптического и паравентрикулярного ядер. Эта афферентная импульсация в сочетании с нисходящими влияниями со стороны высших отделов головного мозга в конечном итоге достигает гипоталамуса и приводит к различным нейроэндокринным эффектам, относящимся к изменению режима секреции пролактина, окситоцина и гонадолиберина, определяющих и лактацию, и функцию яичников (овариальный цикл).
Рис. 20–19. Нейроэндокринные рефлексы, инициируемые сосанием груди
Пролактин. В нейросекреторных нейронах дугового ядра (n. arcuatus) афферентная импульсация подавляет секрецию дофамина. Поскольку дофамин в аденогипофизе блокирует секрецию пролактина, то угнетение секреции дофамина увеличивает секрецию пролактина. Таким образом, кормление приводит к резкому, но кратковременному возрастанию секреции пролактина. Этот транзиторный всплеск секреции пролактина приводит к образованию молока для следующего кормления.
У кормящих грудью женщин концентрация пролактина остаётся повышенной в течение 4–6 нед после родов, после чего уровень пролактина уменьшается до показателей, характерных для небеременных женщин. Приблизительно в течение 2 мес после родов сосание ребёнка вызывает всплески секреции пролактина, но этот рефлекс неуклонно затухает даже в том случае, если ежедневная секреция молока превышает 1 л.
Курение ингибирует выброс пролактина, что вызывает снижение секреции молока.
Окситоцин. Афферентная импульсация к паравентрикулярному (n. paraventricularis) и супраоптического (n. supraopticus) ядрам гипоталамуса стимулирует синтез, транспорт и секрецию окситоцина. Окситоцин вызывает сокращение миоэпителиальных клеток секреторных отделов молочной железы и тем самым способствует продвижению молока в выводные протоки. У кормящих матерей спонтанная секреция окситоцина происходит также во время игры с ребёнком или при его плаче.
Гонадолиберин. В нейронах дугового ядра (n. arcuatus) афферентная импульсация подавляет синтез и секрецию гонадолиберина. В результате ингибируется секреция ФСГ и лютропина, т.е. блокируется овариальный цикл. Другими словами, лактация предупреждает овуляцию и нормальный менструальный цикл. Если же родильница не сама вскармливает ребёнка, овариально–менструальный цикл восстанавливается примерно через 10 нед.
Физиология новорождённого
Период новорождённости (неонатальный период) продолжается 4 нед. В течение этого периода происходит адаптация организма новорождённого к условиям самостоятельного существования. Адаптация касается всех органов и систем, но в наибольшей степени относится к перестройке кровообращения, началу функционирования органов дыхания и ЖКТ, необходимости гомеостатического поддержания таких жизненно важных функций как постоянство температуры тела, кислотно–щелочное равновесие (КЩР) и других параметров гомеостаза, ранее обеспечивавшихся плацентой (например, функций почек, печени, иммунной системы).
studfiles.net
Нейроэндокринная регуляция лактации
Во время кормления ребёнка раздражение чувствительных нервных окончаний соска молочной железы при сосании передаётся в ЦНС по восходящим путям (рис. 20–19) до содержащих активин нейронов ядра одиночного пути (nucleus tractus solitarii) и далее — до крупноклеточной части супраоптического и паравентрикулярного ядер. Эта афферентная импульсация в сочетании с нисходящими влияниями со стороны высших отделов головного мозга в конечном итоге достигает гипоталамуса и приводит к различным нейроэндокринным эффектам, относящимся к изменению режима секреции пролактина, окситоцина и гонадолиберина, определяющих и лактацию, и функцию яичников (овариальный цикл).
Рис. 20–19. Нейроэндокринные рефлексы, инициируемые сосанием груди
Пролактин. В нейросекреторных нейронах дугового ядра (n. arcuatus) афферентная импульсация подавляет секрецию дофамина. Поскольку дофамин в аденогипофизе блокирует секрецию пролактина, то угнетение секреции дофамина увеличивает секрецию пролактина. Таким образом, кормление приводит к резкому, но кратковременному возрастанию секреции пролактина. Этот транзиторный всплеск секреции пролактина приводит к образованию молока для следующего кормления.
У кормящих грудью женщин концентрация пролактина остаётся повышенной в течение 4–6 нед после родов, после чего уровень пролактина уменьшается до показателей, характерных для небеременных женщин. Приблизительно в течение 2 мес после родов сосание ребёнка вызывает всплески секреции пролактина, но этот рефлекс неуклонно затухает даже в том случае, если ежедневная секреция молока превышает 1 л.
Курение ингибирует выброс пролактина, что вызывает снижение секреции молока.
Окситоцин. Афферентная импульсация к паравентрикулярному (n. paraventricularis) и супраоптического (n. supraopticus) ядрам гипоталамуса стимулирует синтез, транспорт и секрецию окситоцина. Окситоцин вызывает сокращение миоэпителиальных клеток секреторных отделов молочной железы и тем самым способствует продвижению молока в выводные протоки. У кормящих матерей спонтанная секреция окситоцина происходит также во время игры с ребёнком или при его плаче.
Гонадолиберин. В нейронах дугового ядра (n. arcuatus) афферентная импульсация подавляет синтез и секрецию гонадолиберина. В результате ингибируется секреция ФСГ и лютропина, т.е. блокируется овариальный цикл. Другими словами, лактация предупреждает овуляцию и нормальный менструальный цикл. Если же родильница не сама вскармливает ребёнка, овариально–менструальный цикл восстанавливается примерно через 10 нед.
Физиология новорождённого
Период новорождённости (неонатальный период) продолжается 4 нед. В течение этого периода происходит адаптация организма новорождённого к условиям самостоятельного существования. Адаптация касается всех органов и систем, но в наибольшей степени относится к перестройке кровообращения, началу функционирования органов дыхания и ЖКТ, необходимости гомеостатического поддержания таких жизненно важных функций как постоянство температуры тела, кислотно–щелочное равновесие (КЩР) и других параметров гомеостаза, ранее обеспечивавшихся плацентой (например, функций почек, печени, иммунной системы).
studfiles.net
Строение молочных желех, особенности желез в период лактации. Эндокринная регуляция желез.
Молочная железа. Молочные железы по своему происхождению представляют видоизмененные кожные потовые железы, т.е. молочные железы имеют эпителиальное происхождение. Но по своему функциональному значению они относятся к женской репродуктивной системе, так как обеспечивают первоначальное питание ребенка. У половозрелой женщины каждая молочная железа состоит из 15-20 отдельных железок, разделенных прослойками рыхлой соединительной и жировой ткани. Эти железы по строению являются сложными альвеолярными, и их выводные протоки открываются на вершине соска. Выводные протоки переходят в молочные синусы, служащие для накапливания молока. Полного развития молочная железа достигает во время беременности. В дольках молочной железы разрастаются альвеолярные ходы, на концах которых формируются альвеолы. Во второй половине беременности железистые клетки начинают вырабатывать секрет и незадолго до родов наступает секреция молозива. Интенсивная секреция полноценного молока устанавливается в течении первых дней после рождения ребенка. Молоко – сложная водная эмульсия, в состав которой входят жировые капельки, белки (лактоглобулины, лактоальбумины), углеводы (лактоза или молочный сахар), соли и вода. В лактоцитах хорошо развита гр и агр ЭПС, много микротубул и микрофиламентов. Опорожнению альвеолы и переходу молока в млечные ходы способствует сокращение звездчатых миоэпителиальных клеток. По окончании периода лактации молочная железа претерпевает инволюцию, однако часть альвеол, образовавшаяся во время предыдущей беременности, сохраняется. В период полового созревания начинается интенсивное развитие молочных желез. Дифференцируются секреторные отделы – альвеолы (ацинусы). В течение полового цикла секркторная активность повышается в период овуляции и снижается во время менструации. Регуляция деятельности функционирующей молочной железы осуществляется: аденогипофизарным пролактином ( лактотропный гормон ), который стимулирует лактацию и окситоцин – под его влиянием происходит выброс секрета из млечного синуса.
Выделительная система
Общая морфо-функциональная характеристика выделительной системы. Почки: основные этапы развития. Строение и кровоснобжение. Нефроны, их разновидности, основные отделы, гисто-физиология. Структурные основы эндокринной функции почек.
Почка является паренхиматозным зональным органом. Снаружи она покрыта капсулой из плотной волокнистой соединительной ткани и серозной оболочки. От капсулы отходят прослойки рыхлой волокнистой неоформленной соединительной ткани, по которым идут сосуды. Почка состоит из коркового и мозгового вещества. Граница между ними неровная: корковое вещество проникает в мозговое в виде колонок Бертини, а мозговое в корковоев виде мозговых лучей Феррейна.
Корковое вещество занимает наружную, поверхностную часть почки и мозговыми лучами Феррейна разделяется на отдельные участки. Участки коркового вещества своей нижней частью внедряются между основаниями мозговых пирамид в мозговое вещество в виде колонок Бертини, отделяя пирамиды друг от друга.
Мозговое вещество образовано мозговыми пирамидами. Их широкие основания повернуты в сторону коркового вещества, вершины пирамид называются сосочками. Они обращены к малым чашечкам, которые далее продолжаются в большие чашечки и затем в почечную лоханку.
Гистофизиология нефрона Структурно-функциональной единицей почки является нефрон.Он состоит из капсулы и переходящих друг в друга канальцевпроксимальных извитого и прямого, дистальных извитого и прямого. В каждой почке около 2 млн нефронов.
По локализации различают: суперфициальные или подкапсульные (около 1 %); корковые (85 %); юкстамедуллярные, или околомозговые (около 14 %).
В нефроне выделяют:
1) капсулу (вместе с сосудистым клубочком формирует почечное тельце Мальпиги); 2) проксимальный извитой отдел; 3)проксимальный прямой отдел; 4) тонкий отдел; 5) дистальный извитой отдел; 6)дистальный прямой отдел.
Дистальные извитые канальцы впадают в собирательные трубочки, которые берут начало в мозговых лучах в корковом веществе, продолжаются в мозговое вещество и на вершине пирамид открываются в сосочковые каналы.
В состав коркового вещества входят следующие структуры:
1) очечные тельца Мальпиги; 2) проксимальные извитые канальцы; 3) дистальные извитые канальцы.
В корковом веществе залегают также компоненты юкстагломерулярного аппарата. В мозговом веществе находятся: проксимальные прямые канальцы, тонкие канальцы, дистальные прямые канальцы, а также в мозговом веществе находятся собирательные трубочки. У корковых нефронов в корковом веществе находятся почечное тельце, проксимальный и дистальный отделы, и только тонкий отдел и восходящая часть петли лежат в мозговом слое. Юкстагломерулярные нефроны имеют очень длинный тонкий сегмент, который состоит из нисходящей и восходящей частей (петля Генле). Они глубоко спускаются в мозговое вещество, в котором лежат также прямые проксимальные и прямые дистальные канальцы. Остальные части нефронов лежат в корковом веществе.
Капсула нефрона, имеющая вид двустенной чаши, и входящие в нее капилляры первичной капиллярной сети образуют почечное тельце Мальпиги. В почечном тельце выделяют сосудистый полюс, находящийся в месте расположения приносящей и выносящей артериол, и мочевой полюс, прилежащий к начальному сегменту проксимального канальца.
Первичная капиллярная сеть лежит между приносящей и выносящей артериолами и содержит около 30 капиллярных петель. Между капиллярными петлями располагается мезангий — соединительная ткань клубочка с особыми мезангиальными клетками и межклеточным веществом. Эндотелий капилляров состоит из сильно уплощенных эндотелиоцитов с фенестрами размером 0,1 мкм. Число фенестр меняется в зависимости от функциональной нагрузки, при этом их площадь может составлять до 30 % от общей площади эндотелиоцитов. Эндотелий лежит на трехслойной базальной мембране, общей для эндотелиоцитов и подоцитов. Наружный и внутренний слои в мембране светлые, а средний — темный. В темном слое находятся микрофибриллы, которые образуют сеть с диаметром около 7 нм. Через эти ячейки в мочу могут попасть только очень мелкие белковые молекулы.
Внутренний (париетальный) листок капсулы нефрона со всех сторон окружает клубочковые капилляры. Этот листок состоит из одного слоя эпителиоцитов, которые называются подоцитами. От тела подоцитов во все стороны отходят крупные отростки цитотрабекулы, а от цитотрабекул — более мелкие отростки — цитоподии. Цитоподии прикрепляются к базальной мембране, между ними имеются фильтрационные щели, через которые натянуты тонкие мембраны с поперечной исчерченностьющелевые диафрагмы.
Эндотелий капилляров, трехслойная мембрана и мембраны между цитоподиями подоцитов образуют фильтрационный (почечный) барьер, через который из плазмы крови фильтруется первичная моча. Этот фильтр пропускает воду, соли, глюкозу, низкомолекулярные белки.
Наружный (париетальный) листок капсулы нефронапредставлен плоскими эпителиоцитами. В области сосудистого полюса он продолжается во внутренний листок. В этом месте наружный листок капсулы окружает сосудистый полюс в виде пояска. Между двумя листками капсулы находится полость капсулы, в которую поступает первичная моча. В области мочевого пояска наружный листок капсулы продолжается в эпителий проксимального отдела нефрона, а полость капсулыв полость проксимального канальца.
В проксимальном отделе нефронавыделяют извитую и прямую части. Проксимальный извитой отдел многократно извивается в корковом веществе. Проксимальный прямой каналец является толстым нисходящим коленом петли нефрона и находится в мозговых лучах и мозговом веществе. Каналец имеет слабо выраженный просвет и образован эпителиальными клетками цилиндрической или кубической формы, лежащими на базальной мембране, а на апикальном полюсе имеют щеточную каемку. Щеточная каемка представлена многочисленными длинными микроворсинками, 30—40 раз увеличивающими всасывающую поверхность клеток.
Проксимальный каналец выполняет следующие функции:
1) облигатное (обязательное) обратное всасывание из первичной мочи в кровь белков и глюкозы; 2) факультативное всасывание воды и минеральных веществ; 3) секреция некоторых органических кислот и оснований; 4) экскреция некоторых экзогенных веществ; 5) биосинтез кальцитриола.
Тонкий отдел нефронаВ корковых нефронах этот отдел имеет нисходящую часть и залегает в основном в мозговых лучах и наружных отделах мозгового вещества, тогда как в юкстагломерулярных нефронах в нем имеются нисходящая и восходящая части. которые спускаются глубоко в мозговое вещество. Тонкий отдел участвует в формировании петли Генле. Его стенка выстлана плоскими клетками, которые имеют глубокие складки цитолеммы.
Функции:
1) пассивная реабсорбция воды из первичной мочи; 2) в восходящей части тонкого отдела юкстагломерулярных нефронов, напротив, непроницаемая для воды, помимо этого происходит диффузия солей.
Дистальный отделделится на дистальный прямой и дистальный извитой канальцы. Дистальный прямой каналец образует восходящее колено петли и входит в состав мозгового вещества и мозговых лучей. Дистальный извитой каналец, многократно извиваясь в корковом веществе, подходит к почечному тельцу, образуя плотное пятно, а затем впадает в собирательную трубку. Дистальный отдел имеет хорошо выраженный просвет, образован кубическими или цилиндрическими клетками.
Функции:
1) в дистальном отделе происходит дополнительная реабсорция электролитов из мочи. Эти процессы идут активно, то есть против градиента концентрации, с затратой энергии; 2) в клетках дистального отдела синтезируется калликреин.
Эндокринная система почек
Она представлена рениновыми и простогландиновым аппаратами.
Рениновый аппарат, или юкстагломерулярный аппарат (ЮГА) – секретирует в кровь активное вещество – ренин. Он катализирует образование в организме ангиотензинов, оказывающих сильное сосудосуживающие действие и также стимулирует продукцию гормона альдостерона в надпочечниках. Кроме того, ЮГА принадлежит важная роль в выработке эритропоэтинов. В состав ЮГА входят:
-юкстагломерулярные клетки (лежат в стенке приносящих и выносящих артериол под эндотелием, имеют овальную или полигональную форму).
-плотное пятно (это участок стенки петли дистального канальца, которым он прилежит к почечному тельцу. Служит осморецептором- реагирует на повышение содержание ионов Na+ в просвете канальца)
-юкставаскулярные (находятся в области сосудистого полюса и дублируют функцию юкстагломерулярных клеток).
Простогландиновый аппарат включает интерстициальные клетки и нефроциты собирающих трубочек.
megalektsii.ru
Гормональная регуляция лактации и некоторых других механизмов выхаживания потомства
10 Августа в 17:56 4623
Гормоны выполняют ведущую роль в регуляции репродуктивных процессов не только на стадиях полового развития, спаривания, беременности и родов, но и в осуществлении выхаживания потомства материнским организмом. Важнейший физиологический механизм выхаживания потомства у млекопитающих — это кормление новорожденных особей молоком матери. Определяющими моментами в реализации этого процесса служат дифференцировка специализированных органов для образования молока — молочных желез, а также сам процесс его образования и секреции — лактация. Оба эти процесса гормонзависимы. Закладка молочных желез из эктодермальных зачатков происходит уже на ранних этапах эмбриогенеза самок и самцов (Паттон, 1969; Рейно, 1971). В дальнейшем рост и развитие желез у мужских особей заторможен Т, у женских же особей на эмбриональных стадиях развития в будущих железах формируется первичный тяж, дающий впоследствии начало протокам. В постэмбриональном периоде у женских особей происходит рост и ветвление железистых протоков, в пубертатном периоде — ускорение роста и дальнейшее ветвление протоков, а также формирование в них альвеол — основных морфофункциональных единиц желез (рис. 85). Альвеолярные клетки зрелой молочной железы вне беременности обладают лишь потенциальной готовностью к лактации, но при этом не функционируют.Рис 85. Основные этапы дифференцировки молочной железы у женских особей млекопитающих: 1 — эмбриональная закладка железы, 2 — гормонзависимая эмбриональная стадия формирования первичного тяжа, 3 — пубертатное гормонзависимое формирование альвеолярного аппарата нелактируюшей железы, 4 — гормонзависимое формирование лактирующей железы при беременности и в послеродовой период; а — протоки, б — альвеолы, в — миоэпитслиальный аппарат, г — сосок
Таким образом, в процессе пубертации осуществляется только начальная дифференцировка железистой структуры, подготавливающая возможность дальнейшего ее развития и функционирования в послеродовой период. В регуляции первого этапа пубертатной дифференцировки молочных желез принимают решающее участие эстрогены, прогестины и пролактин. При этом эстрогены инициируют рост и ветвление протоков и, кроме того, сенсибилизируют их клетки к действию прогестинов и пролактина, стимулирующих формирование альвеолярного аппарата. Вместе с тем эффекты перечисленных гормонов в процессе формирования молочных желез при половом созревании облегчаются и усиливаются СТГ, инсулином, глюкокортикоидами и тиреоидными гормонами. Часть гормональных эффектов может опосредоваться местными эпителиальными факторами роста (Тёркингтон, 1971). При беременности происходит следующий этап развития желез. Под влиянием ряда гормонов осуществляется стимуляция роста и развития активной формы альвеолярного аппарата грудных желез, способного синтезировать специфические факторы молока, формировать его состав и секретировать на начальных стадиях лактации молозиво (коллострум), а затем собственно молоко. Главными инициаторами предлактационной дифференцировки желез являются сначала прогестерон и ХСМ, а затем ЛТГ. Вмете с тем, как показали эксперименты, проведенные in vivo и на культурах тканей, действие этих гормонов подготавливается и пермиссируется инсулином, СТГ и глюкокортикоидами (Блэкстер, 1971; Тёркингтон, 1971, 1973). Прошедшие второй этап дифференцировки молочные железы также под действием гормонов способны активно лактировать и обеспечивать кормление родившегося потомства. В молоке содержатся все вещества, необходимые для нормального существования и развития новорожденных. Среди специфических гормонзависимых факторов молока особо следует отметить белки — казеин (фосфопротеин), а-лактальбумин, в-лактоглобулин, лактоферин, а также дисахарид лактозу. Биосинтез белков и лактозы, а также липидов осуществляется в альвеолярных клетках железы, остальные компоненты поступают из крови. Биосинтез белков в форме предшественников происходит в особых ансамблях полисом, связанных с эндоплазматическим ретикулумом. Синтезируемые белки депонируются в агрегируемой форме в секреторных гранулах и освобождаются из них в протоки под действием гормональных стимулов путем экзоцитоза.Белки молока выполняют важную трофическую функцию для потомства. Вместе с тем а-лактальбумин, находясь в альвеолярных клетках молочной железы, участвует также в синтезе лактозы (рис. 86). Конечные этапы биосинтеза молочного сахара из уридиндифосфогалактозы (активированной галактозы) и глюкозы контролируются специальной ферментной системой — синтетазойлактозы. В молочной железе эта система состоит из ферментов галактозил-трансферазы («белок А»), содержащейся в различных тканях, и а-лактальбумина («белок В»), специфичного для лактирующих молочных желез.
Рис 86. Биосинтез лактозы и белковых компонентов молока и их регуляция в лактирующей молочной железе
Последний сам не обладает каталитической активностью, но специфически повышает сродство «белка А» к глюкозе. В результате «белок А» в молочной железе использует в качестве второго субстрата реакции (первый УДФ-галактоза) не N-ацетилглюкозамин, как в других тканях, не содержащих а-лактальбумин, а глюкозу. Тем самым а-лактальбумин тканеспецифически переключает реакцию с образования N-ацетиллактозамина на синтез лактозы, легко расщепляемой в пищеварительном тракте детеныша. Биосинтез а-лактальбумина и, следовательно, лактозы, а также биосинтез казеина, в-лактоглобулина и лактоферина непосредственно стимулируется пролактином и ХСМ, особенно в присутствии инсулина и СТГ. Все эти эффекты пермиссируются глюкокортикоидами и эстрогенами в низких концентрациях. В то же время прогестерон и особенно тестостерон тормозят образование специфических компонентов молока. Ингибиторный эффект упомянутых стероидов также пермиссируется глюкокортикоидами. Образование специфических факторов молока и собственно лактация как секреторный процесс начинаются еще при беременнести. В это время в небольших количествах секретируется преимущественно молозиво. Обильная секреция молока начинается в первые дни после родов. Эндокринные механизмы лактации могут варьироваться у разных видов животных (Блэкстер, 1971). Однако у всех видов главный стимулятор секреции молока после родов — ЛТГ. Его эффекты усиливаются или пермиссируются теми же гормонами, которые обусловливали дифференцировку железистых клеток и биосинтез молочных факторов во время беременности. Стимуляция секреции ЛТГ гипофизом в послеродовом периоде определяется относительно высоким уровнем эстрогенов и низким содержанием прогестинов в организме кормящей матери. Действие этих половых стероидов на секрецию ЛТГ реализуется через гипоталамус и гипофиз. Лактогенный эффект ЛТГ, как уже упоминалось, усиливается СТГ и пермиссируется глюкокортикоидами. Причиной усиленной секреции этих гормонов является, по-видимому, родовая и послеродовая стрессовая ситуация, возникающая в материнском организме. Наряду с усиленной секрецией глюкокортикоидов в послеродовом периоде происходит снижение синтеза и секреции транскортина печенью (Вестфал, 1970). Вследствие этого концентрация свободной, эффективной формы кортикостероидов возрастает. Данный механизм активации глюкокортикоидных гормонов дополняет усиление секреции гормонов корой надпочечников. Помимо эндокринных факторов стимулятором лактации служит акт сосания молока новорожденными. Сосание оказывает стимулирующий эффект как в результате прямого действия на железу, способствуя выходу молока из железистых клеток, так и рефлекторно через гипоталамические вазомоторные центры, изменяющие кровоток в железе. При этом увеличивается секреция ЛТГ и АКТГ. В увеличении секреции ЛТГ важную роль играет рефлекторное торможение дофаминергических нейронов гипоталамуса. Соответственно дофамин и его агонисты (бромкриптин и а-эргокриптин) ингибируют/секрецию ЛТГ и лактацию (Флинт, Энсор, 1979). На уровень лактации и качество молока у представителей каждого вида влияют факторы питания. Дисбаланс секреции упомянутых гормонов может быть одной из причин развития рака молочной железы (Лазарев, 1969; Мак Гуайр и др., 1976). Особое место в эвакуации молока из лактирующей молочной железы принадлежит окситоцину. Этот гормон усиленно секретируется нейрогипофизом рефлекторно на акт сосания и способствует выходу молока из молочной железы, вызывая сокращение особых миоэпителиальных клеток (см. рис. 86). Обеспечивая усиленную эвакуацию молока из железистых клеток, окситоцин косвенно стимулирует процесс лактации (Мартини, 1965; Тиндал, 1974). Кормление новорожденного потомства на ранних этапах онтогенеза продуктами, образующимися в теле матери, присуще не только млекопитающим, но и некоторым видам птиц. Например, у самок и самцов голубей в конце периода насиживания яиц в нижнем отделе слизистой пищевода гипертрофируются две особые железы (зобные), продуцирующие специфический секрет — голубиное молочко (зобная кашица). Показано, что процессы дифференцировки желез и секреции молочка специфически индуцируются ЛТГ (Риддл, 1931). ЛТГ обусловливает также проявление инстинктов насиживания яиц, кормления птенцов и их обучения. Он важнейший стимулятор различных инстинктов выхаживания потомства не только у птиц, но и у млекопитающих, а также других классов позвоночных. В.Б. Розенmedbe.ru