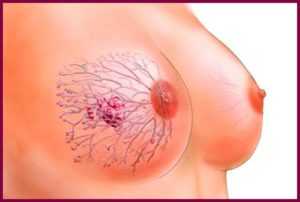
Неоадъювантная химиотерапия при раке молочной железы
Адъювантная химиотерапия при раке молочной железы
Цель адъювантной химиотерапии рака молочной железы — элиминация микрометастазов опухоли, которые могли появиться после или присутствовать до хирургического лечения и не обнаруживаться существующими методами в ходе стадирования заболевания.
В зависимости от стадии и типа опухоли молочной железы использование системной терапии позволяет достичь снижения летальности на 35-72%. Уровень экспрессии рецептора эстрогена (РЭ) и наличие гиперэкспрессии (амплификации) HER2 являются наиболее достоверными предиктивными факторами для выбора адъювантной химиотерапии рака молочной железы. При этом, по данным рекомендаций Европейского общества медицинской онкологии, опухоли с любой определяемой экспрессией РЭ и (или) РП (> 1%) можно считать эндокриночувствительными. Среди других характеристик, которые могут помочь предположить отсутствие чувствительности к эндокрино-терапии, выделяют низкий уровень экспрессии стероидных гормонов, в том числе низкий уровень экспрессии РП, низкую дифференцировку опухоли (G3), высокий уровень экспрессии маркеров пролиферации (Ki67), гиперэкспрессию или амплификацию HER2. При отсутствии описанных выше признаков опухоль можно считать высокочувствительной к эндокринотерапии.
Все опухоли люминальных подтипов в рамках комплексного адъювантного лечения должны получать эндокринотерапию. При этом химиотерапия должна проводиться при люминальном А подтипе только в тех ситуациях, когда ожидаемый риск рецидивирования крайне высок, например при массивном поражении регионарных лимфатических узлов. Отдельно необходимо сказать, что опухоли люминального В подтипа характеризуются разнообразной агрессивностью течения, что определяет крайнюю неточность в определении целесообразности цитостатической терапии в этой группе пациентов. При этом в случае опухоли с экспрессией HER2 люминального В подтипа должна проводиться системная лекарственная терапия с использованием всех известных методов: эндокринотерапии, цитостатической терапии и анти-HER2 терапии.
Больные с признаками эндокриночувствительных опухолей могут получать только эндокринотерапию или комбинацию эндокринотерапии вместе с химиотерапией. При сомнительной чувствительности опухоли к гормональным воздействиям чаще всего предлагается использовать комбинированный подход. Независимо от экспрессии РЭ/ РП в случае наличия гиперэкспрессии/амплификации HER2 больные должны получать таргетную терапию анти-HER2 препаратами. При этом чаще всего схемы с использованием антрациклинов не комбинируются с анти-HER2 препаратами в связи с крайне высоким риском кардиотоксичности.
В каждом случае выбор тактики профилактической лекарственной терапии должен базироваться на потенциальном преимуществе от использования агрессивного лечения, возможных осложнений лечения и предпочтениях больного.
У больных репродуктивного возраста стандартом адъювантной эндокринотерапии является монотерапия тамоксифеном 20 мг/сут в течение 5-10 лет или его комбинация с подавлением функции яичников. При этом подавление функции яичников может быть достигнуто либо билатеральной овариэктомией, либо при помощи ингибиторов гонадотропин-рилизинг гормонов. При этом последние должны использоваться не менее 2 лет.
В случае постменопаузы стандартный подход включает использование ингибиторов ароматазы (ИА) в течение 5 лет или последовательное использование тамоксифена в течение 3 лет с последующим переходом на ИА.
Адъювантная химиотерапия рака молочной железы рекомендована пациентам с отсутствующей или неопределенной эндокриночувствительностью, а также пациентам с гиперэкспрессией (амплификацией) HER2. При этом наибольшие преимущества от проведения цитостатической адъювантной терапии достигаются именно в группе опухолей без экспрессии РЭ. При этом в группе РЭ+ РМЖ по некоторым данным противоопухолевый эффект химиотерапии отчасти реализуется за счет подавления функции яичников. На настоящий момент в адъювантном режиме при РМЖ изучено и предложено для клинического применения много различных режимов лекарственной терапии. Наиболее часто используемыми препаратами являются антрациклины и таксаны. При этом более интенсивные стандартные режимы несколько превосходят по эффективности менее агрессивные варианты даже у пожилых пациентов. Так, четыре цикла химиотерапии доксорубицин + цикло-фосфан считаются сходными по эффективности с шестью циклами циклофосфан + метотрексат + 5-фторурацил. Использование в адъювантном режиме таксанов улучшает отдаленные результаты независимо от всех прогностически значимых клинических факторов, таких как возраст, поражение лимфоузлов, размеры первичной опухоли, экспрессии стероидных рецепторов. Совместное последовательное использование таксанов и антрациклинов позволяет снизить вероятность рецидива заболевания на одну треть.
Анти-ИБВ2 препараты в адъювантной химиотерапии
Одним из основных прорывов последнего десятилетия в адъювантной химиотерапии рака молочной железы было выявление драматического улучшения результатов лечения одной из самых прогностически неблагоприятных групп опухолей молочной железы — HER2 позитивной. Наиболее изученным и широко используемым среди анти-HER2 препаратов является трастузумаб. Так, применение трастузумаба у больных РМЖ с гиперэкспрессией или амплификацией HER2 позволяет снизить риск рецидива заболевания практически вдвое, что приводит к увеличению 3-летней выживаемости на 3%. В большинстве исследований больные получали лечение трастузумабом в течение 1-го года, продолжение лечения до 2 лет не приводило к дальнейшему улучшению отдаленных результатов.
Полезно:
surgeryzone.net
Неоадъювантная химиотерапия при раке молочной железы - Портал о скорой помощи и медицине
Неоадъювантная химиотерапия
А. Стадии II и IIIA (N1). Если органосохраняющей операции мешает лишь размер первичной опухоли, для ее уменьшения можно провести химиотерапию. Неоадъювантная химиотерапия не повышает выживаемость по сравнению с адъювантной. Неизвестно, нужна ли адъювантная химиотерапии, если больная до операции получала и антрациклины, и таксаны.
- Перед лечением проводят пункционную биопсию первичной опухоли для определения гормональных рецепторов и экспрессии гена ERBB2. Подозрительные лимфоузлы также подвергают пункции или пункционной биопсии.
- Схема должна включать антрациклины (с таксанами или без них). В случае прогрессирования рака на фоне химиотерапии выполняется мастэктомия. Органосохраняющая операция возможна лишь при значительном уменьшении опухоли.
Б. Стадии IIIA (N2), ШВ и ШС
- После определения гормональных рецепторов и экспрессии гена ERBB2 необходимо исключить отдаленные метастазы. Обследование включает сцинтиграфию костей и УЗИ печени, для поиска метастазов в окологрудинные лимфоузлы проводят КТ грудной клетки.
- Показана химиотерапия с применением антрациклинов (с таксанами или без них) до или после операции. Если опухоль содержит гормональные рецепторы, в дальнейшем обязательна гормональная терапия.
- При эффективности химиотерапии выполняется мастэктомия или секторальная резекция, в обоих случаях с подмышечной лимфаденэктомией. Затем облучают грудную стенку (после мастэктомии) или молочную железу (в случае ее резекции) и надключичную область. При стадии IIIC показано облучение окологрудинных лимфоузлов. 4. Неясно, нужна ли адъювантная химиотерапии, если неоадъю-вантная химиотерапия включала и антрациклины, и таксаны.
IV стадия
А. Химиотерапия. Оптимальная схема химиотерапии диссеминиро ванного рака молочной железы неизвестна.
1. Опухоли без эстрогеновых рецепторов и усиления экспрессии гена ERBB2
а. Преимущество полихимиотерапии перед последовательным использованием тех же препаратов в рандомизированных испытаниях не доказано.
б. В качестве монотерапии предпочтительнее антрациклины (доксорубицин, обычный или липосомный, и эпирубицин), таксаны (паклитаксел, доцетаксел), капецитабин, винорельбин.
в. Помогают также гемцитабин, препараты платины, фторурацил (длительная в/в инфузия), винбластин, митомицин.
2. Опухоли с усилением экспрессии гена ERBB2
а. Эффективен трастузумаб в качестве монотерапии или в сочетании с каким-либо цитостатиком.
б. В одном рандомизированном испытании сочетание трастузумаба с химиотерапией повышало выживаемость, однако на фоне трастузумаба и доксорубицина у 27% больных развилась сердечная недостаточность.
в. Трастузумаб можно сочетать и с другими цитостатиками (п. IX.А. 1). Исследования in vitro показали его синергизм с доцетакселом, винорельбином и препаратами платины.
Б. Опухоли с гормональными рецепторами. В большинстве случаев рекомендуется гормональная терапия. Химиотерапия показана при непосредственной угрозе жизни (например, при раковом лимфангиите легких или быстро растущих метастазах в печени).
1. Женщины в постменопаузе. Гормональные препараты назначают в следующем порядке.
а. Ингибиторы ароматазы:
1) анастрозол, 1 мг/сут внутрь;
2) экземестан, 25 мг/сут внутрь;
3) летрозол, 2,5 мг/сут внутрь.
б. Тамоксифен, 20 мг/сут внутрь; или торемифен, 60 мг/сут внутрь.
в. Фульвестрант, 250 мг в/м 1 раз в месяц.
г. Мегестрол, 40 мг внутрь 4 раза в сутки.
д. Флуоксиместерон, 10 мг внутрь 2—3 раза в сутки.
е. Диэтилстильбэстрол, 5 мг внутрь 3 раза в сутки.
2. Женщины детородного возраста
а. Тамоксифен.
б. Аналоги гонадолиберина, овариэктомия или лучевая кастрация.
в. Мегестрол.
г. Флуоксиместерон.
д. Диэтилстильбэстрол. В. Дифосфонаты показаны при метастазах в кости. Памидронат натрия, 90 мг в/в 1 раз в месяц, и золедроновая кислота, 4 мг в/в
1 раз в месяц, уменьшают боль в костях и риск патологических переломов. Вероятно, золедроновая кислота в большей степени снижает риск переломов, гиперкальциемии, сдавления спинного мозга, а также потребность в паллиативной лучевой терапии. Г. Местное лечение. Отдаленные метастазы обычно требуют системного лечения, но иногда прибегают и к лучевой терапии.
- Метастазы в кости часто не требуют специального лечения. При боли и угрозе перелома обычно помогает лучевая терапия. При метастазах в позвонки в поле облучения включают по одному позвонку выше и ниже пораженного. Кроме того, всем больным вводят дифосфонаты (п. IX.B). Сдавление спинного мозга требует немедленной операции: в недавнем испытании хирургическая декомпрессия увеличила долю больных, которые смогли ходить, по сравнению с получавшими лишь лучевую терапию, хотя выживаемость в обеих группах была одинаковой.
- Метастазы в шейные позвонки и шейку бедренной кости независимо от симптомов обычно требуют лучевой терапии из-за угрозы перелома. При поражении шейки бедренной кости может понадобиться и профилактическая фиксация.
- Метастазы в головной мозг и глазницу. Головная боль, тошнота и рвота при метастазирующем раке молочной железы требуют немедленного исключения метастазов в головной мозг и мозговые оболочки. Для этого нужна МРТ, с контрастированием или без него. При одиночном метастазе возможна операция или стереотаксическое облучение, при множественных метастазах показано облучение всего головного мозга.
- Рецидив в грудной стенке. Обычно начинают с гормональной терапии или химиотерапии; в некоторых случаях, главным образом при изолированном рецидиве, применяют лучевую терапию.
www.03-ektb.ru
Виды химиотерапии при раке груди, порядок проведения, побочное действие
Под понятием «химиотерапия» в медицине подразумевается применение любых лекарственных препаратов. Но по разным причинам этот термин чаще всего используется в онкологии, часто сокращают его до простого слова «химия», подразумевая, что химиотерапия влияет на весь организм, распространяясь через кровоток. Химиотерапия при раке молочной железы, как при других злокачественных заболеваниях, способна остановить или замедлить онкопроцесс.
Польза химиотерапии при лечении любой злокачественной опухоли заключается в том, что химиотерапевтический препарат может внедрятся в генетический аппарат раковой клетки в момент её деления.
Проникнув в геном этой клетки, он вызывает нарушения несовместимые с её жизнью. В результате этого запускаются механизмы самоликвидации (суицида клетки). Но борясь со злокачественными клетками, химиотерапия не способна отличить их от делящихся нормальных клеток организма. Большинство нормальных клеток взрослого человека не делятся и химиотерапия на них не действует. Тем не менее, клетки костного мозга, волосяных фолликул, слизистой желудочно-кишечного тракта постоянно размножатся и разрушаются при проведении химиотерапии. Гибель как нормальных клеток, так и злокачественных во время химиотерапии приводит к её побочным эффектам.
В этой статье вы узнаете: какие виды химиотерапии при раке молочной железы применяются, о противоопухолевых препаратах, используемые при этом заболевании, об их побочных эффектах.
Онкологи химиотерапию рака молочной железы подразделяют в зависимости от целей, которые она преследует на:
- химиотерапию при неметастатическом (2–3 стадии) раке;
- и при метастатическом раке молочной железы (4 стадия).
 Схемы химиотерпии при раке молочной железы включают уколы и таблетки
Схемы химиотерпии при раке молочной железы включают уколы и таблетки Применение химиотерапии при 2–3 стадиях рака молочной железы рассматривается, как вспомогательный (адъювантный) вид лечения, дополняющий основной хирургический. При этих стадиях используют химиотерапевтические препараты с целью уничтожить раковые клетки, оставшиеся в послеоперационной ране или те, которые циркулируют с током крови по всему организму. Чаще используется комбинация этих препаратов. Они вводятся в организм через вену или через рот в виде таблеток. Клинические испытания показали, что адъювантная химиотерапия увеличивает сроки выживания и уменьшает риск рецидива среди больных, получивших её, а не только местное лечение (хирургическое или радиационное).
Схемы химиотерапии при раке молочной железы
Онкологами используется значительный арсенал противоопухолевых препаратов и их комбинаций (схем). Например, такая как CMF, включающая в себя циклофосфамид, метотрексат и фторурацил, считается первой стандартной схемой, применяемой у женщин с раком молочной железы 2–3 стадии и широко используется по сегодняшний день. CMF обычно состоит из 6 циклов и длится приблизительно 4–6 месяцев.
Исследования доказали, что включение препарата доксорубицина (адриамицин) в схемы адъювантной химиотерапии увеличивает выживаемость среди женщин с 2–3 стадии в сравнении с теми, которые не получали доксорубицин. Наиболее часто применяются при лечении этих стадий схемы CAF (циклофосфамид, доксорубицин, фторурацил) и AC (доксорубицин и циклофосфамид). Тем не менее, эти схемы, как правило, связаны с более частыми побочными проявлениями, чем CMF.
Таксаны
Таксаны — вид противоопухолевых препаратов, которые, как показали последние исследования, улучшают выживаемость женщин с раком груди 2–3 стадии. В этой группе таксотер (доцетаксел) считается более эффективным, чем паклитаксел при лечении женщин с распространённым раком молочной железы (3 стадия). Таксаны, как правило, применяются в комбинации с AC схемой. Схема, содержащая таксотер ТАС (доцетаксел, доксорубицин, циклофосфамид), показала, что общая выживаемость у женщин, получавших эту комбинацию, составляет 87%. В свою очередь, у тех пациенток с 3 стадией рака груди, которые лечились FAC (5-фторурацил, доксорубицин, циклофосфамид) она была 81%.
У больных, получающие таксотер и циклофосфамид, наблюдается более высокая безрецидивная выживаемость, чем у тех, которые получают стандартные схемы химиотерапии (CMF, FAC, AC, CAF). Кроме того, комбинация таксотера и циклофосфамида менее токсична для сердца.
Уплотнение дозы или так называемая «dose-dense» химиотерапия
Эффективность лечения зависит не только от назначенного препарата, но и от того, как проводится химиотерапия при раке молочной железы, какие интервалы между её введениями. Схемы ТАС, CMF и другие, как правило, проводятся каждые 3 недели. «Dose-dense» химиотерапия проводят каждые 2 недели. Этим достигается увеличение суммарной дозы противоопухолевых препаратов. Исследования доказали, что пациентки с поражением лимфатических узлов, получившие этот вид химиотерапии, живут дольше без рецидива, чем женщины, у которых использовались обычные схемы.
Неоадъювантная химиотерапия
Неоадъювантная терапия в отличие от адъвантной проводится перед операцией. Её цель — быстрое уменьшение размера опухоли в молочной железе для увеличения вероятности выполнения хирургического вмешательства. Результаты проведенных клинических испытаний ясно показывают, что неоадъювантная химиотерапия увеличивает вероятность выполнения органосохраняющих операций.
Рекомендуем к прочтению статью о раке молочной железы 3 стадии. В этой статье вы сможете подробнее узнать о клинических проявлениях на этой стадии рака, какие методы лечения применяются, прогноз на этой стадии заболевания.Химиотерапия при 4 стадии
В настоящее время существует несколько стандартных схем химиотерапии 4 стадии рака груди, которые примерно у 25% пациенток могу полностью затормозить на длительный срок развитие опухоли. К сожалению, у каждой четвертой пациентки они окажутся совершенно неэффективными.
Тип химиотерапии при 4 стадии зависит от цели лечения. Если цель — уменьшить симптомы и улучшить качество жизни, более целесообразно выбрать химиотерапию с минимальными побочными эффектами.
С другой стороны, если цель — попытаться вылечить рак, потребуются более агрессивные схемы или участие в клинических исследованиях, предоставляющие новые стратегии лечения, которые могут быть более подходящими в каждом конкретном случае.
Важно изначально женщине определиться с целью лечения. Причина здесь в том, что начальное лечение рака молочной железы 4 стадии, как правило, более эффективно, чем лечение рецидива, который неизбежно случится. Неудача лечения рецидива в том, что раковые клетки становятся невосприимчивыми к терапии. Пациентки, заинтересованные в агрессивном лечении, могут принять участие в клинических исследованиях, где в качестве первой терапии используются агрессивные схемы.
Побочные эффекты химиотерапии
Тяжесть побочного действия химиотерапии при раке молочной железы зависит от конкретного препарата, способа его введения и особенностей организма. Врачи располагают достаточным арсеналом эффективных средств борьбы с побочными проявлениями химиотерапии. Их можно разделить на две группы.
Побочные эффекты химиотерапии, встречаемые часто, но серьёзную опасность для организма пациента они не представляют:
- тошнота и рвота;
- усталость;
- выпадение волос;
- диарея или запор;
- потеря веса;
- язвочки и инфекционное воспаление ротовой полости;
- реакция со стороны кожи или ногтей;
- депрессия.
Побочные эффекты химиотерапии редко встречаемые, но довольно опасные:
- инфекция, связанная с низким уровнем лейкоцитов;
- кровотечение;
- проблемы с почками или мочевым пузырём;
- проблемы с сердцем;
- проблемы с нервами.
grudinfo.ru
Адъювантная химиотерапия при раке молочной железы - Портал о скорой помощи и медицине
Адъювантная химиотерапия. Без адъювантной системной терапии десятилетняя выживаемость в отсутствие метастазов в лимфоузлы составляет около 65%, при метастазах в 1—3 лимфоузла — 40%, при 4 и более лимфоузлах — 15%. У половины больных из последней группы отдаленные метастазы появлялись в течение 18 мес.
Адъювантная терапия заметно повышает выживаемость
- Показания. Химиотерапия показана почти всем больным с метастазами в лимфоузлы, в отсутствие метастазов она рекомендуется при опухолях без эстрогеновых и прогестероновых рецепторов, с умеренной и низкой дифференцировкой и усиленной экспрессией ERBB2. Эффективность зависит от возраста и наличия гормональных рецепторов.
- Эффективность. Как показал метаанализ, опубликованный в 1998 г. Объединенной группой исследователей ранних стадий рака молочной железы (Early Breast Cancer Trialists Collaborative Group, 1998), эффективность адъювантной химиотерапии снижается с возрастом.
а. У женщин моложе 40 лет адъювантная химиотерапия снижает риск рецидива на 39%, у женщин 50—59 лет — лишь на 22%.
б. При опухолях без эстрогеновых и прогестероновых рецепторов эффективность химиотерапии вышес'Так, у женщин 50 лет и старше риск рецидива снижается на 30%, если опухоль не содержит эстрогеновых рецепторов, и лишь на 18% при их наличии.
в. Если риск рецидива составляет 100%, тридцатипроцентное снижение уменьшит его до 70%, но при исходном риске, равном 10%, абсолютное снижение составит лишь 3%. Таким образом, к назначению химиотерапии на ранних стадиях следует подходить взвешенно.
3. Схемы химиотерапии (табл. 10.4). Согласно рекомендациям. Национальной онкологической сети США (National Compre-hensive Cancer Network — NCCN) от 2003 г., выбор схемы зависит от состояния лимфоузлов.
а. Метастазов в лимфоузлы нет CMF (циклофосфамид, метотрексат и фторурацил). FAC/CAF (циклофосфамид, доксорубицин и фторурацил). АС (доксорубицин и циклофосфамид).
б. Метастазы в лимфоузлы CMF. FAC/CAF.
CEF (циклофосфамид, эпирубицин и фторурацил). АС. АС, затем паклитаксел. ЕС (эпирубицин и циклофосфамид). ТАС (доцетаксел, доксорубицин и циклофосфамид). Доксорубицин каждые 3 нед, затем CMF.
в. Вероятно, при опухолях с усилением экспрессии ERBB2 более эффективны схемы с доксорубицином. Кроме того, схемы с антрациклинами предпочтительнее при метастазах в лимфоузлы.
Химиотерапия рака молочной железы
| Схема | Доза, мг/м2 | |
| (интервал) | ||
| Циклофосфамид | Фторурацил Другие препараты | |
| CMF (3 нед) | 600 (1-е сутки) | 600 (1 -е сутки) Метотрексат, 40 |
| (1-е сутки) | ||
| Исходная CMF | 100 (внутрь, с 1-х | 600 (1-е и 8-е сутки) Метотрексат, 40 |
| (4 нед) | по 14-е сутки) | (1-е и 8-е сутки) |
| АС (3 нед) | 600 (1-е сутки) | Доксорубицин, 60 |
| (1 -е сутки) | ||
| FAC (4 нед) | 400-500 (1-е сут- | 400—500 (1 -е и 8-е Доксорубицин, |
| ки) | сутки) 40—50 (1-е сутки) | |
| CAF (4 нед) | 100 (внутрь, с 1-х | 600 (1-е и 8-е сутки) Доксорубицин, 30 |
| по 14-е сутки) | (1 -е и 8-е сутки) | |
| ЕС (3 нед) | 600 (1-е сутки) | Эпирубицин, 100 |
| (1 -е сутки) | ||
| CEF120 (4 нед) | 75 (внутрь, с 1-х | 500 (1-е и 8-е сутки) Эпирубицин, 60 |
| по 14-е сутки) | (1-е и 8-е сутки) + | |
| антимикробная | ||
| профилактика | ||
| FEC 100 (3 нед) | 500 (1-е сутки) | 500 (1-е сутки) Эпирубицин, 50 |
| (1-е и 8-е сутки) | ||
| или 100 (1-е сутки) | ||
| ТАС (3 нед) | 500 (1-е сутки) | Доксорубицин, 50 |
| (1-е сутки); доцетак- | ||
| сел, 75 (1-е сутки) | ||
| Учащенная схема6 | ||
| АС (2 нед) | 600 (1-е сутки) | Доксорубицин, 60 |
| (1-е сутки) | ||
| Затем пакли- | Паклитаксел, 175 | |
| таксел (2 нед) | (1-е сутки) |
а Препараты вводят в/в (кроме случаев, когда указан прием внутрь).
6 Последовательно проводится по 4 курса АС и паклитаксела на фоне Г-КСФ (филграстим, 300 или 480 мкг п/к со 2-х по 10-е сутки каждого курса, или пэгфилграстим, 6 мг п/к на 2-е сутки).
www.03-ektb.ru