Синдром поликистозных яичников
Синдром поликистозных яичников
Комментарии
И.Б. Манухин, М.А. Геворкян Кафедра акушерства и гинекологии лечебного факультета Московского государственного медико-стоматологического университета
Представлены современные данные об этиопатогенезе, клинике, диагностике и лечении синдрома поликистозных яичников.
Сокращения:
СПКЯ – синдром поликистозных яичников; ИПФР – инсулиноподобный фактор роста; ГИ – гиперинсулинемия; ИР – инсулинорезистентность; ПССГ – половые стероиды, связывающие глобулины; ЛПНП – липопротеины низкой плотности; ЛПОНП – липопротеины очень низкой плотности; ЛПВП – липопротеины высокой плотности; ФКМ – фиброзно-кистозная мастопатия; АГС – адреногенитальный синдром; ДМК – дисфункциональные маточные кровотечения; ИМТ – индекс массы тела; МФЯ – мультифолликулярные яичники; КОК – комбинированные оральные контрацептивы;
СГЯ – синдром гиперстимуляции яичников.
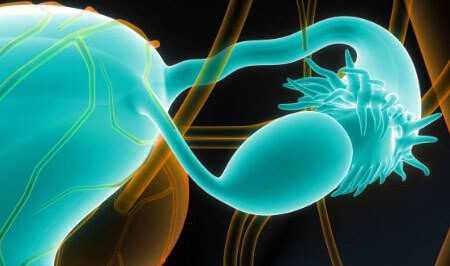
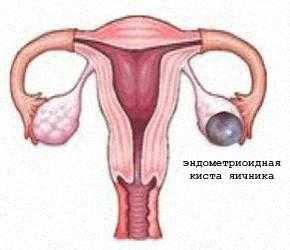
Синдром поликистозных яичников (СПКЯ) – патология структуры и функции яичников, основными критериями которых являются хроническая ановуляция и гиперандрогения. Частота СПКЯ составляет около 30% среди пациенток гинекологов-эндокринологов, а в структуре эндокринного бесплодия достигает 75%.
Структурные изменения яичников при этой патологии хорошо изучены и характеризуются:
- Двухсторонним увеличением размеров яичников в 2–6 раз.
- Гиперплазией стромы.
- Гиперплазией клеток тека с участками лютеинизации.
- Наличием множества кистозно-атрезирующихся фолликулов диаметром 5–8 мм, расположенными под капсулой в виде «ожерелья».
- Утолщением капсулы яичников.
Патогенез СПКЯ
Суммируя основные современные представления об этой патологии можно выделить следующие основные положения патогенеза. Но сначала напомним основы стероидогенеза в яичниках. Синтез андрогенов происходит в клетках тека фолликулов определенной стадии зрелости диаметром 5–8 мм и в строме. Регулируют синтез андрогенов ЛГ инсулиноподобный фактор роста-I (ИПФР-I) и энзим (цитохром Р450с17). В превращении андрогенов (тестостерона и андростендиона) в эстрогены (эстрадиол и эстрон), так называемый процесс ароматизации андрогенов, участвует цитохром Р450с17. Синтез энзима регулируется ФСГ.
В ПКЯ гиперандрогения является следствием:
- Повышения уровня ЛГ в результате нарушения цирхорального ритма выделения ГнРГ и гонадотропинов, формирующегося в пубертатном возрасте, в период становления гормональной функции репродуктивной системы. Возможной причиной являются генетические факторы. Гиперстимуляция ЛГ нарушает фолликулогенез в яичниках, формируется кистозная атрезия фолликулов с гиперплазией тека-клеток, стромы и увеличением синтеза андрогенов. В результате дефицита ФСГ, необходимого для синтеза энзимов, ароматизирующих андрогены в эстрогены, происходит накопление андрогенов и дефицит эстрадиола.
- Важным механизмом гиперандрогении является характерная для СПКЯ инсулинорезистентность (ИР) – уменьшение утилизации глюкозы в организме. В результате возникает компенсаторная гиперинсулинемия. Поскольку имеется дефект рецепторов инсулина, его действие реализуется через рецепторы ИПФР-I. Инсулин и ИПФР-I способствуют усилению ЛГ-зависимого синтеза андрогенов в тека-клетках и строме, а также стимулируя выброс ЛГ.
- Увеличение концентрации свободного биологически активного Т за счет уменьшения образования ПССГ. Синтез ПССГ уменьшается вследствие снижения уровня эстрадиола и гиперинсулинемии.
- – Определенная роль принадлежит жировой ткани. При ожирении нарушается толерантность к глюкозе по диабетогенному типу. Развивается инсулинорезистентность и компенсаторная гиперинсулинемия. Вследствие этих метаболических нарушений усиливается синтез андрогенов в адипоцитах (жировых клетках) и соответственно превращение (ароматизация) тестостерона в эстрадиол и андростендиона в эстрон. Этот процесс имеет автономный характер, не зависит от гонадотропной стимуляции. Таким образом, жировая ткань является источником андрогенов и эстрогенов (в основном эстрона) внегонадного происхождения.
Нарушения синтеза половых гормонов при СПКЯ и их клинические проявления представлены на схеме 1.
Основными клиническими проявлениями СПКЯ являются хроническая ановуляция и яичниковая гиперандрогения. Различия в патогенезе, преобладание того или другого механизма, позволяют выделить два основных механизма формирования: СПКЯ с ожирением и СПКЯ без ожирения, представленных на схеме 2.
При ожирении имеет место ИР и, как следствие, ГИ, что повышает ЛГ-зависимый синтез андрогенов в тека-клетках (как было указано выше). У женщин с нормальной массой тела повышенный уровень гормона роста стимулирует синтез ИПФР в клетках гранулезы, что, в свою очередь, паракринным путем осуществляет эффект ИПФР на тека-клетки. В сочетании с увеличением уровня ЛГ это приводит к гиперпродукции андрогенов по тому же механизму, что и при ожирении. Как видно, различия только в пусковом механизме, результатом является увеличение синтеза андрогенов в яичниках.
Итак, СПКЯ – многофакторная патология, возможно, генетически детерминированная, в патогенезе которой участвуют центральные механизмы гонадотропной функции гипофиза (с пубертатного периода), местные яичниковые факторы, экстраовариальные эндокринные и метаболические нарушения, определяющие клиническую симптоматику и морфологические изменения яичников.
Клиническая картина
Для СПКЯ характерны следующие симптомы:
1. Нарушение менструального цикла по типу олигоаменореи. Поскольку нарушение гормональной функции яичников начинается с пубертатного периода, с момента физиологической активации функции яичников, нарушения цикла начинаются с менархе и не имеют тенденции к нормализации. Следует отметить, что возраст менархе соответствует таковому в популяции – 12–13 лет, в отличие от надпочечниковой гиперандрогении при адреногенитальном синдроме (АГС), когда менархе запаздывает. Примерно у 10–15% пациенток нарушения менструального цикла имеют характер ДМК на фоне гиперпластических процессов эндометрия. Поэтому женщины с СПКЯ входят в группу риска развития аденокарциномы эндометрия, ФКМ и рака молочных желез. 2. Ановуляторное бесплодие. Важно отметить, что бесплодие имеет первичный характер в отличие от надпочечниковой гиперандрогении при АГС, при которой возможна беременность и характерно невынашивание. 3. Гирсутизм, различной степени выраженности, развивается постепенно с периода менархе. Отметим, что при АГС гирсутизм развивается до менархе, с момента активации гормональной функции надпочечников в период адренархе. 4. Превышение массы тела отмечается примерно у 70% женщин при ИМТ 26—30, что соответствует II–III степени ожирения. Ожирение чаще имеет универсальный характер, о чем свидетельствует отношение объема талии к объему бедер (ОТ/ОБ) менее 0,85, характеризующего женский тип ожирения. Соотношение ОТ/ОБ более 0,85 характеризует кушингоидный (мужской) тип ожирения и встречается реже. 5. Молочные железы развиты правильно, у каждой третьей женщины имеет место фиброзно-кистозная мастопатия (ФКМ), развивающаяся на фоне хронической ановуляции и гиперэстрогении.
В последние годы было установлено, что при СПКЯ часто имеет место инсулинорезистетность (ИР) и компенсаторная гиперинсулинемия (ГИ) – нарушения углеводного и жирового обмена по диабетоидному типу. Отмечается также дислипидемия с преобладанием липопротеинов атерогенного комплекса (холестерина, триглицеридов, ЛПНП и ЛПОНП). Это, в свою очередь, повышает риск развития сердечно-сосудистых заболеваний во 2–3-м десятилетиях жизни, которым эти заболевания не свойственны.
Диагностика
Характерный анамнез, внешний вид и клиническая симптоматика облегчают диагностику СПКЯ. В современной клинике диагноз СПКЯ можно поставить без гормональных исследований, хотя они также имеют характерные особенности.
Диагноз ПКЯ может быть установлен при трансвагинальном УЗИ, на основании четких критериев эхоскопической картины: объем яичников более 9 см3, гиперплазированная строма составляет 25% объема, более 10 атретичных фолликулов диаметром до 10 мм, расположенных по периферии под утолщенной капсулой. Объем яичников определяется по формуле: см3 = ДЅ Т Ѕ Ш Ѕ 0,5, где Д, Т, Ш – длина, толщина и ширина яичника, 0,5 – коэффициент. Увеличение объема яичников за счет гиперплазированной стромы помогает дифференцировать ПКЯ от нормальных (на 5–7-й день цикла) или мультифолликулярных (МФЯ). Последние характерны для раннего пубертата, гипогонадотропной аменореи, длительного приема комбинированных оральных контрацептивов. Характерной УЗ-картиной МФЯ является небольшое число фолликулов диаметром от 4 до 10 мм, расположенных по всей строме, и, главное, нормальный объем яичников. М.В. Медведев, Б.И. Зыкин (1997) дают следующее определение МФЯ: «преходящие изменения в структуре яичников в виде множества эхонегативных включений диаметром 5–10 мм, имеющих обратное развитие при отсутствии клинической картины и эхоструктуры поликистозных яичнииков».
Внедрение трансвагинальной эхографии с высокой разрешающей способностью аппаратов значительно улучшило диагностику ПКЯ, приближая ее к морфологической. Последним достижением стало внедрение Dewailly и соавт. (1994) компьютеризированной УЗИ техники для детального исследования стромы и фолликулярного аппарата яичников.
Итак, УЗИ является неинвазивным, высокоинформативным методом, который можно считать золотым стандартом в диагностике СПКЯ.
Гормональная характеристика СПКЯ. Критериями диагностики СПКЯ являются: повышение уровня ЛГ, соотношения ЛГ/ФСГ более 2,5, увеличение уровня общего и свободного Т при нормальном содержании ДЭА-С и 17-ОНП. После пробы с дексаметазоном содержание андрогенов незначительно снижается, примерно на 25% (за счет надпочечниковой фракции). Проба с АКТГ отрицательная, что исключает надпочечниковую гиперандрогению, характерную для АГС. Отмечено также повышение уровня инсулина и снижение ПССГ в крови.
Метаболические нарушения при СПКЯ характеризуются: повышением уровня триглицеридов, ЛПНП, ЛПОНП и снижением ЛПВП. В клинической практике простым и доступным методом определения нарушения толерантности глюкозы к инсулину является сахарная кривая. Определение сахара крови натощак и затем в течение 2-х часов после приема 75 г глюкозы. На основании результатов строится гликемическая кривая. Если через 2 часа уровень сахара крови не приходит к исходным цифрам, это свидетельствует о нарушенной толерантности к глюкозе, т.е. ИР, и требует соответствующего лечения. Биопсия эндометрия показана женщинам с ациклическими кровотечениями в связи с большой частотой гиперпластических процессов эндометрия.
Таким образом, диагноз СПКЯ ставится на основании следующих данных:
- своевременный возраст менархе,
- нарушение менструального цикла с периода менархе в подавляющем большинстве по типу олигоменореи,
- гирсутизм и у более чем половины женщин — ожирение с периода менархе,
- первичное бесплодие,
- хроническая ановуляция,
- увеличение объема яичников за счет стромы и кистозных фолликулов по данным трансвагинальной эхографии,
- повышение уровня тестостерона,
- увеличение ЛГ и отношения ЛГ/ФСГ.
Дифференциальная диагностика СПКЯ проводится с гиперандрогенией, обусловленной АГС, а также с вирилизирующими опухолями яичников и/или надпочечников.
Лечение
Как правило, пациентки с СПКЯ обращаются к врачу с жалобами на бесплодие. Поэтому целью лечения является восстановление овуляторных циклов.
При СПКЯ с ожирением и с нормальной массой тела последовательность терапевтических мер различается.
При наличии ожирения первый этап терапии – нормализация массы тела. Снижение массы тела на фоне редукционной диеты приводит к нормализации углеводного и жирового обмена. Диета предусматривает снижение общей калорийности пищи до 2000 ккал в день, из них 52% приходится на углеводы, 16% – на белки и 32% – на жиры, причем насыщенные жиры должны составлять не более 1/3 общего количества жира. Важным компонентом диеты является ограничение острой и соленой пищи, жидкости. Очень хороший эффект отмечается при использовании разгрузочных дней, голодание не рекомендуется в связи с расходом белка в процессе глюконеогенеза. Повышение физической активности является важным компонентом не только для нормализации массы тела, но повышения чувствительности мышечной ткани к инсулину. Самое главное убедить пациентку в необходимости нормализации массы тела как первого этапа в лечении СПКЯ.
Вторым этапом в лечении является медикаментозная терапия метаболических нарушений (ИР и ГИ) в случае отсутствия эффекта от редукционной диеты и физических нагрузок. Препаратом, повышающим чувствительность периферических тканей к инсулину, является метформин – из класса бигуанидов. Метформин приводит к снижению периферической ИР, улучшая утилизацию глюкозы в печени, мышцах и жировой ткани, нормализует липидный профиль крови, снижая уровень триглицеридов и ЛПНП. Препарат назначается по 1000–1500 мг/сутки в течение 3–6 мес под контролем глюкозотолерантного теста.
При СПКЯ на фоне нормальной массы тела начинают с лечения бесплодия, т.е. стимуляции овуляции. Стимуляция овуляции проводится после нормализации массы тела, исключения трубного и мужского факторов бесплодия. В настоящее время большинство клиницистов на первом этапе индукции овуляции применяют кломифен. Надо отметить, что длительно применявшийся метод стимуляции овуляции применением эстроген-гестагенных препаратов, основанный на ребаунд-эффекте после их отмены, не потерял своей популярности. При отсутствии эффекта от терапии эстроген-гестагенами, кломифеном, рекомендуется назначение гонадотропинов или хирургическая стимуляция овуляции.
Стимуляция овуляции кломифеном начинается с 5-го по 9-й день менструального цикла по 50 мг в день. При таком режиме повышение уровня гонадотропинов, индуцированное кломифеном, происходит в то время, когда уже завершился выбор доминантного фолликула. Более раннее назначение кломифена может стимулировать развитие множества фолликулов и увеличивает риск многоплодной беременности. При отсутствии овуляции по данным базальной температуры дозу кломифена можно увеличивать в каждом последующем цикле на 50 мг, достигая 200 мг в день. Однако многие клиницисты считают, что если нет эффекта при назначении 100–150 мг, то дальнейшее увеличение дозы кломифена не целесообразно. При отсутствии овуляции при максимальной дозе в течение 3-х мес пациентку можно считать резистентной к кломифену. Критерием эффективности стимуляции овуляции служит восстановление регулярных менструальных циклов с гипертермической базальной температурой в течение 12–14 дней второй фазы цикла, уровень прогестерона в середине второй фазы цикла 15 нг/мл и более, преовуляторный пик ЛГ; а также УЗИ признаки овуляции на 13–15 день цикла – наличие доминантного фолликула не менее 18 мм, толщины эндометрия не менее 8–10 мм. При наличии этих показателей рекомендуется введение овуляторной дозы 7500–10 000 человеческого хорионического гонадотропина – чХГ (профази, прегнил), после чего овуляция отмечается через 36–48 часов. Важно помнить, что раннее назначение чХГ может привести к преждевременной лютеинизации незрелого фолликула, а позднее назначение чХГ – к лютеолитическому эффекту. При лечении кломифеном следует помнить, что он обладает антиэстрогенными свойствами, уменьшает количество цервикальной слизи («сухая шейка»), что препятствует пенетрации сперматозоидов и тормозит пролиферацию эндометрия и приводит к нарушению имплантации в случае оплодотворения яйцеклетки. С целью устранения этих нежелательных эффектов кломифена рекомендуется после окончания приема кломифена принимать натуральные эстрогены в дозе 1–2 мг или синтетические эстрогены (микрофоллин) в дозе 0,05 мг с 10 по 14 день цикла для повышения проницаемости шеечной слизи и пролиферации эндометрия.
При недостаточности лютеиновой фазы (НЛФ) рекомендуется назначить гестагены во вторую фазу цикла с 16 по 25 день. При этом предпочтительнее препараты прогестерона (дюфастон), так как производные норстероидов могут оказывать лютеолитический эффект.
Частота индукции овуляции при лечении кломифеном составляет примерно 60–65%, наступление беременности в 32–35%, частота многоплодной беременности, в основном двойней, составляет 5–6%, риск внематочной беременности и самопроизвольных выкидышей не выше, чем в популяции. При отсутствии беременности на фоне овуляторных циклов требуется исключение перитонеальных факторов бесплодия при лапароскопии.
При резистентности к кломифену назначают гонадотропные препараты – прямые стимуляторы овуляции. Используется чМГ, приготовленный из мочи женщин постменопаузального возраста. Препараты чМГ содержат ЛГ и ФСГ по 75 ЕД (пергонал, хумигон и др.). В последние годы разработан высокоочищенный препарат ФСГ (метродин) для стимуляции овуляции у женщин с высоким ЛГ. Перспективным является клиническое применение рекомбинантного ФСГ, полученного путем генной инженерии. Этот высокоочищенный препарат вводится подкожно, что удобно для использования самой пациенткой. Однако их высокая стоимость не дает возможности широкого применения в практике. При назначении гонадотропинов пациентка должна быть информирована о риске многоплодной беременности, возможном развитии синдрома гиперстимуляции (СГЯ), а также о высокой стоимости лечения. Лечение должно проводиться только после исключения патологии матки и труб, а также мужского фактора бесплодия. В процессе лечения обязательным является трансвагинальный УЗ мониторинг фолликулогенеза и состояния эндометрия. Овуляция инициируется путем однократного введения чХГ в дозе 7500–10 000 ЕД, когда имеется хотя бы один фолликул диаметром 17 мм. При выявлении более 2 фолликулов диаметром более 16 мм или 4 фолликулов диаметром более 14 мм введение чХГ нежелательно из-за риска наступления многоплодной беременности.
При стимуляции овуляции гонадотропинами частота наступления беременности повышается до 60%, риск многоплодной беременности составляет 10–25%, внематочной от 2,5 до 6%, самопроизвольные выкидыши в циклах, закончившихся беременностью, достигают 12–30% и СГЯ наблюдается в 5–6% случаев.
Клиновидная резекция яичников, хирургический метод стимуляции овуляции, предложенный еще в 30-х годах был наиболее распространенным до 60-х годов, до кломифеновой эры. Из-за спаечного процесса, резко снижающего частоту наступления беременности, большинство клиницистов отказались от резекции яичников при лапаротомии. В последние годы интерес к хирургическому лечению возрос в связи с внедрением операционной лапароскопии, преимуществами которой являются минимальное инвазивное вмешательство и снижение риска спайкообразования. Кроме того, преимуществами лапароскопической резекции являются: отсутствие риска гиперстимуляции, наступления многоплодной беременности и возможность ликвидации часто сопутствующего перитонеального фактора бесплодия. Патофизиологические механизмы клиновидной резекции в стимуляции овуляции основаны на уменьшении объема стероидпродуцирующей стромы яичников. В результате чего нормализуется чувствительность гипофиза к ГнРГ и восстанавливаются гипоталамо-гипофизарно-яичниковые связи.
Помимо клиновидной резекции, при лапароскопии можно производить каутеризацию яичников при помощи различных энергий (термо-, электро-, лазерной), которая основана на разрушении стромы точечным электродом. Производится от 15 до 25 пунктур в каждом яичнике, операция менее травматичная и длительная по сравнению с клиновидной резекцией. При достаточной технической оснащенности и опыте хирурга лапароскопическая резекция яичников занимает 10–15 мин, кровопотеря минимальная. Гемостаз предпочтительнее проводить коагуляцией, так как наложение швов увеличивает риск спайкообразования. Обязательным является тщательное промывание брюшной полости, что снижает риск развития постоперационных спаек. Преимуществами лапароскопии также является косметический эффект и длительность пребывания в стационаре не более 2 суток. При анализе лапароскопических осложнений было показано, что подавляющее большинство их наблюдается на этапах вхождения в брюшную полость. В послеоперационном периоде через 3–5 дней наблюдается менструальноподобная реакция, а через 2 недели овуляция, которая тестируется по базальной температуре. Отсутствие овуляции в течение 2–3 циклов требует дополнительного назначения кломифена. Как правило, беременность наступает в течение 6–12 мес, в дальнейшем частота наступления беременности уменьшается. Отсутствие беременности при наличии овуляторных менструальных циклов диктует необходимость исключения трубного фактора бесплодия.
Частота индукции овуляции после хирургической лапароскопии составляет 84–89%, наступление беременности в среднем отмечается в 72%.
Несмотря на достаточно высокий эффект в стимуляции овуляции и наступлении беременности, большинство клиницистов отмечают рецидив ПКЯ и клинической симптоматики примерно через 5 лет. Поэтому после беременности и родов необходима профилактика рецидива СПКЯ, что важно, учитывая риск развития гиперпластических процессов эндометрия. С этой целью наиболее целесообразно назначение комбинированных оральных контрацептивов (КОК), предпочтительнее монофазных (марвелон, фемоден, диане, мерсилон и др.). При плохой переносимости КОК, что бывает при избыточной массе тела, можно рекомендовать гестагены во вторую фазу цикла: дюфастон 20 мг с 16 по 25 день цикла, медроксипрогестеронацетат (МПА) по 10—20 мг с 16 по 25 день цикла или 17-ОПК 12,5% в/м на 16 и 21 день цикла по 125–250 мг.
У женщин, не планирующих беременность после первого этапа стимуляции овуляции кломифеном, направленного на выявление резервных возможностей репродуктивной системы, также рекомендуется назначение КОК или гестагенов для регуляции цикла, уменьшения гирсутизма и профилактики гиперпластических процессов.
Лечение гиперпластических процессов эндометрия у женщин с СПКЯ. При выявлении гиперплазии эндометрия, подтвержденной гистологическим исследованием, первым этапом проводится терапия эстроген-гестагенными и гестагенными препаратами, при ожирении предпочтительнее гестагены. Гормонотерапия гиперпластических процессов эндометрия предусматривает центральный и местный механизм действия препарата, заключающийся в подавлении гонадотропной функции гипофиза, приводящее к торможению фолликулогенеза в яичниках и, как следствие этого, снижение эндогенного синтеза стероидов; местное действие гормонального препарата сводится к гипопластическим процессам в эндометрии. Из эстроген-гестагенных препаратов применяются биссекурин, марвелон, фемоден, мерсилон, которые назначаются по 1 таблетке в день с 5 по 25 день цикла в течение 6 мес.; из гестагенов – норколут 5–10 мг в день или медроксипрогестерона ацетат – 20 мг в день с 16 по 26 день цикла. При рецидивирующих гиперпластических процессах, аденоматозе показана терапия гестагенами в непрерывном режиме (провера по 250 мг 2–3 раза в неделю) в течение 6 мес с проведением контрольного диагностического выскабливания через 3 и 6 мес от начала лечения. Следует напомнить, что показанием к резекции яичников является не только бесплодие, но и рецидивирующие гиперпластические процессы у женщин с СПКЯ. Перспективным в лечении аденоматоза у женщин репродуктивного возраста, в частности не выполнивших генеративную функцию, является назначение аналогов гонадолиберина (Г.Е. Чернуха, В.П. Сметник, 1998) – золадекс, декапептил и другие в течение 6 месяцев. Однако высокая стоимость лечения ограничивает его широкое применение в практике.
Вторым этапом в лечении гиперпластических процессов является восстановление овуляторных менструальных циклов, что наблюдается часто после отмены гормонотерапии (ребаунд эффект). Можно также назначать кломифен – по общепринятой схеме под контролем базальной температуры.
Непременным условием проведения терапии гиперпластических процессов эндометрия является коррекция метаболических нарушений (гиперинсулинемии, гипергликемии, дислипидемии) на фоне редукционной диеты и медикаментозных препаратов. В противном случае возможен рецидив, что связано с образованием эстрогенов в жировой ткани.
Лечение гирсутизма является наиболее трудной задачей. На уровне волосяного фолликула происходит превращение тестостерона в активный дигидротестостерон под влиянием фермента 5a-редуктазы. Немаловажное значение играет повышение свободного тестостерона, что усугубляет клинические проявления гиперандрогении.
Лечение гирсутизма предусматривает блокирование действия андрогенов различными путями:
- торможение синтеза в эндокринных железах,
- увеличение концентрации ПССГ, т.е. снижение биологически активных андрогенов,
- торможение синтеза дигидротестостерона в ткани-мишени за счет угнетения активности фермента 5a-редуктазы,
- блокада рецепторов к андрогенам на уровне волосяного фолликула.
Непременным условием лечения гирсутизма у женщин с ожирением является нормализация массы тела. Показана четкая положительная корреляция между уровнем андрогенов и ИМТ.
Комбинированные оральные контрацептивы (КОК) широко используются для лечения гирсутизма, особенно при нерезко выраженных формах. Механизм действия КОК основан на подавлении синтеза ЛГ, а также повышении уровня ПССГ, что снижает концентрацию свободных андрогенов. Наиболее эффективны по клиническим исследованиям КОК, содержащие дезогестрел, гестоден, норгестимат.
Одним из первых антиандрогенов был ципротеронацетат (андрокур) – по химической структуре прогестаген, производное медроксипрогестерон ацетата (МПА). Механизм действия основан на блокаде рецепторов андрогенов в ткани-мишени и подавлении гонадотропной секреции. Антиандрогеном также является Диане-35, сочетание 2 мг ципротеронацетата с 35 мкг этинилэстрадиола, обладающий еще и контрацептивным эффектом. Усиление антиандрогенного эффекта Диане можно получить дополнительным назначением Андрокура по 25–50 мг с 5 по 15 день цикла. Длительность лечения от 6 мес до 2 лет и более. Препарат переносится хорошо, из побочных эффектов иногда в начале приема отмечается вялость, отеки, масталгия, прибавка в весе и снижение либидо (полового чувства).
Спиронолактон (верошпирон) также обладает антиандрогенным эффектом, блокируя периферические рецепторы и синтез андрогенов в надпочечниках и яичниках, снижая активность цитохрома Р450с17; подавляет активность фермента 5a-редуктазы, способствует снижению массы тела. При длительном приеме по 100 мг в день отмечается уменьшение гирсутизма. Побочное действие: слабый диуретический эффект (в первые 5 дней лечения), вялость, сонливость. Длительность лечения от 6 до 24 месяцев и более.
Флютамид – нестероидный антиандроген, используемый для лечения рака простаты. Механизм действия основан в основном на торможении роста волоса путем блокады рецепторов и незначительного подавления синтеза тестостерона. Побочного действия не отмечено. Назначается по 250–500 мг в день в течение 6 мес и более. Уже через 3 мес отмечен выраженный клинический эффект без изменения уровня андрогенов в крови. Поскольку не обладает контрацептивным эффектом, можно сочетать с ОК.
Финастерид – специфический ингибитор фермента 5a-редуктазы, под влиянием которого происходит образование активного дигидротестостерона. Основное назначение препарата — лечение доброкачественной гиперплазии простаты. В России флютамид и финастерид для лечения гирсутизма применяются редко.
Агонисты гонадотропных рилизинговых гормонов (а-ГнРГ) (Золадекс, Люкрин-депо, Буселерин, Декапептил) эффективны в лечении гирсутизма при СПКЯ, особенно при высоком ЛГ. Механизм действия основан на блокаде гонадотропной функции гипофиза и, следовательно, ЛГ-зависимого синтеза андрогенов в тека-клетках яичников. Недостатком является появление характерных для климактерического синдрома жалоб в связи с резким снижением функции яичников. Эти препараты для лечения гирсутизма используются редко.
Медикаментозное лечение гирсутизма не всегда эффективно, поэтому широкое распространение получили различные виды эпиляции (электор-лазерной, химической и механической).
Гиперандрогения и хроническая ановуляция наблюдается при таких эндокринных нарушениях, как АГС, нейрообменноэндокринном синдроме, болезнь Кушинга и гиперпролактинемия. При этом в яичниках развиваются морфологические изменения, сходные с СПКЯ. В подобных случаях речь идет о так называемых вторичных ПКЯ и основным принципом лечения является терапия вышеперечисленных заболеваний.
Формин (метформин) - Досье препарата
Комментарии (видны только специалистам, верифицированным редакцией МЕДИ РУ) Если Вы медицинский специалист, войдите или зарегистрируйтесьmedi.ru
Синдром поликистозных яичников | Гинекология/Акушерство
Общие сведения
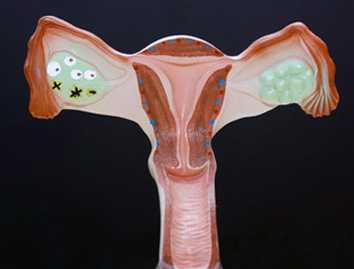
Синдром поликистозных яичников (СПКЯ), также известный как синдром Штейна-Левенталя или склерокистоз яичников, представляет собой эндокринное (гормональное) заболевание, при котором яичники увеличены и содержат множество маленьких пузырьков, заполненных жидкостью. СПКЯ - довольно частое заболевание. Поликистоз возникает, когда яичники в избытке продуцируют мужские гормоны (андрогены), которые в норме образуются в очень небольших количествах.
В течение каждого менструального цикла в яичниках формируется множество маленьких фолликулов (пузырьков), из которых впоследствии может выйти яйцеклетка. В норме в середине менструального цикла во время овуляции (разрыва фолликула) одна яйцеклетка покидает один из фолликулов (какого-либо яичника), а другие фолликулы перезревают и перестают работать. При СПКЯ, яйцеклетка не вызревает и овуляции не происходит. Фолликулы не разрываются, а заполняются жидкостью и превращаются в кисты. Соответственно, яичники могут увеличиваться в размерах, становясь больше нормальных в 2-5 раз.
У женщин, страдающих синдромом поликистозных яичников, часто проявляются мужеподобные черты, такие как избыточный рост волос на лице и теле, прыщи, затылочная плешь и абдоминальные жировые отложения (жир откладывается на талии). По оценкам врачей он поражает около 5-10% всех женщин, ещё не прошедших через менопаузу. Это одна из основных причин бесплодия, к тому же многие женщины не знают, что больны.
Причины
Единого мнения среди врачей до сих пор нет. Однако известно, что это заболевание связано с нечувствительностью тканей организма к инсулину (гормон, участвующий в регуляции уровня сахара в крови). Недавние исследования дают возможность предположить, что яичники женщин, страдающих синдромом поликистозных яичников, в избытке продуцируют мужские половые гормоны, поскольку организм не может должным образом перерабатывать инсулин. Уровень инсулина в крови настолько высок, что яичники реагируют на него избыточной продукцией мужских половых гормонов.
Cимптомы
Симптомы могут проявиться в любом возрасте. Могут развиться в течение пубертатного периода, и тогда менструальный период может задержаться или вообще не прийти. Девушки могут страдать избыточным весом и иметь рост волос по мужскому типу, например, на груди и на лице. Также у них может быть нарушен менструальный цикл, а менструальное кровотечение быть достаточно тяжелым.
У каждой женщины симптомы могут немного отличаться, хотя обычно наблюдаются отдельные или все из следующих симптомов:
- избыточный рост волос на лице, груди и животе; - отсутствие или нерегулярные менструальные кровотечения; - кровотечения из матки;
- повышенное артериальное давление;
- прыщи;- ожирение в области талии;
- тонкие волосы и облысение по мужскому типу; - бесплодие.Как мы уже упоминали, синдром поликистозных яичников сопровождается симптомами диабета, такими как полнота или усиленное мочевыделение, вагинальная молочница (кандидоз) или хронические кожные инфекции. Поликистоз яичников виден при ультразвуковом исследовании, хотя и не всегда. У 20% женщин (не прошедших ещё через менопаузу), не имеющих симптомов поликистоза как такового, при ультразвуковом исследовании обнаруживают поликистозные яичники.
Осложнения
Синдром Штейна-Левенталя может повысить вероятность развития некоторых заболеваний. Поэтому важно проводить регулярные медицинские обследования. Даже в том случае, если некоторые симптомы синдрома поликистозных яичников частично исчезают после наступления менопаузы, через определённое время могут проявиться различные заболевания.
Сахарный диабет 2 типа. К моменту достижения менопаузы около 50% женщин со склерокистозом яичников диагностируется диабет 2 типа. Поэтому так важно заранее начать вести правильный образ жизни и соблюдать здоровую диету.
Повышенный уровень холестерина. Повышенный уровень тестостерона может служить причиной возрастания уровня ЛПНП (так называемая «плохая» форма холестерина) в вашем организме, что в итоге приводит к повышению риска сердечных заболеваний и сердечных приступов.
Рак эндометрия. Поскольку у женщин с синдромом поликистозных яичников овуляция не происходит часто, у них есть периоды, в течение которых эндометрий чрезмерно наращивается. Это может увеличить риск онкологических заболеваний стенки матки, хотя точных данных об этом явлении пока нет.
Что можете сделать Вы
Доктор может посоветовать соблюдать определённую диету, чтобы попытаться нормализовать уровень инсулина и поддерживать в норме уровень холестерина. Также очень важно снижение веса и поддержание хорошей физической подготовки, уже сами по себе эти меры помогают некоторым женщинам с СПКЯ реализовать желание забеременеть.
Что может сделать врач
Вашему врачу нужно будет оценить симптомы, исходя из данных вашей медицинской карты и общего осмотра. Если у вас предполагают синдром поликистозных яичников, врач назначит соответствующие анализы, чтобы подтвердить его и исключить другие возможные заболевания.
Необходимое обследование: ультразвуковое исследование (покажет общий вид ваших яичников), анализы крови – общий уровень мужских половых гормонов, инсулина, глюкозы, холестерина, или лютеинизирующего гормона.
Хотя синдром поликистозных яичников невозможно вылечить, некоторые симптомы всё же можно держать под контролем. Лечение будет зависеть от вашего набора симптомов, того, насколько остро они проявляются и вашего отношения к возможности забеременеть.
Лекарственные средства
Вам могут выписать прогестаген (синтетический аналог женского полового гормона прогестерона) или противозачаточные средства, чтобы индуцировать регулярные менструальные циклы.
Некоторые противозачаточные средства с низкой концентрацией активных компонентов, обычно имеющиеся в продаже содержат эстроген и небольшое количество анти-андрогена (вещество, блокирующее эффекты мужских половых гормонов) ципротерон ацетат. Это помогает эффективно контролировать избыточный рост волос и появление прыщей. Ацетат ципротерона доступен и сам по себе и ваш доктор может посоветовать вам этот или другой анти-андроген, спиронолактон, действующий схожим образом. С избыточным ростом волос можно бороться одновременно с помощью медикаментов и эпиляционных процедур. Ваш врач подберёт способ, оптимальный для вас.
Изотретиноин используется в случае наличия обильной угревой сыпи. Этот препарат уменьшает количество сальных выделений кожи и сокращает количество кожных желёз, их продуцирующих. Из-за наличия побочных эффектов этот медикамент может быть выписан только специальным врачом. Он противопоказан беременным и планирующим беременность, поскольку есть опасность повредить ребёнку.
Также вам могут быть прописаны лекарства, такие как метформин, помогающие организму правильно использовать продуцируемый им инсулин. Эти лекарства способствуют снижению массы тела и понижению артериального давления у больных с синдромом поликистозных яичников, а иногда позволяет восстановить менструальный цикл. Кроме того, оно позволяет контролировать избыточный рост волос, вызванное повышенным уровнем тестостерона.
Используя все эти препараты, вы должны понимать, что их эффект проявляется не сразу. Также учтите, что в случае если медикаменты, направленные на снижение роста волос, неэффективны, вам придётся воспользоваться другими методами, такими как лазерное удаление волос, восковая или электроэпиляция.
Лечение бесплодия может включать использование таких лекарств, как цитрат кломифена, стимулирующий рост фолликулов в яичниках и образование яйцеклетки в середине менструального цикла, или инъекции синтетических гормонов, схожих с теми, которые естественным путём вырабатывает ваш организм.
Лечение хирургическим путём
В качестве лечения бесплодия ваш доктор может предложить вам хирургическую процедуру - лапароскопию. При этом используется либо раскалённая игла, либо лазерный луч, чтобы прижечь яичник в нескольких местах. Эта процедура может стимулировать овуляцию и повысить ваши шансы забеременеть. Однако хирургическое вмешательство обычно считается крайней мерой, поскольку тканевой шрам может впоследствии деформировать яичники, что может отрицательно повлиять на вашу способность забеременеть.
www.vidal.ru
Синдром поликистозных яичников
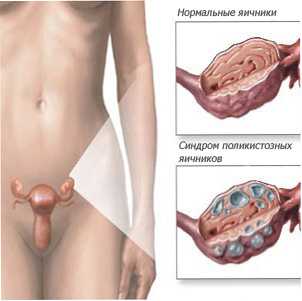 |
| СПКЯ часто сопровождает ожирением и повышенным оволосением (гирсутизмом) |
Синдром поликистозных яичников (СПКЯ)— патология структуры и функции яичников, основными критериями которой являются хроническая ановуляция и гиперандрогения. Частота СПКЯ в структуре эндокринного бесплодия достигает 75%.
Симптомы синдрома поликистозных яичников
Нарушение менструального цикла по типу олиго-, аменореи. Поскольку нарушение гормональной функции яичников начинается с пубертатного периода, то и нарушения цикла начинаются с менархе и не имеют тенденции к нормализации. Следует отметить, что возраст менархе соответствует таковому в популяции — 12-13 лет (в отличие от надпочечниковой гиперандрогении при адреногенитальном синдроме, когда менархе запаздывает). Примерно у 10-15% пациенток нарушения менструального цикла имеют характер дисфункциональных маточных кровотечений на фоне гиперпластических процессов эндометрия. Поэтому женщины с СПКЯ входят в группу риска развития аденокарциномы эндометрия, фиброзно-кистозной мастопатии и рака молочных желез, а также проблем с беременностью.
Ановуляторное бесплодие. Бесплодие имеет первичный характер в отличие от надпочечниковой гиперандрогении, при которой возможна беременность и характерно ее невынашивание.
Гирсутизм различной степени выраженности развивается постепенно с периода менархе, в отличие от адреногенитального синдрома, когда гирсутизм развивается до менархе, с момента активации гормональной функции надпочечников в период адренархе.
Превышение массы тела отмечается примерно у 70% женщин и соответствует II-III степени ожирения. Ожирение чаще имеет универсальный характер, о чем свидетельствует отношение объема талии к объему бедра (ОТ/ОБ) менее 0,85, характеризующее женский тип ожирения. Соотношение ОТ/ОБ более 0,85 характеризует кушингоидный (мужской) тип ожирения и встречается реже.
Молочные железы развиты правильно, у каждой третьей женщины имеет место фиброзно-кистозная мастопатия, развивающаяся на фоне хронической ановуляции и гиперэстрогении.
В последние годы, когда начали изучать особенности метаболизма при СПКЯ, было установлено, что часто имеют место инсулинорезистентностъ и компенсаторная гиперинсулинемия — нарушения углеводного и жирового обмена по диабетоидному типу. Отмечается также дислипидемия с преобладанием липопротеинов атерогенного комплекса (холестерина, триглицеридов, ЛПНП и ЛПОНП). Это, в свою очередь, повышает риск развития сердечно-сосудистых заболеваний во втором-третьем десятилетии жизни, т. е. в возрастных периодах, которым эти заболевания не свойственны.
Причины синдрома поликистозных яичников
Единого мнения о причинах развития заболевания до сих пор не существует.
СПКЯ является многофакторной патологией, возможно, генетически детерминированной, в патогенезе которой действуют центральные механизмы регуляции гонадотропной функции гипофиза с пубертатного периода, местные яичниковые факторы, экстраовариальные эндокринные и метаболические нарушения, определяющие клиническую симптоматику и морфологические изменения яичников.
Диагностика синдрома поликистозных яичников
- Гиперплазией стромы;
- гиперплазией клеток теки с участками лютеинизации;
- наличием множества кистозно-атрезирующихся фолликулов диаметром 5-8 мм, расположенных под капсулой в виде «ожерелья»;
- утолщением капсулы яичников.
Характерный анамнез, внешний вид и клиническая симптоматика облегчают диагностику СПКЯ. В современной клинике диагноз можно поставить без гормональных исследований, хотя они тоже имеют характерные особенности.
Диагноз поликистозных яичников может быть установлен при трансвагинальном УЗИ, так как описаны четкие критерии эхоскопической картины: объем яичников более 9 см3, гиперплазированная строма составляет 25% объема, более десяти атретичных фолликулов диаметром до 10 мм, расположенных по периферии под утолщенной капсулой.
Объем яичников определяется по формуле: V = 0,523 ( L х Sx Н) см3, где V , L , S , Н — соответственно объем, длина, ширина и толщина яичника; 0,523 — постоянный коэффициент. Увеличение объема яичников за счет гиперплазированной стромы и характерное расположение фолликулов помогают дифференцировать поликистозные яичники от нормальных (на 5-7-й день цикла) или мультифолликулярных. Последние характерны для раннего пубертата, гипогонадотропной аменореи, длительного приема КОК. Мультифолликулярные яичники характеризуются при УЗИ небольшим числом фолликулов диаметром 4-10 мм, расположенных по всему яичнику, обычной картиной стромы и, главное, нормальным объемом яичников (4-8 см3).
Таким образом, УЗИ является неинвазивным, высокоинформативным методом, который можно считать «золотым стандартом» в диагностике СПКЯ.
Гормональная характеристика СПКЯ. Критериями диагностики являются: повышение уровня ЛГ, увеличение соотношения ЛГ/ФСГ более 2,5, увеличение уровня общего и свободного Т при нормальном содержании ДЭА-С и 17-ОНП.
После пробы с дексаметазоном содержание андрогенов незначительно снижается, примерно на 25% (за счет надпочечниковой фракции).
Проба с АКТГ отрицательная, что исключает надпочечниковую гиперандрогению, характерную для адреногенитального синдрома. Отмечено также повышение уровня инсулина и снижение ПССГ в крови.
Метаболические нарушения при СПКЯ характеризуются повышением уровня триглицеридов, ЛПНП, ЛПОНП и снижением ЛПВП.
В клинической практике простым и доступным методом определения нарушения толерантности глюкозы к инсулину является сахарная кривая. Определяется сахар крови сначала натощак, затем — в течение 2 ч после приема 75 г глюкозы. Если через 2 ч уровень сахара крови не приходит к исходным цифрам, это свидетельствует о нарушенной толерантности к глюкозе, т. е. об инсулинрезистентности, что требует соответствующего лечения.
Биопсия эндометрия показана женщинам с ациклическими кровотечениями в связи с большой частотой гиперпластических процессов эндометрия.
Критериями для постановки диагноза СПКЯ являются:
- Своевременный возраст менархе;
- нарушение менструального цикла с периода менархе в подавляющем большинстве случаев по типу олигоменореи;
- гирсутизм и ожирение с периода менархе у более 50% женщин;
- первичное бесплодие;
- хроническая ановуляция;
- увеличение объема яичников за счет стромы по данным трансвагинальной эхографии;
- повышение уровня Т;
- увеличение ЛГ и отношения ЛГ/ФСГ > 2,5.
Этапы лечения синдрома поликистозных яичников
Как правило, пациентки с СПКЯ обращаются к врачу с жалобами на бесплодие. Поэтому целью лечения является восстановление овуляторных циклов.
При СПКЯ с ожирением и с нормальной массой тела последовательность терапевтических мер различна.
При наличии ожирения:
- Первый этап терапии — нормализация массы тела. Снижение массы тела на фоне редукционной диеты приводит к нормализации углеводного и жирового обмена. Диета при СПКЯ предусматривает снижение общей калорийности пищи до 2000 ккал в день, из них 52% приходится на углеводы, 16% — на белки и 32% — на жиры, причем насыщенные жиры должны составлять не более 1/3 общего количества жира. Важным компонентом диеты является ограничение острой и соленой пищи, жидкости. Очень хороший эффект отмечается при использовании разгрузочных дней, голодание не рекомендуется в связи с расходом белка в процессе глюконеогенеза. Повышение физической активности является важным компонентом не только для нормализации массы тела, но и повышения чувствительности мышечной ткани к инсулину. Самое главное, необходимо убедить пациентку в необходимости нормализации массы тела, как первого этапа в лечении СПКЯ.
- Второй этап терапии — медикаментозное лечение метаболических нарушений (инсулинорезистентности и гиперинсулинемии) в случае отсутствия эффекта от редукционной диеты и физических нагрузок. Препаратом, повышающим чувствительность периферических тканей к инсулину, является метформин. Метформин приводит к снижению периферической инсулинорезистентности, улучшая утилизацию глюкозы в печени, мышцах и жировой ткани; нормализует липидный профиль крови, снижая уровень триглицеридов и ЛПНП. Препарат назначается по 1000-1500 мг в сутки в течение 3-6 месяцев под контролем глюкозотолерантного теста.
- Третий этап терапии – стимуляция овуляции после нормализации массы тела и при СПКЯ при нормальной массе тела. Стимуляция овуляции проводится после исключения трубного и мужского факторов бесплодия.
Терапевтические методы стимуляции овуляции при СПКЯ
После нормализации массы тела и при СПКЯ при нормальной массе тела показана стимуляция овуляции. Стимуляция овуляции проводится после исключения трубного и мужского факторов бесплодия.
Большинство врачей начинают индукцию овуляции с применения «Кломифена». Надо отметить, что длительно применявшийся метод стимуляции овуляции с использованием эстроген-гестагенных препаратов, основанный на ребаунд-эффекте после их отмены, не потерял своей популярности. При отсутствии эффекта от терапии эстроген-гестагенами и «Кломифеном» рекомендуется назначение гонадотропинов или хирургическая стимуляция овуляции.
«Кломифен» относится к нестероидным синтетическим эстрогенам. Механизм его действия основан на блокаде рецепторов эстрадиола. После отмены «Кломифена» по механизму обратной связи происходит усиление секреции ГнРГ, что нормализует выброс ЛГ и ФСГ и, соответственно, рост и созревание фолликулов в яичнике. Таким образом, «Кломифен» не стимулирует яичники непосредственно, а оказывает воздействие через гипоталамо-гипофизарную систему. Стимуляция овуляции «Кломифеном» начинается с 5-го по 9-й день менструального цикла, по 50 мг в день. При таком режиме повышение уровня гонадртропинов, индуцированное препаратом, происходит в то время, когда уже завершился выбор доминантного фолликула. Более раннее назначение может стимулировать развитие множества фолликулов и увеличивает риск многоплодной беременности. При отсутствии овуляции по данным УЗИ и базальной температуры дозу «Кломифена» можно увеличивать в каждом последующем цикле на 50 мг, до достижения 200 мг в день. Однако многие клиницисты полагают, что если нет эффекта при назначении 100-150 мг «Кломифена», дальнейшее увеличение дозы нецелесообразно. При отсутствии овуляции при максимальной дозе в течение 3 месяцев пациентку можно считать резистентной к препарату.
Критериями эффективности стимуляции овуляции служат:
- Восстановление регулярных менструальных циклов с гипертермической базальной температурой в течение 12-14 дней;
- уровень прогестерона в середине второй фазы цикла 5 нг/мл и более, преовуляторный пик ЛГ;
- УЗИ-признаки овуляции на 13-15-й день цикла:
- наличие доминантного фолликула диаметром не менее 18 мм;
- толщина эндометрия не менее 8-10 мм.
При наличии этих показателей рекомендуется введение овуляторной дозы 7500-10000 МЕ человеческого хорионического гонадотропина — чХГ («Профази», «Хорагон», «Прегнил»), после чего овуляция отмечается через 36-48 ч. При лечении «Кломифеном» следует учитывать, что он обладает антиэстрогенными свойствами, уменьшает количество цервикальной слизи («сухая шейка»), что препятствует пенетрации сперматозоидов и тормозит пролиферацию эндометрия и приводит к нарушению имплантации в случае оплодотворения яйцеклетки. С целью устранения этих нежелательных эффектов препарата рекомендуется после окончания приема «Кломифена» принимать натуральные эстрогены в дозе 1-2 мг или их синтетические аналоги («Микрофоллин») с 10-го по 14-й день цикла для повышения проницаемости шеечной слизи и пролиферации эндометрия.
При недостаточности лютеиновой фазы рекомендуется назначить гестагены во вторую фазу цикла с 16-го по 25-й день. При этом предпочтительнее препараты прогестерона («Дюфастон», «Утрожестан»).
Частота индукции овуляции при лечении «Кломифеном» составляет примерно 60-65%, наступление беременности — в 32-35% случаев, частота многоплодной беременности, в основном двойней, составляет 5-6%, риск внематочной беременности и самопроизвольных выкидышей не выше, чем в популяции. При отсутствии беременности на фоне овуляторных циклов требуется исключение перитонеальных факторов бесплодия при лапароскопии.
При резистентности к «Кломифену» назначают гонадотропные препараты — прямые стимулятороы овуляции. Используется человеческий менопаузальный гонадотропин (чМГ), приготовленный из мочи женщин постменопаузального возраста. Препараты чМГ содержат ЛГ и ФСГ, по 75 МЕ («Пергонал», «Меногон», «Менопур» и др.). При назначении гонадотропинов пациентка должна быть информирована о риске многоплодной беременности, возможном развитии синдрома гиперстимуляции яичников, а также о высокой стоимости лечения. Лечение синдрома поликистозных яичников должно проводиться только после исключения патологии матки и труб, а также мужского фактора бесплодия. В процессе лечения обязательным является трансвагинальный УЗ-мониторинг фолликулогенеза и состояния эндометрия. Овуляция инициируется путем однократного введения чХГ в дозе 7500-10000 МЕ, когда имеется хотя бы один фолликул диаметром 17 мм. При выявлении более 2 фолликулов диаметром более 16 мм или 4 фолликулов диаметром более 14 мм введение чХГ нежелательно из-за риска наступления многоплодной беременности.
При стимуляции овуляции гонадотропинами частота наступления беременности повышается до 60%, риск многоплодной беременности составляет 10-25%, внематочной — 2,5-6%, самопроизвольные выкидыши в циклах, закончившихся беременностью, достигают 12-30%, синдром гиперстимуляции яичников наблюдается в 5-6% случаев.
Хирургические методы стимуляции овуляции при СПКЯ
Хирургический метод стимуляции овуляции (клиновидная резекция яичников) в последние годы проводится лапароскопическим путем, тем самым обеспечивается минимальное инвазивное вмешательство и снижается риск спайкообразования. Кроме того, преимуществом лапароскопической резекции является возможность ликвидации часто сопутствующего перитонеального фактора бесплодия. Помимо клиновидной резекции, при лапароскопии можно производить каутеризацию яичников с помощью различных видов энергии (термо-, электро-, лазерной), которая основана на разрушении стромы точечным электродом. Производится от 15 до 25 пунктур в каждом яичнике; операция менее травматичная и длительная по сравнению с клиновидной резекцией.
В большинстве случаев в послеоперационном периоде через 3-5 дней наблюдается менструальноподобная реакция, а через 2 недели — овуляция, которая тестируется по базальной температуре. Отсутствие овуляции в течение 2-3 циклов требует дополнительного назначения «Кломифена». Как правило, беременность наступает в течение 6-12 месяцев, в дальнейшем частота наступления беременности уменьшается. Отсутствие беременности при наличии овуляторных менструальных циклов диктует необходимость исключения трубного фактора бесплодия.
Частота индукции овуляции при любой лапароскопической методике примерно одинакова и составляет 84-89%, наступление беременности в среднем отмечается в 72% случаев.
Несмотря на достаточно высокий эффект при стимуляции овуляции и наступлении беременности, большинство клиницистов отмечают рецидив клинической симптоматики примерно через 5 лет. Поэтому после беременности и родов необходима профилактика рецидива СПКЯ, что важно, учитывая риск развития гиперпластических процессов эндометрия. С этой целью наиболее целесообразно назначение КОК, предпочтительнее монофазных («Марвелон», «Фемоден», «Диане», «Мерсилон» и др.). При плохой переносимости КОК, что бывает при избыточной массе тела, можно рекомендовать гестагены во вторую фазу цикла: «Дюфастон» в дозе 20 мг с 16-го по 25-й день цикла.
Женщинам, не планирующим беременность, после первого этапа стимуляции овуляции «Кломифеном», направленного на выявление резервных возможностей репродуктивной системы, также рекомендуется назначение КОК или гестагенов для регуляции цикла, уменьшения гирсутизма и профилактики гиперпластических процессов.
Техника операции клиновидной резекции яичника
Показания: синдром склерокистозных яичников. При этом яичники увеличены в 2-5 раз, иногда меньше нормальных, покрыты плотной толстой фиброзной оболочкой белесоватого или серого цвета.
Характерными особенностями являются также отсутствие в яичниках желтых тел, очень малое число мелких недозревших фолликулов.
При синдроме склерокистозных яичников, несмотря на их большую массу, во много раз превосходящую массу нормальных яичников, их гормональная функция часто бывает пониженной. Клинически это нередко проявляется нарушением менструальной функции, гипоменструальным синдромом или аменореей. У части больных иногда наблюдается созревание и разрыв фолликулов. В этих случаях детородная функция может быть не нарушена, хотя, как правило, при синдроме склерокистозных яичников наблюдается нарушение менструальной функции и бесплодие.
Общепризнанной методикой оперативного лечения синдрома склерокистозных яичников является краевая клиновидная резекция обоих яичников; рекомендуется иссекать две трети массы каждого яичника.
Техника операции проста. После лапаротомии из брюшной полости выводят сначала один, затем второй яичник. Трубный конец яичника прошивают (берут на «держалку») для удобства манипулирования и приступают к выполнению основной части операции.
Удерживая яичник пальцами левой руки, правой иссекают по свободному краю значительную часть его тканей — от половины до двух третей. Лучше всего это делать скальпелем. Следует помнить, что если лезвие скальпеля будет проникать очень глубоко в направлении ворот яичника, то могут быть повреждены кровеносные сосуды, перевязка которых вызывает развитие ишемии оставшихся тканей яичника. Это незамедлительно отрицательно повлияет на результаты операции. Если ранение яичниковых сосудов во время операции останется незамеченным, в послеоперационный период возникнет внутреннее кровотечение, для остановки которого неизбежно придется произвести релапаротомию и прошивание кровоточащих сосудов. При зашивании яичника не следует стараться тщательно соединять края раны.
Если они немного расходятся в дальнейшем легче будет происходить овуляция.
После туалета брюшной полости приступают к восстановлению целости передней стенки живота послойным сшиванием краев операционной раны и в заключение накладывают асептическую повязку.
Основными моментами операции краевой клиновидной резекции яичника после лапаротомии являются следующие:
- Осмотр матки, обоих яичников и маточных труб;
- прошивание трубного конца каждого яичника (взятие их на «держалки»);
- краевая клиновидная резекция двух третей массы обоих яичников при мелкокистозном их перерождении, обусловленном персистенцией фолликулов, или при склерокистозном перерождении яичников (синдром Штейна-Левенталя);
- при обнаружении опухоли во время операции производят иссечение в пределах здоровых тканей;
- прокалывание или диатермопунктура персистирующих фолликулов;
- восстановление целости яичников наложением непрерывного кетгутового шва или узловатых швов;
- туалет брюшной полости;
- послойное зашивание операционной раны;
- асептическая повязка.
Лечение гиперпластических процессов при СПКЯ
Лечение гиперпластических процессов эндометрия (см. гиперплазия эндометрия, а также статью о ее лечении). Рецидивирующие гиперпластические процессы эндометрия при СПКЯ являются показанием к резекции яичников.
Лечение гирсутизма
Лечение гирсутизма является наиболее трудной задачей, что обусловлено не только гиперсекрецией андрогенов, но и их периферическим метаболизмом.
На уровне ткани-мишени, в частности волосяного фолликула, происходит превращение Т в активный дигидротестостерон под влиянием фермента 5α-редуктазы. Немаловажное значение играет повышение фракций свободных андрогенов, что усугубляет клинические проявления гиперандрогении.
Лечение гирсутизма предусматривает блокирование действия андрогенов различными путями:
- Торможение синтеза в эндокринных железах;
- увеличение концентрации ПССГ, т. е. снижение биологически активных андрогенов;
- торможение синтеза дигидротестостерона в ткани-мишени за счет угнетения активности фермента 5α-редуктазы;
- блокада рецепторов к андрогенам на уровне волосяного фолликула.
Учитывая роль жировой ткани в синтезе андрогенов, непременным условием при лечении гирсутизма у женщин с ожирением является нормализация массы тела. Показана четкая положительная корреляция между уровнем андрогенов и индексом массы тела. Кроме того, учитывая роль инсулина в гиперандрогении у женщин с СПКЯ, необходима терапия инсулинорезистентности.
Комбинированные оральные контрацептивы широко используются для лечения гирсутизма, особенно при нерезко выраженных формах. Механизм действия КОК основан на подавлении синтеза ЛГ, а также повышении уровня ПССГ, что снижает концентрацию свободных андрогенов. Наиболее эффективны, исходя из клинических исследований, КОК, содержащие дезогестрел, гестоден, норгестимат.
Одним из первых антиандрогенов был ципротеронацетат («Андрокур»), механизм действия которого основан на блокаде рецепторов андрогенов в ткани-мишени и подавлении гонадотропной секреции. Антиандрогеном также является «Диане-35», сочетающий 2 мг ципротеронацетата с 35 мкг этинилэстрадиола, обладающий еще и контрацептивным эффектом. Усиления антиандрогенного эффекта «Диане» можно добиться дополнительным назначением «Андрокура» — по 25-50 мг с 5-го по 15-й день цикла. Длительность лечения составляет от 6 месяцев до 2 лет и более. Препарат переносится хорошо, из побочных эффектов иногда в начале приема отмечается вялость, пастозность, масталгия, прибавка в весе и снижение либидо.
«Спиронолактон» («Верошпирон») также обладает антиандрогенным эффектом. Блокирует периферические рецепторы и синтез андрогенов в надпочечниках и яичниках, способствует снижению массы тела. При длительном приеме по 100 мг в день отмечается уменьшение гирсутизма. Побочное действие: слабый диуретический эффект (в первые 5 дней лечения), вялость, сонливость. Длительность лечения — от 6 месяцев до 2 лет и более.
«Флутамид» — нестероидный антиандроген, используемый при лечении рака простаты. Механизм действия основан преимущественно на торможении роста волос путем блокады рецепторов и незначительного подавления синтеза Т. Побочного действия не отмечено. Назначается по 250-500 мг в день в течение 6 месяцев и более. Уже через 3 месяца отмечен выраженный клинический эффект без изменения уровня андрогенов в крови.
Агонисты гонадотропных рилизинговых гормонов («Золадекс», «Диферелин депо», «Бусерелин», «Декапептил») для лечения гирсутизма используются редко. Их можно назначать при высоком уровне ЛГ. Механизм действия основан на блокаде гонадотропной функции гипофиза и, следовательно, ЛГ-зависимого синтеза андрогенов в клетках теки яичников. Недостатком является появление характерных для климактерического синдрома жалоб, обусловленных резким снижением функции яичников. Эти препараты для лечения гирсутизма используются редко.
Медикаментозное лечение гирсутизма не всегда эффективно, поэтому широкое распространение получили различные виды эпиляции (электро-, лазерной, химической и механической).
Гиперандрогения и хроническая ановуляция наблюдаются при таких эндокринных нарушениях, как адреногенитальный синдром, нейрообменно-эндокринный синдром, болезнь Кушинга и гиперпролактинемия. При этом в яичниках развиваются морфологические изменения, сходные с синдромом поликистозных яичников, и имеет место гиперандрогения. В подобных случаях речь идет о так называемых вторичных поликистозных яичниках и основным принципом лечения является терапия вышеперечисленных заболеваний.
ztema.ru
Синдром поликистозных яичников: противоречия в диагностике
Авторы: Березовская Е.П.
Вокруг синдрома поликистозных яичников (СПКЯ) создано чрезвычайно много мифов, основанных на отсутствии как четкого понимания причин и механизмов возникновения этого заболевания, так и четких диагностических критериев и эффективного лечения. Это заболевание поражает женщин репродуктивного возраста, а одним из признаков его является наличие множественных мелких кист (фолликулов) в яичниках. Это заболевание имеет и другие названия: болезнь поликистозных яичников, синдром Штейна-Левенталя, метаболический сидром, синдром Х, синдром микрокистозных яичников, синдром мелкокистозных яичников, синдром склерокистозных яичников, СПЯ…
В классическую триаду диагностических признаков, описанных в 1935 году Штейном и Левенталем, входили ожирение, гирсутизм и акне. Об уровне мужских половых гормонов и других признаках СПКЯ в те времена ничего еще не знали, как и о состоянии яичников, которое теперь можно увидеть и оценить с помощью УЗИ. Эндокринологические изменения тогда доминировали в постановке диагноза, и современная гинекология возвращается к пониманию того, что СПКЯ — это эндокринопатия, гормонально-метаболический синдром.
СКПЯ встречается у 5–10% пациенток, начиная от подростков и заканчивая женщинами в менопаузе, однако частота может где-то оказаться большей из-за чрезмерного злоупотребления этим диагнозом. Причины возникновения синдрома до сих пор не известны, но считается, что нарушения возникают в гипоталамо-гипофизарной системе и связаны с неправильной выработкой гонадотропинов — гормонов, которые регулируют функцию яичников. Не исключено и вовлечение определенных генов, так как при наблюдениях больных с СПКЯ нередко фиксируется наследование по женской линии.
Казалось бы, с прогрессом науки и медицины, развития доказательной медицины в постановке СПКЯ должны использоваться международные стандарты, приемлемые большинством прогрессивных врачей мира, но в реальности наблюдается, что это один из немногочисленных диагнозов, когда врачи не могут прийти к общей точке зрения.
Во-первых, в постановку этого диагноза вовлечены как гинекологи, так и эндокринологи, а промежуточную роль в диагностике играют врачи-радиологи (УЗИ-врачи). Эндокринологи акцентируют внимание на изменениях уровней гормонов и ряда веществ, гинекологи — на нарушении менструального цикла и нередко проблемах с зачатием ребенка. УЗИ-специалисты утверждают, что почти у трети здоровых женщин можно обнаружить поликистозные яичники. Однако при этом важно никогда не путать понятия «мультифолликулярный» с «поликистозным». Яичники имеют мультифолликулярную структуру — так их создала природа. Нельзя ставить диагноз СПКЯ при обнаружении мультифолликулярности яичников, ибо это их нормальное состояние. Отсутствие овуляции не означает автоматически диагноз СПКЯ! В жизни каждой женщины бывают периоды, когда созревание половых клеток может быть замедлено или приостановлено в силу ряда причин, но не из-за заболевания яичников. Около 300 заболеваний, известных медицине, могут сопровождаться нарушением овуляции.
Во-вторых, разногласия в постановке СПКЯ наблюдаются вот уже почти двадцать лет между европейской и американской медициной. Правда, они чаще объясняются конкуренцией личностей и организаций, стремящихся к первенству и доминированию в принятии общих стандартов диагностики и лечения.
В странах Европы диагноз СПКЯ ставится только по УЗИ-исследованию без лабораторного обследования, с учетом всего лишь одного клинического признака — нарушения менструального цикла. Американские рекомендации, наоборот, не признают признаки СПКЯ, видимые при УЗИ-исследовании как диагностические критерии. Такое несоответствие в постановке диагноза приводит к большому количеству ложно-положительных и ложно-отрицательных диагнозов.
Старая школа врачей пользуется Роттердамскими критериями постановки диагноза СПКЯ (2003 г.) — у пациентки должно быть минимум два признака заболевания из следующих: гиперандрогения (повышенный уровень мужских половых гормонов), хроническая ановуляция, поликистозное строение яичников на УЗИ (минимум 12 фолликулов размерами 2–9 мм) и увеличенный размер яичников (минимум на 10 мм).
Но все большее количество врачей придерживается критериев, предложенных Androgen Excess Society и PCOS Society в 2009 году, которые включают два обязательных признака — гирсутизм и гиперандрогению, подтверждённые лабораторно, и один из двух дополнительных признаков — олигоановуляцию или поликистозную морфологию яичников. Исследование, сравнившее разные классификации диагностических критериев постановки СПКЯ, показало, что это один из лучших подходов — он учитывает до 80% случаев этого заболевания. Другие классификации страдают недооценкой или переоценкой данного состояния и не учитывают другие заболевания, при которых есть похожие симптомы и лабораторные показатели.
Синдром поликистозных яичников может проявляться следующими признаками:
- нарушение менструального цикла (цикл меньше 21 дня или больше 35 дней, меньше 9 циклов в год);
- отсутствие созревания яйцеклеток (ановуляция);
- повышенная волосатость (гирсутизм);
- акне;
- повышенное количество мужских половых гормонов (гиперандрогения);
- повышенный уровень лютеинизирующего гормона (ЛГ);
- повышенный уровень жиров (гиперлипидемия);
- повышенный уровень инсулина (гиперинсулинемия);
- ожирение (до 75% случаев, умеренное — в 50% случаев), чаще всего по андроидному типу, когда основная масса жировой ткани размещена центрально (живот, бедра).
Часто к врачу обращаются женщины по поводу бесплодия из-за нарушения овуляции и проблем с зачатием.
Существуют три категории женщин, которым СПКЯ ставится ошибочно. В первую категорию входят подростки и молодые женщины (до 21–22 лет), проходящие последнюю стадию полового созревания и формирования механизма регуляции менструального цикла на гипоталамо-гипофизарном уровне. Нерегулярность менструального цикла, незначительное повышение уровня мужских половых гормонов и поликистозное строение яичников в этой возрастной группе являются частым явлением и в большинстве случаев физиологической нормой. Нередко в этот период появляются первые признаки конституционального гирсутизма, на что молодые девушки реагируют негативно. Также не учитывается тот факт, что многие женщины имеют слишком низкий вес из-за недоедания, голодания, диет, интенсивных занятий физическими упражнениями. Именно в этой категории женщин врачебная ошибка доминирует в постановке диагноза СПКЯ.
Вторая категория женщин — планирующие беременность. Некоторые из них проходят обследование как часть подготовки к беременности. Так как женщины чаще всего не знают, какой цикл считается регулярным, жалобы о задержке месячных до 7 дней воспринимаются и женщинами, и врачами как признак СПКЯ. Треть женщин, прекративших прием гормональных препаратов, может иметь нарушение менструальных циклов в течение 3–6 месяцев, что ошибочно может быть принято за СПКЯ.
Третья категория женщин — это женщины, страдающие бесплодием. Часто они также жалуются на редкие менструальные циклы. Ошибка врачей заключается в том, что обследуется обычно только женщина, а обследование мужчины не проводится. Мужской фактор бесплодия при таком подходе не учитывается. Не учитывается стрессовый, возрастной и многие другие факторы. Не измеряются вес и рост женщины, как и не определяется индекс массы тела.
Хотя СПКЯ является эндокринопатией, важно не загружать женщину многочисленными тестами, а определить следующие показатели:
- уровень ЛГ;
- уровень инсулина в сыворотке крови;
- глюкозо-толерантный тест;
- уровень жиров в сыворотке крови (глицериды, холестерол);
- уровень мужских половых гормонов (свободный и общий тестостерон);
- уровень 17-гидроксипрогестерона;
- уровень ТСГ и тироксина;
- уровень пролактина;
- тест на беременность;
- уровень DHEA-S;
- суточное количество свободного кортизола в моче.
Ни лапароскопия, ни МРТ, ни компьютерная томография не должны применяться в постановке диагноза СПКЯ, если параллельно нет подозрения на опухоли яичников, надпочечников и матки.
Врачам также необходимо помнить о некоторых особенностях результатов обследования при постановке диагноза.
- Соотношение уровней ЛГ к ФСГ не является критерием для постановки диагноза СПКЯ. Прием гормональных контрацептивов значительно влияет на соотношение ФСГ и ЛГ, поэтому обследование должно проводиться не ранее чем через 3 месяца после прекращения приема гормональных контрацептивов.
- Уровень тестостерона может быть в пределах нормы в ряде случаев СПКЯ. Ряд гормональных контрацептивов понижают уровень тестостерона в сыворотке крови, поэтому обследование должно проводиться через 3 месяца после окончания приема гормональных контрацептивов.
- У женщин с СПКЯ тестостерон повышен незначительно. При более высоких показателях (больше 7 нмоль/л) необходимо исключить опухоль яичников или надпочечников.
- Уровень DHEA-S у женщин с СПКЯ обычно в норме или незначительно повышен. При показателях >21,7 μмоль/л необходимо исключить опухоль надпочечников.
- У женщин, принимающих гормональные контрацептивы, определение уровня кортизола в сыворотке крови не должно проводиться, так как контрацептивы повышают уровень кортизол-связывающего глобулина, что повышает уровень кортизола тоже.
- Уровень суточного свободного кортизола в моче у женщин с СПКЯ обычно в пределах нормы, но в ряде случаев может быть повышен. Если он более чем в 2 раза превышает верхний уровень нормы, необходимо исключить синдром Кушинга. При незначительном повышение кортизола мочи рекомендуется провести ряд тестов (с дексаметазоном, кортикотропин-рилизинг гормоном) для исключения других диагнозов.
- Пролактинемия наблюдается у 5–30% женщин с СПКЯ. Обычно уровни пролактина повышены не более чем на 50% верхней границы нормального уровня (30 нг/мл).
- 17-гидроксипрогестерон (17-ОПГ) необходимо сдавать натощак ранним утром в первую фазу цикла. Уровень < 6 нмоль/л обычно исключает заболевание надпочечников — недостаточность 21-гидрокислазы. Если уровень 17-ОПГ повышен, проводится АКТГ-стимулирующий тест. Применение гормональных контрацептивов и глюкокортикоидов влияет на уровень 17-ОПГ.
Врожденная гиперплазия надпочечников, нарушение функции щитовидной железы, пролактинома, синдром Кушинга, опухоль яичников, вырабатывающая андрогены, — эти пять основных заболеваний должны быть в списке предполагаемых диагнозов при обследовании женщины с признаками синдрома поликистозных яичников, так как они могут сопровождаться нарушениями менструального цикла и гирсутизмом. Помимо этих заболеваний необходимо исключить опухоли надпочечников и беременность.
(Об особенностях лечения СПКЯ читайте здесь.)
Страница Е. П. Березовской в КлубКоме
опубликовано 07/12/2016 19:06обновлено 17/12/2016
— Анализы и обследования, Болезни, врачи, лечение и лекарства, Женское здоровье
lib.komarovskiy.net