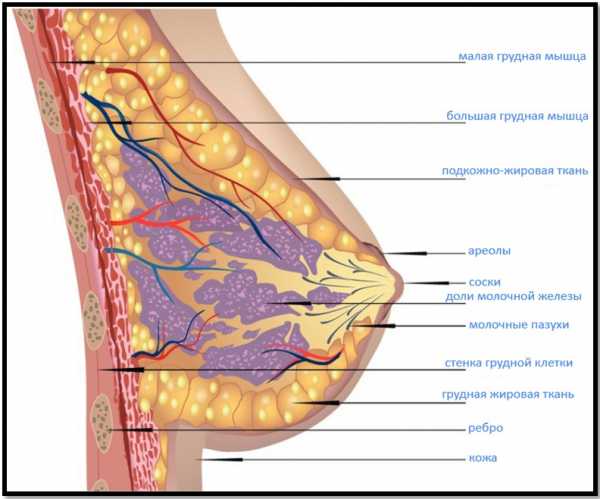
Зно молочной железы
Злокачественные новообразования молочной железы. Страница 1 - Онкология . Каталог статей. Медицинский ресурс Николаева
В России, к ак в прочем, и в большинстве развитых стран, неуклонно растет заболеваемость ЗНО молочной железы. В самой структуре общей онкологической заболеваемости ЗНО молочной железы имеет удельный вес - 15% от всех онкологических заболеваний. Среди женского взрослого населения это самая часто диагностируемая злокачественная патология. Заболеваемость возрастает с увеличением возраста и становится наиболее высокой в возрасте 60 - 65 лет.Ведущее значение в возникновении ЗНО молочной железы имеет воздействие эстрогенов. Генетически предопределенный рак составляет 9% всех случаев. К основным факторам риска заболевания следует прежде всего отнести:
- раннее начало месячных (младше 12 лет);
- поздние первые роды (старше 30 лет) или же их отсутствие;
- позднее наступление менопаузального периода (старше 55 лет);
- возраст женщины, превышающий 50 лет;
- доброкачественные опухолевые заболевания молочной железы;
- наличие ЗНО молочной железы у ближайших родственников;
- мутации генов ИКСФ-1б, ИКСФ-2б, ИКСФ-3;
- ранее пролеченное ЗНО молочной железы
Ультразвуковое исследование является современным неинвазивным методом осуществления дифференциальной диагностики различных образований молочной железы. Для оценки распространенности процесса и исключения метастатического поражения применяют такие вспомогательные методы диагностики как КТ и МРТ. О том, в чем заключается отличие КТ от МРТ и каковы показания к использованию этих диагностических методов читайте в отдельной статье на сайте kt-diagnostika.ru. Для выявления субклинического отдаленного метастазирования по показаниям выполняют радиоизотопное сканирование костей.
При наличии патологического отделяемого из соска выполняют его цитологическое исследование. Для получения материала используют тонкоигольчатую аспирационную биопсию образования.Все пациенты с подозрением на ЗНО должны быть консультированы онкологом (маммологом). При диагностированном ЗНО молочной железы необходимо как можно быстрее определиться с тактикой дальнейшего лечения с привлечением хирурга - маммолога, радиолога и врач - химиотерапевта. После направления пациентки на консультацию или лечение к специалистам необходимо проконтролировать, обратилась ли она за лечением и выполняет ли рекомендации.Наиболее распространенным методом лечения ЗНО молочной железы является хирургический. Большинству больных начальными стадиями заболевания (I—II стадии) показаны органосохраняющие операции (лобпэктомия, широкое иссечение опухоли, секторальная резекция, квадрантэктомия). По современным данным эффективность квадрантэктомии, выполненой на начальных стадиях заболевания, не уступает эффективности выполненной радикальной мастэктомии. Обязательным этапом операции является подмышечная лимфаденэктомия или, как минимум, интраоперационная биопсия ткани подмышечных лимфатических узлов. После органосохраняющих операций пациентам назначают курсы гаммалучевой терапию на оставшуюся часть железы. При выполнении мастэктомии возможно проведение одномоментных реконструктивных операций.При обнаружении во время гистологического исследования в опухолевой ткани эстрогенных рецепторов показана гормонотерапия. В пременопаузе обычно выключают функцию яичников (оперативным, гормональным путем или радиационным воздействием), а затем назначают антиэстрогенный препарат тамоксифен. Последний также назначают в постменопаузе для длительного применения (в среднем, 5 лет). При опухолевом поражении регионарных путей лимфооттока, а так же при наличии удаленных метастазов обязательна химиотерапия. Лучевую терапию проводят перед операцией при- противопоказаниях к химиотерапии,
- для снижения вероятности развития рецидива роста первичного очага после выполнения органосохраняющей операции,
- после проведения мастэктоми,
- при опухолевом поражении 4 или более лимфоузлов,
- при наличии удаленных метастазов
- при местных формах рака (с профилактической целью).
Продолжение читайте на этой странице.
Автор - Лебедев А.К.
medresurs.in
Злокачественные новообразования молочной железы. Страница 3 - Онкология . Каталог статей. Медицинский ресурс Николаева
Около 2% взрослых женщин во всем мире имеют неблагоприятный семейный анамнез. При неотягощенной наследственности вероятность развития мутации генов ВКСА-1 и ВКСА-2 весьма низка. Расчеты позволяют предсказать риск клинически значимых ВКСА мутаций (ВКСА мутации обусловливают развитие ЗНО молочной железы, ЗНО яичника или обоих нозологий одновременно), но эти расчеты не позволяют верифицировать их в общей популяции. Нет никаких эмпирических правил, определяющих риск ВКСА мутаций, которые давали бы повод для направления пациента на генетическую консультацию.Вместе с тем, не у всех женщин, имеющих ВКСА мутации, разовьется ЗНО молочной железы или ЗНО яичника. У женщин, имеющих клинически значимые ВКСА мутации вероятность возникновения ЗНО молочной железы или ЗНО яичника к 70 годам, оценивается в диапазоне 35 - 84 % для ЗНО молочной железы и 10 - 50 % — для ЗНО яичника.Генетическое консультирование помогает женщинам принять осознанное решение, может расширить их знания и понимание абсолютного риска для ЗНО молочной железы и ЗНО яичника, а зачастую снизить уровень тревоги. Генетическое консультирование включает элементы консультирования, оценку риска, анализ родословной и, в некоторых случаях, рекомендации по тестированию на наличие мутаций генов ВКСА. Консультирование проводит специально обученный медицинский персонал.Генетическое исследование может рекомендовать семейный врач. Когда это делается при согласовании с генетической консультацией, тест позволяет связать результаты исследования с адекватной лечебной тактикой. Генетическое консультирование может привести к нежелательным этическим, юридическим и социальным последствиям, таким как проблемы с медицинским страхованием или дискриминация при устройстве на работу.Среди женщин с ВКСА 1 и ВКСА 2 мутациями, профилактическая мастэктомия и оофорэктомия снижает частоту возникновения ЗНО молочной железы или яичника, однако имеются неоднозначные научные доказательства в плане снижения смертности. Химиопрофилактика селективными модуляторами эстрогеновых рецепторов может снизить частоту возникновения эстроген-чувствительных раков, однако их применение сопровождается побочными эффектами (эмболия легочной артерии, тромбоз глубоких вен, рак эндометрия). Большинство раков, обусловленных ВКСА 1 мутациями не чувствительны к эстрогенам и соответственно они не предотвращаются приемом тамоксифена.Таким образом, учет факторов риска, своевременная диагностика, адекватное лечение и полноценная реабилитация пациентов с ЗНО молочной железы способны достоверно увеличить продолжительность жизни.Автор - Лебедев А.К.
Page 2
В России, к ак в прочем, и в большинстве развитых стран, неуклонно растет заболеваемость ЗНО молочной железы. В самой структуре общей онкологической заболеваемости ЗНО молочной железы имеет удельный вес - 15% от всех онкологических заболеваний. Среди женского взрослого населения это самая часто диагностируемая злокачественная патология. Заболеваемость возрастает с увеличением возраста и становится наиболее высокой в возрасте 60 - 65 лет.Ведущее значение в возникновении ЗНО молочной железы имеет воздействие эстрогенов. Генетически предопределенный рак составляет 9% всех случаев. К основным факторам риска заболевания следует прежде всего отнести:
- раннее начало месячных (младше 12 лет);
- поздние первые роды (старше 30 лет) или же их отсутствие;
- позднее наступление менопаузального периода (старше 55 лет);
- возраст женщины, превышающий 50 лет;
- доброкачественные опухолевые заболевания молочной железы;
- наличие ЗНО молочной железы у ближайших родственников;
- мутации генов ИКСФ-1б, ИКСФ-2б, ИКСФ-3;
- ранее пролеченное ЗНО молочной железы
Ультразвуковое исследование является современным неинвазивным методом осуществления дифференциальной диагностики различных образований молочной железы. Для оценки распространенности процесса и исключения метастатического поражения применяют такие вспомогательные методы диагностики как КТ и МРТ. О том, в чем заключается отличие КТ от МРТ и каковы показания к использованию этих диагностических методов читайте в отдельной статье на сайте kt-diagnostika.ru. Для выявления субклинического отдаленного метастазирования по показаниям выполняют радиоизотопное сканирование костей.
При наличии патологического отделяемого из соска выполняют его цитологическое исследование. Для получения материала используют тонкоигольчатую аспирационную биопсию образования.Все пациенты с подозрением на ЗНО должны быть консультированы онкологом (маммологом). При диагностированном ЗНО молочной железы необходимо как можно быстрее определиться с тактикой дальнейшего лечения с привлечением хирурга - маммолога, радиолога и врач - химиотерапевта. После направления пациентки на консультацию или лечение к специалистам необходимо проконтролировать, обратилась ли она за лечением и выполняет ли рекомендации.Наиболее распространенным методом лечения ЗНО молочной железы является хирургический. Большинству больных начальными стадиями заболевания (I—II стадии) показаны органосохраняющие операции (лобпэктомия, широкое иссечение опухоли, секторальная резекция, квадрантэктомия). По современным данным эффективность квадрантэктомии, выполненой на начальных стадиях заболевания, не уступает эффективности выполненной радикальной мастэктомии. Обязательным этапом операции является подмышечная лимфаденэктомия или, как минимум, интраоперационная биопсия ткани подмышечных лимфатических узлов. После органосохраняющих операций пациентам назначают курсы гаммалучевой терапию на оставшуюся часть железы. При выполнении мастэктомии возможно проведение одномоментных реконструктивных операций.При обнаружении во время гистологического исследования в опухолевой ткани эстрогенных рецепторов показана гормонотерапия. В пременопаузе обычно выключают функцию яичников (оперативным, гормональным путем или радиационным воздействием), а затем назначают антиэстрогенный препарат тамоксифен. Последний также назначают в постменопаузе для длительного применения (в среднем, 5 лет). При опухолевом поражении регионарных путей лимфооттока, а так же при наличии удаленных метастазов обязательна химиотерапия. Лучевую терапию проводят перед операцией при- противопоказаниях к химиотерапии,
- для снижения вероятности развития рецидива роста первичного очага после выполнения органосохраняющей операции,
- после проведения мастэктоми,
- при опухолевом поражении 4 или более лимфоузлов,
- при наличии удаленных метастазов
- при местных формах рака (с профилактической целью).
Продолжение читайте на этой странице.
Автор - Лебедев А.К.
medresurs.in
С00-С97 Злокачественные новообразования (ЗНО)
Классификация TNM (международный противораковый союз)
Т - первичная опухоль, N - регионарные лимфоузлы, M - отдаленные метастазы.
~~~ Рак желудка * Cancer ventriculi ~~~
Клинические симптомы появляются, как правило, слишком поздно. Дисфагия. Диспепсия в сочетании с похуданием, анемией или потерей аппетита. Чувство переполнения желудка, дискомфорт в области эпигастрия, отрыжка, отрыжка тухлым, рвота застоявшейся пищей. Боли - при прорастании опухоли в поджелудочную железу. Желтуха - при распространении процесса на желчные пути. Кровавая рвота, мелена - кровотечение из распадающейся опухоли.
Плотные увеличенные надключичные лимфатические узлы (чаще слева). Метастазы в печень, брюшину (плотный метастатический узел в области пупка), яичники, двугласово пространство.
Лечение. Неоадъювантная (дооперационная) химиотерапия, лучевая терапия. Радикальная резекция желудка. Адъювантная (послеоперационная) химиотерапия. Паллиативное лечение при запущенном (нерезектабельном) раке: паллиативная резекция желудка, наложение анастомоза, стомы, установка эндопротеза при дисфагии, химиолучевая терапия.
~~~ Колоректальный рак * Cancer colorectalis ~~~
Опухоль обычно возникает в местах изгибов толстой кишки, в зоне задержки каловых масс (слепой, печеночный, селезеночный, сигмовидный отделы).
Рак восходящего отдела. Характерна общая симптоматика (преобладание симптомов слабости, быстрой утомляемости, абдоминальный дискомфорт, неопределенные боли в животе, лихорадочные состояния, прогрессирующая железодефицитная анемия).
Поражение левых отделов толстой кишки. Преобладают локальные симптомы (чередование запоров и поносов, приступообразные боли, патологические примеси в кале, задержка газов, ложные позывы на дефекацию).
Острая кишечная непроходимость характерная для рака сигмовидной кишки и селезеночного изгиба.
Рак прямой кишки. Проявляется поздно. Чувство неполного опорожнения кишечника, примесь крови и слизи в кале, вздутие живота, чередование поноса с запором. Постоянные боли указывают на значительное распространение опухоли на крестец и нервные сплетения. Дизурия, блокада мочеточников.
Отдаленные метастазы в печень.
У 6% радикально излеченных больных развиваются метахронные опухоли ЖКТ.
Лечение. Правосторонняя или левосторонняя гемиколэктомия, резекция или экстирпация прямой кишки, наложение колостомы (anus praeternaturalis). Химиолучевая терапия. Паллиативное лечение.
~~~ Рак легкого * Cancer pulmonis~~~
Метастазирование: средостение, крупные сосуды грудной стенки, перикард, лимфатические узлы ворот легких, средостения, надключичные и подмышечные л/узлы; головной мозг, кости, печень, надпочечники. Мелкоклеточный рак на очень ранних стадиях заболевания метастазирует как в грудные, так и во внегрудные области (основной метод лечения - химиотерапия).
Симптомы
Общие: слабость, утомляемость, похудание, отсутствие аппетита, потеря интереса к окружающему.
Окклюзия главного бронха или трахеи: одышка в сочетании со стридором.
Помощь: глюкокортикоиды, эуфиллин, сальбутамол, атропин, кислород; при отсутствии специфической причины, поддающейся лечению применяют морфин, диазепам, комбинацию небольшой дозы хлорпромазина с атропином; при кашле - противокашлевые средства, содержащие кодеин; паллиативная лучевая терапия.
Обтурационный пневмонит при эндобронхиальной опухоли: симптомы пневмонии - лихорадка, одышка, боль в груди, кашель, аускультативно ослабление дыхания.
Помощь: антибиотики в сочетании с симптоматической терапией. Гидроторакс: одышка, боли, наличие плеврального выпота.
Помощь: Распад опухоли легкого с инфильтрацией стенки крупного сосуда: кровохаркание или легочное кровотечение.
Помощь: транексамовая кислота в достаточно высоких дозах. Инфекционные поражения легких при распространенном раке легкого(обтурационный пневмонит, эмпиема плевры, кандидоз, аспергиллез): часто в терминальной стадии заболевания.
Помощь: фторхинолоны; плевральная пункция с установкой дренажа при гнойном плеврите. Сепсис: анемия, одышка, прогрессирующая недостаточность кровообращения, аритмия, тахикардия, падение АД. Онкогенная лихорадка: на фоне антибиотикотерапии сохраняется высокая температура тела. Помощь: регулярный прием НПВП.
Поражение возвратного нерва в средостении: охриплость голоса, афония.
Синдром полой вены (обструкция сосуда опухолью средостения): расширение вен грудной клетки, цианоз, отечность лица с повышением ВЧД .
Прорастание опухоли в грудную стенку и средостение: дисфагия, вторичные боли в груди.
Поражение ЦНС: эпилептиформные судороги, головная боль, гемиплегия, признаки карциноматоза мозговых оболочек.
Метастазы в кости и печень: боли в костях, увеличение размеров печени с болями в правой подрёберной области.
Действие гормонов и гормоноподобных веществ, выделяемых опухолью: синдром Кушинга, гиперкальциемия, остеоартропатии, гинекомастия, мышечная слабость, гипокалиемия, гипонатриемия.
Поражение плечевого сплетения и симпатических ганглиев, поражение позвонков: боли и слабость в руке, ее отек, синдром Горнера - птоз, миоз, энофтальм, ангидроз; боли в позвоночнике.
Лечение. Лобэктомия или пневмонэктомия. Химиотерапия, лучевое лечение. Паллиативное лечение.
~~~ Рак молочной железы * Cancer mammae ~~~
Боль в молочной железе у 5-20% больных. Наличие асимметрии молочных желез, деформации контура, отека или гиперемии кожи молочной железы, деформации ареолы, изменения положения соска. При пальпации - плотная с нечеткими контурами, ограниченно подвижная опухоль. Может быть втяжение, отек, утолщение кожи. При надавливании на область ореолы могут быть кровянистые или обильные прозрачные выделения. Увеличение регионарных (подмышечных) лимфоузлов.
Результаты маммографии, аспирационной биопсии или трепан-биопсии.
Лечение. Мастэктомия. Лампэктомия, сегментарная (секторальная) резекция, квадрантэктомия. Подмышечная лимфоденэктомия. Лучевая терапия. Химиотерапия. Гормональная терапия. Выключение функции яичников (овариоэктомия, облучение яичников).
см. Паранеопластический синдром
см. Синдром распада опухоли
ПОМОЩЬ НА ДГЭ
При рвоте:
МЕТОКЛОПРАМИД (Церукал) 2 мл (10 мг) в/м.
При желудочно-кишечном кровотечении:
Смотри раздел «Хирургия».
При кишечной непроходимости:
Смотри раздел «Хирургия».
При острой задержке мочи:
Смотри раздел «Урология».
Тактика
Актив в ЛПУ или Хоспис.
У детей при подозрении на ЗНО и/или выявлении впервые:
Госпитализация, при отказе - актив в ЛПУ.
Алгоритм оказания помощи онкологическим больным при болевом синдроме
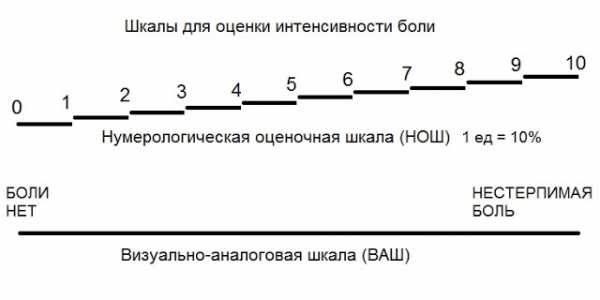
Боль по ВАШ или НОШ 0%
Жалоб нет. Введение обезболивающих препаратов не требуется.
I ступень. Боль по ВАШ или НОШ до 40%
Больной спокойно сообщает о своей боли, которая хорошо купируется на 4-6 часов парацетамолом, анальгином или средними дозами НПВС, ночной сон не нарушен из-за боли.
Метамизол натрия (Анальгин) 1000 мг в/в или
Кеторолак 30 мг в/м или
Трамадол 100 мг в/м или в/в (можно дополнительно дать Парацетамол 500-1000 мг внутрь).
II ступень. Боль по ВАШ или НОШ 40-70%
Парацетамол, анальгин или средние дозы НПВС малоэффективны (не более 1-3 часов), ночной сон нарушен приступами боли.
Трамадол 100 мг в/м или в/в (при необходимости в сочетании с 500-1000 мг парацетамола внутрь)
III ступень. Боль по ВАШ или НОШ 70%-100%
Трамадол в комбинации с парацетамолом или анальгином или НПВС – малоэффективен, боль вызывает страдание у пациента при воспоминании о ней, нарушает его ночной сон.
Больной на момент осмотра мечется, стонет, страдает от сильнейшей боли, принимает вынужденное положение.
Морфин 5-10 мг в/в или в/м.
neotloga-ru.blogspot.ru
Рак молочной железы
Цели лечения: - удаление опухоли; - комплексное воздействие на опухоль, для улучшения условий проведения хирургического этапа;- профилактика отдаленного метастазирования.
Общие принципы лечения РМЖ
Немедикаментозное лечение
РМЖ – одно из немногих онкологических заболеваний, при котором лечение всех стадий многовариантно.
Несмотря на значительный прогресс в разработке новых методов лечения РМЖ, хирургическое вмешательство по-прежнему остается основным, а в ряде случаев – единственным методом лечения этого заболевания (Са insitu).
Выбор того или иного вида радикальной операции определяется не только степенью распространения опухолевого процесса, но и клинической формой, локализацией опухоли, возрастом больных и некоторыми другими факторами, характеризующими их общее состояние.
В последнее время все большее значение придается вопросам улучшения качества жизни, которое достигается выполнением органосохраняющих операций на молочной железе, а также реконструктивно-восстановительных операций с использованием местных тканей.
Органосохраняющие операции при РМЖ обеспечивают, наряду с высокими показателями выживаемости, хорошие косметические и функциональные результаты. Социально-трудовая реабилитация больных после радикальной резекции молочной железы происходит быстрее, чем после мастэктомии.
Показания к выполнению органосохраняющих операций на молочной железе:
- наличие узловой формы рака размером до 2,5 см;
- отсутствие мультицентричности и мультифокальности опухолевого роста (на маммограммах, УЗИ клинически);
- медленный и умеренный темп роста, удвоение размера опухоли не быстрее чем за 3 месяца (по данным анамнеза);
- благоприятное соотношение размеров молочной железы и опухоли для получения хорошего косметического результата операции;
- отсутствие отдаленных метастазов;
- допустимо наличие одиночных метастазов в подмышечной области;
- желание больной сохранить молочную железу.
Реконструктивно-восстановительные операции могут выполняться при I-III стадиях РМЖ по желанию пациентки при любой локализации опухоли.
Женщина должна быть ознакомлена со всеми видами хирургических вмешательств.
Адъювантная терапия рака молочной железы
Рекомендации по адъювантной системной терапии подтипов рака молочной железы (Сент-Галлен, 2011)| Подтип РМЖ | Тип терапии | Комментарии |
| Люминальный А | Только гормональная терапия | Только отдельным пациентам может потребоваться цитотоксическая терапия (например при обширном поражении лимфатических узлов или с другими показателями высокого риска) |
| Люминальный В (Her-негативный с высоким индексом ki67) | Гормональная + цитотоксическая терапия | Решение о проведении и типе цитотоксической терапии может приниматься в зависимости от уровня экспрессии эндокринных рецепторов, риска и предпочтений пациента |
| Люминальный В (Her-позитивный) | Цитотоксическая + таргетная+ гормональная терапия | Данных в поддержку отказа от цитотоксической терапии в данной группе не существует |
| Трижды негативный | Цитотоксическая терапия |
NB! - при медулярном раке и аденокистозной карциноме адъювантная химиотерапия может не потребоваться (при отсутствии поражения лимфатических узлов)
Схемы адъювантной химиотерапии РМЖ: FАС, АС, ТАС, CMF, доцетаксел + трастузумаб; паклитоксел + трастузумаб. Применение герцептина в сочетании с препаратами антрациклинового ряда невозможно, поскольку оба препарата обладают кардиотоксическим действием.
C 2011 г., StGallen, рекомендовано применение трастузумаба (герцептин), в адъювантной терапии РМЖ при высокой экспрессии Her2/neu и размере образования от 1 см.
Лечение по стадиям
Хирургическое лечение производится в объеме радикальных мастэктомий по Madden, Patey, а также в объеме органосохраняющих операций с подключично-подмышечно-подлопаточной лимфаденэктомией, реконструктивно-восстановительной операцией или без нее.
0, I стадия
1. Органосохраняющее лечение. После органосохраняющей операции, с учетом уровня экспрессии ЭР, ПР, Her-2/neu, назначается один из видов системного лечения. Лишь только при отсутствии необходимости проведения системного лечения возможно назначение лучевой терапии. Облучение молочной железы осуществляется с помощью фотонного излучения (6 МэВ), линейного ускорителя или гамма-излучения 60Со-установки (1,25 МэВ) с двух тангенциально расположенных полей, имеющих целью обеспечить максимально гомогенное облучение железы. РОД 2 Гр, СОД 60 Гр. Послеоперационная зона дополнительно облучается в дозе 12 Гр (по 2 Гр). Предпочтительно облучение электронным пуском.
2. Радикальная мастэктомия. При всех вышеперечисленных локализациях I стадии заболевания возможно выполнение радикальной мастэктомии с восстановлением формы железы или без восстановления (по желанию пациентки).
Системное лечение предусматривает: химиотерапию у больных до 50 лет при инвазивных формах, гормонотерапию антиэстрогенами (тамоксифен, торемифен) или ингибиторами ароматазы у постменопаузальных больных с рецептор-положительными опухолями в течение 5 лет.Больным младше 50 лет с сохраненной менструальной функцией:
- двухсторонняя овариэктомия;
- LHRH-аналоги (диферелин, золадекс) ежемесячно, в течение 2 лет.
В дальнейшем – назначение антиэстрогена (тамоксифен, торемифен).
Больным с отрицательными ЕР, ПР с неблагоприятными прогностическими факторами, с положительным Her 2-neu, гормонотерапия не проводится, рекомендована химиотерапия или химиотаргетная терапия.Схемы химиотерапии при 0 и I стадиях:
1. АС:
- доксорубицин 60 мг/м*2 в/в, 1 дн.;
- циклофосфан 600 мг/м*2 в/в, 1 дн.
Повторять каждые 3-4 недели в зависимости от восстановления гематологических показателей.
2. FАС:
- фторурацил 500 мг/м2 в/в, в 1-й и 8-й дни;
- доксорубицин 50мг/м2 в/в длительная инфузия 72 часа, с 1-го по 3-й дни;
- циклофосфамид 500мг/м2 в/в, 1-й день.
Повторять 21, если восстановлены гематологические показатели.
3. FEC:
- фторурацил 500 мг/м2 в/в, в 1-й день;
- эпирубицин 50-100 мг/м2 в/в, в 1-й день;
- циклофосфамид 500 мг/м2 в/в, в 1-й день;
Повторять через 3 недели.
4. ТАС:
- доцетаксел 75 мг/м2 в/в, 1-й день;
- доксорубицин 50мг/м2 в/в, 1-й день;
- циклофосфамид 500 мг/м2 в/в, 1-й день.
Повторять каждый 21 день.
5. ТА:
- доцетаксел 75 мг/м2 в/в, 1-й день;
- доксорубицин 50 мг/м2 в/в, 1-й день.
Повторять каждый 21 день.
6. ТС:
- доцетаксел 75 мг/м2 в/в, 1-й день;
- циклофосфамид 500 мг/м2 в/в, 1-й день.
Повторять каждый 21 день.
7. САF:
- циклофосфамид 600 мг/м2 в/в, 1-й день;
- доксорубицин 60 мг/м2 в/в, 1-й день;
- фторурацил 600 мг/м2 в/в, 1-й день;
Повторять каждые 21-28 дней.
8. CMF:
- циклофосфан 100 мг/м*2 перорально, 1-14 дн.;
- метотрексат 40 мг/м*2 в/в, 1 и 8 дн.;
- 5ФУ 600 мг/м*2 в/в, 1 и 8 дн.;
- преднизолон 40 мг/м*2 перорально, 1и 14 дн.
Повторять каждые 4 недели, 6 циклов.
При гиперэкспрессии Her2/neu проводится таргетная терапия трастузумабом 8 мг/кг – нагрузочная доза, затем по 6 мг/кг 1 раз в 3 недели. Длительность таргетной терапии в адъювантном режиме – 1 год.II стадия
Лечение, идентичное таковому при I-ой стадии, однако у больных с N0, но с наличием неблагоприятных прогностических признаков (возраст до 35 лет, отрицательные гормональные рецепторы) в послеоперационном периоде, кроме всей молочной железы, при локализации опухоли во внутренних квадрантах или центральной зоне, а также у всех больных с N+ (при метастатическом поражении трех и менее подмышечных лимфатических узлов) дополнительно облучаются парастернальная и надключичная зоны со стороны основного очага.
Послеоперационная ЛТ проводится в режиме классического фракционирования дозы (РОД 2 Гр, СОД 30 Гр) после выполнения органосохраняющей операции и проведения системной терапии. Послеоперационная зона дополнительно облучается в дозе 12 Гр (по 2 Гр).
У больных с N+, при поражении четырех и более подмышечных лимфатических узлов и/или при прорастании опухолью капсулы лимфатического узла, кроме оставшейся молочной железы, облучается парастернальная, надподключично-подмышечная зона со стороны поражения.ВСЕ пациенты со II-ой стадией должны получать адъювантную системную химиотерапию (AC, ТАС, АС+Т, FAC, CАF, FЕC,CMF).
При +ER – гормонотерапия: антиэстрогены (тамоксифен или торемифен) в течение 5 лет, у женщин в постменопаузе в адъювантном режиме могут назначаться так же ингибиторы ароматазы – анастрозол, летрозол. При -ER – химиотерапия.
Схемы химиотерапии:
1. FАС:
- фторурацил 500 мг/м2 в/в, в 1-й и 8-й дни;
- доксорубицин 50 мг/м2 в/в длительная инфузия 72 часа, с 1-го по 3-й дни;
- циклофосфамид 500 мг/м2 в/в, 1-й день.
Повторять 21, если восстановлены гематологические показатели.
2. FEC:
- фторурацил 500 мг/м2 в/в, в 1-й день;
- эпирубицин 50-100 мг/м2 в/в, в 1-й день;
- циклофосфамид 500 мг/м2 в/в, в 1-й день.
Повторять через 3 недели.
3. VC:
- винорельбин - 25 мг/м2 в/в, в 1, 8, 15, 22-й дни;
- капицитабин - 1000 мг/м2 внутрь, 2 раза в сутки (2 г/м2/сут.) с 1-го по 14-й дни;
Интервал между курсами - 1 неделя.
4. ТАС:
- доцетаксел 75 мг/м2 в/в, 1-й день;
- доксорубицин 50 мг/м2 в/в, 1-й день;
- циклофосфамид 500 мг/м2 в/в, 1-й день.
Повторять каждый 21 день.
5. САF:
- циклофосфамид 600 мг/м2 в/в, 1-й день;
- доксорубицин 60 мг/м2 в/в, 1-й день;
- фторурацил 600 мг/м2 в/в, 1-й день.
Повторять каждые 21-28 дней.
6. АС:
- доксорубицин 60 мг/м2 в/в, 1-й день;
- циклофосфамид 600 мг/м2 в/в, 1-й день;
Повторять каждые 3-4 недели в зависимости от восстановления гематологических показателей.
7. АСТ:
- доксорубицин 60 мг/м2 в/в, 1-й день;
- циклофосфамид 600 мг/м2 в/в, 1-й день х 4 цикла;
- затем паклитаксел 175 мг/м2 в/в, 3-х часовая инфузия, 1 раз в 3 недели х 4 цикла.
8. CMF:
- циклофосфамид 100 мг/м2 перорально, с 1-го по 14-й дни;
- метотрексат 40 мг/м2 в/в, в 1-й и 8-й дни;
- фторурацил 600 мг/м2 в/в, в 1-й и 8-й дни.
Повторять каждые 28 дней.
Или:
- циклофосфамид 600 мг/м2 в/в, 1-й день;
- метотрексат 40 мг/м2 в/в, в 1-й и 8-й дни;
- фторурацил 600 мг/м2 в/в, в 1-й и 8-й дни;
Повторять каждые 21-28 дней. Каждые 3 недели повторять 8 циклов.
При гиперэкспрессии Her2/neu проводится таргетная терапия трастузумабом 8 мг/кг – нагрузочная доза, затем по 6 мг/кг каждые 3 недели, в течение 1 года.
При IIА стадии общие воздействия назначают в соответствии с табл. 2
Таблица 2. Отсутствие метастазов в подмышечных лимфатических узлах| Менструальный статус | Низкий риск | Высокий риск |
| Гормоночувствительные опухоли | ||
| Менструирующие | Тамоксифен Торемифен Гозерилин Трипторелин | Химиотерапия Химиотерапия + антиэстроген (тамоксифен или торемифен) (при выключении функции яичников) |
| Постменопауза | Антиэстрогены (тамоксифен, торемифен) Ингибиторы ароматазы (аримидекс, летрозол) | Гормонотерапия: антиэстрогены (тамоксифен, торемифен); ингибиторы ароматазы (анастрозолс, летрозол) или химиотерапия + антиэстрогены (тамоксифен, торемифен); ингибиторы ароматазы (анастрозолс, летрозол) |
| Гормонорезистентные опухоли | ||
| Менструирующие | - | Химиотерапия |
| Постменопауза | - | Химиотерапия |
IIIа и IIIb, IIIc (при N3a, N3b) стадии
Необходим мультимодальный подход.
Оперативное вмешательство через 3 недели после окончания лечения в объеме РМЭ по Мадену, радикальной резекции молочной железы, органосохраняющей или реконструктивно-пластической операции.
Оперативное лечение. Оперативное пособие выполняется по общепринятой методике в объеме радикальной мастэктомии (по Madden, Patey). Объем хирургического вмешательства (вариант мастэктомии) определяется распространенностью опухолевого процесса. Во всех случаях показано удаление регионарных лимфатических узлов трех уровней: подмышечных, подключичных, подлопаточных с их последующей маркировкой. Опухоль подлежит маркировке в соответствии с размерами и локализацией по квадрантам молочной железы.
Возможно одномоментное или отсроченное выполнение реконструктивно-восстановительной операции (по желанию пациентки).
Послеоперационная лучевая терапия. Послеоперационная ЛТ проводится в режиме классического фракционирования дозы (РОД 2 Гр, СОД до эквивалентной дозы 40 Гр). Поля облучения: надподключичное, подмышечное, парастернальное, грудная стенка (при рТ3, 4).
Неоадъювантная терапия РМЖ
Клинически часто приходится встречаться со сложнейшим выбором лечения больных местнораспространенным РМЖ. Удельный вес таких опухолей колеблется от 5% до 40%. Обоснованиями для назначения неоадъювантной системной терапии МРРМЖ являются:1. Высокая вероятность скрытого (микрометастатического) распространения.
2. Возможность сократить объем хирургического вмешательства в пределах «чистых» хирургических краев.
3. Возможность оценить клинический ответ на терапию in vivo.
4. Доступность точной патоморфологической оценки степени регрессии опухоли.
5. Возможность специальных исследований биопсийного опухолевого материала до, во время и после завершения первичного системного лечения.
Целями данного вида системного лечения являются: 1. Добиться регресса опухоли и провести радикальное местно-регионарное лечение.2. С учетом крайне неблагоприятного прогноза у этой группы пациентов с помощью системной терапии добиться улучшения отдаленных результатов лечения.
Схема проведения неоадъювантного системного лечения: маммография, УЗИ, трепан-биопсия с определением уровня ЭР, ПР, Her 2/neu, ki67.4 курса неоадъювантной химиотерапии – операция – 4 курса адъювантной химиотерапии. При отсутствии эффекта после 4 курсов неоадъювантной химиотерапии необходимо сменить схему химиотерапии. При гиперэкспрессии Her2/neu в неоадъювантном режиме проводится таргетная терапия трастузумабом 8 мг/кг – нагрузочная доза в последующем по 6 мг/кг каждые 3 недели. После которой следует адъювантное назначение трастузумаба 8 мг/кг – нагрузочная доза в последующем по 6 мг/кг каждые 3 недели.
Метастатический РМЖ
Лечебная полихимиотерапия
Общие принципы лечения при обязательном определении рецепторного статуса: РП, РЭ, Her-2, ki67. При положительных гормональных рецепторах – люминальном А типе РМЖ, первым этапом проводят гормонотерапию антиэстрогенами (тамоксифен, торемифен) или ингибиторами ароматазы (анастрозол, летрозол) у больных в постменопаузе. При этом эффект химиотерапии должен оцениваться не ранее, чем через 3 месяца после начала лечения. При прогрессировании заболевания на фоне 1-й линии гормонотерапии, больную переводят на 2, затем 3-ю линии химиотерапии.
Химиотерапия МРМЖ назначается пациенткам с орицательными РЭ и РП, а также у больных с высоким уровнем ki67>15% и Her(3+). В качестве химиотерапии 1-ой линии используют антрациклин содержащие схемы: АС, FAC, FEC, CAF, АТ, СТ.При прогрессировании процесса, 2-3 линия химиотерапии с включением таксанов, винорельбина, капецитабина, препаратов платины, гемцитабина. При противопоказании к антрациклинам CMF, монотерапия капецитабином.
Высокий риск: пациенты с быстро прогрессирующим заболеванием, висцеральным поражением, гормонотрицательными рецепторами: FAC, CAF, AT, СТ, капецитабин.
1. При прогрессировании процесса проведение 2-3 линии химиотерапии с таксановыми препаратами.
2. При резистентности к таксанам в схему подключают капецитабин, гемцитабин, винорельбин, препараты платины, липосомальный доксорубицин. Химиопрепараты могут быть использованы в комбинации или в монорежиме, а также в комбинации с таргетными препаратами при гиперэкспрессии Her-2-neu (трастузумаб, лапатиниб).
3. При частичном или отрицательном ответе продолжают пробные курсы химиотерапии препаратами, проявляющими чувствительность к РМЖ.
4. При отсутствии ответа на все линии противоопухолевой терапии, больные переводятся на поддерживающую терапию.Кроме того, в качестве второй линии химиотерапии рекомендуется:
| 1. | Доцетаксел 75 мг/м2 1-й день, доксорубицин 50 мг/м2 1-й день, циклофосфан 500 мг/м2 1-й день |
| 2. | Доцетаксел 75 мг/м2 1-й день, цисплатин 75 мг/м2 1-й день |
| 3. | Доцетаксел 75 мг/м2 1-й день, винорельбин 20 мг/м2 в 1-й, 5-й дни |
| 4. | Доцетаксел 75 мг/м2 11-й день, фторурацил 500 мг/м2 2-й, 3-й, 4-й дни |
| 5. | Капецитабин 2500 мг/м2 с 1-го по 14 дни, доцетаксел 75 мг/м2 1-й день |
| 6. | Паклитаксел 90 мг/м2 1-й день, цисплатин 60 мг/м2 1-й день |
| 7. | Паклитаксел 135 мг/м2 1-й день, винорельбин 20 мг/м2 в 1-й, 8-й дни |
| 8. | Винорельбин 30 мг/м2 с 1-го по 5-й дни, доксорубицин 50 мг/м2 1-й день |
| 9. | Винорельбин 20-25 мг/м2 в 1-й и 15-й дни, цисплатин 80 мг/м2 1-й день |
| 10. | Винорельбин 25 мг/м2 в 1-й и 8-й дни, митомицин С 7 мг/м2 1-й день |
| 11. | Винорельбин 25 мг/м2 в 1-й и 8-й дни, фторурацил 750 мг/м2 в 1-й и 8-й дни |
| 12. | Митомицин С 8 мг/м2 1-й день, митоксантрон 8 мг/м2 1-й день, метотрексат 30 мг/м2 1-й день |
| 13. | Золендровая кислота 4 мг 1 раз в 28 дней |
| 14. | Памидроновая кислота 90 мг в/в, 1 раз в 28 дней |
| 15. | Липосомальный доксорубицин 30 мг/м2 1 раз в 3 недели |
| 16. | Паклитаксел 80 мг/м2 1-й, 8-й, 21-й дни, транстузумаб 4 мг/кг в/в, затем 2 мг/кг еженедельно |
| 17. | Капицетабин 1000 мг/м2 с 1-го по 14-й дни, лапатиниб 1250 мг/м2 ежедневно |
| 18. | Бевацизумаб 10 мг/кг в/в, 0-й и 14-й дни, паклитаксел 90 мг/м2 в/в, 1-й, 8-й, 15-й дни |
| 19. | Бевацизумаб 15 мг/кг в/в, 0-й день, доцетаксел 75-100 мг/м2 в/в, 1-й день |
| 20. | Бевацизумаб 15 мг/кг в/в, 0-й день, гемцитабин 1250 мг/м2 в/в, 1-й, 8-й день |
| 21. | Тегафур 800-1000 мг/м2 внутрь, ежедневно до суммарной дозы 30 г, повторение цикла через 2-3 недели |
Низкий риск: пациенты с длительным безрецидивным периодом, положительными гормональными рецепторами, или только костным поражением, без поражения внутренних органов.
Проведение гормонотерапии у менопаузальных больных ингибиторами ароматазы: летрозол по 2,5 мг ежедневно, длительно или анастрозол по 1 мг ежедневно, длительно.
При прогрессировании процесса больным назначаются антиэстрогены – тамоксифен или торемифен. При дальнейшем прогрессировании процесса 3 линия гормонотерапии – фулвестран по схеме: 500 мг нагрузочная доза, затем по 250 мг, 1 раз в 28 дней. В настоящее время закончены исследования по увеличению дозы фулвестрана, в котором показана достоверно большая активность фулвестрана в режиме: фулвестран – 500 мг, 1 день, 14 день, затем по 500 мг 1 раз в 28 дней.
При рефрактерности к фулвестрану переходят на химиотерапию. У женщин в пременопаузе при наличии 8 и более метастатических лимфатических узлов после завершения ПХТ и при достижении стабильного клинического эффекта, продолжающейся менструальной функции показано выключение функции яичников (агонисты рилизинг-гормонов ЛГГ (трипотрелин 3,75 мг каждые 28 дней, в течение 2 лет; гизерелин 3,6 мг каждые 28 дней, в течение 2 лет), или овариэктомия) с последующим назначением антиэстрогена - тамоксифена по 20 мг или торемифена по 60 мг в сутки, до прогрессирования процесса.
Схемы химиотерапии, не содержащие анрациклинов:
- паклитаксел 135 мг/м2 1-й день, винорельбин 20 мг/м2 1-й, 8-й дни;
- винорельбин 30 мг/м2 1-й и 5-й дни, доксорубицин 50 мг/м2 1-й день;
- винорельбин 20-25 мг/м2 1-й и 15-й дни, цисплатин 80 мг/м2 1-й день;
- винорельбин 25 мг/м2 1-й и 8-й дни, фторурацил 750 мг/м2 1-й и 8-й дни;
- капецитабин 2500 мг/м2 с 1-го по 14-й дни, винорельбин 25 мг/м2 1-й, 8-й дни;
- капецитабин 2500 мг/м2 с 1-го по 14-й дни, гемцитабин 1000 мг/м2 1-й, 8-й дни;
- доцетаксел 75 мг/м2 1-й день, гемцитабин 1000 мг/м2 1-й, 8-й дни, винорельбин 25 мг/м2 1-й, 8-й дни;
- гемцитабин 1000 мг/м2 1-й, 8-й дни, паклитаксел 100 мг/м2 1-й, 8-й дни;
- карбоплатин 300-400 мг/м2 1-й день, капецитабин 2500 мг/м2 с 1-го по 14-й дни;
- этопозид 50-100 мг/м2 в 3 приема, 1-5 дн.
При гиперэкспресси Her 2/neu (+3) в схему лечения химиотерапии включается трастузумаб 8 мг/кг – нагрузочная доза, в последующем по 6 мг/кг каждые 3 недели. У больных с прогрессированием, на таргетной терапии трастузумабом возможен переход на вторую линию таргетной терапии с включением лапатиниба - 1250 мг 1 раз в сутки в комбинации с капецитабином или паклитакселом.
Для больных с люминальным В типом РМЖ рекомендована таргетная терапия лапатинибом 1500 мг в комбинации с гормональной терапией – ингибиторами ароматазы.При наличии костных метастазов при любых стадиях заболевания, включение в схему лечения бисфосфонатов (памидроновая кислота, золедроновая кислота, денозумаб). При необходимости - подключение ЛТ.
При наличии метастазов головного мозга: химиолучевая терапия с включением всех тропных препаратов, проникающих через ГЭБ, в т.ч. и темодала.
Больным РМЖ с изъязвленной опухолью, осложненной инфицированием, кровотечением, выполняется паллиативная мастэктомия с санитарной целью. Лечение дополняется химиолучевой, гормональной терапией.
Методика лучевой терапии
Дистанционная лучевая терапия проводится по методике конвенциального (стандартного) или конформного облучения РОД 1,8-2,0-2,5 Гр, 5 фракций в неделю до СОД 60-64 Гр в самостоятельном режиме, СОД 50-60 Гр («Boost») в послеоперационном режиме после органосохраняющих операций, СОД 40-50 Гр после радикальных мастэктомий. Используется непрерывный курс лучевой терапии. Облучение проводится на гамматерапевтических аппаратах или линейных ускорителях.
Техника лучевой терапии: лучевая терапия молочной железы и зон регионарного метастазирования (надподключичной, подмышечной) осуществляется тормозным излучением ускорителя (6 МэВ) или на гамма-терапевтических аппаратах (1,25 МэВ), а парастернальной зоны – путем чередования фотонного и электронного пучков или только электронным излучением до 20 МэВ в зависимости от глубины залегания цепочки парастернальных лимфатических узлов. Облучение парастернальной зоны с помощью 60Со или только фотонным пучком с энергией свыше 4 МэВ чревато развитием постлучевого пульмонита, медиастинита, перикардита. Предоперационную лучевую терапию во многих научных центрах мира не проводят.
Послеоперационное облучение передней грудной стенки после мастэктомии или облучения оставшейся молочной железы после радикальной резекции осуществляется фотонным пучком 1,25 МэВ или 6 МэВ с тангенциальных полей, направленных таким образом, чтобы в зону 100%-й изодозы попадало не более 2 см легочной ткани.
Тангенциальные поля Границы:
1. Верхняя – уровень грудинно-ключичного сочленения (угол Луиса); если необходимо, верхняя граница может быть расположена выше, чтобы включить всю молочную железу.
2. Медиальная – вдоль середины грудины.
3. Нижняя – на 2 см ниже субмаммарной (переходной) складки.
4. Латеральная – на 2 см латеральнее пальпируемой ткани молочной железы, обычно вдоль среднеподмышечной линии.
В послеоперационном периоде после мастэктомии границы тангенциальных полей следующие:
1. Верхняя – угол Луиса.
2. Медиальная – срединная линия тела.
3. Нижняя – на уровне субмаммарной складки противоположной железы.
4. Латеральная – средняя подмышечная линия.
При нетипичной локализации послеоперационного рубца и расположении его за пределами обозначенных границ полей облучения, рекомендуется дополнительное облучение зоны рубца с захватом тканей не менее чем на 2 см за его пределами. Такое облучение должно осуществляться электронным пучком или с помощью контактной лучевой терапии.
Надподключичное поле
Облучение надподключичных и подмышечных лимфатических узлов происходит с переднего поля и наклоном пучка на 10–150 к одноименной стороне, чтобы избежать облучения пищевода и трахеи.
Верхний край поля – на уровне верхнего края перстнещитовидного углубления.
Медиальная граница – середина грудины.
Латеральная граница – медиальный край головки плеча; при необходимости облучение всей подмышечной впадины, боковая граница должна быть расширена до латерального края головки плеча, которая должна быть прикрыта защитным блоком.
Нижняя граница соприкасается с верхней границей тангенциального поля на уровне прикрепления второго ребра к грудине (угол Луиса).
Всегда обязательно защищаются свинцовым блоком гортань, пищевод, трахея.
Заднее подмышечное поле используется при необходимости облучения всей подмышечной зоны.
Медиальная граница поля расположена на 1 см кнутри от края грудной клетки.
Верхняя граница – верхний край ключицы.
Боковая граница – латеральный край головки плеча.
Нижняя граница – тот же уровень, что и нижний край надподключичного поля.
Парастернальное поле Границы:
1. Медиальный край – средняя линия грудины.
2. Латеральный край – на 4-5 см латеральнее средней линии.
3. Верхний край – нижний край надподключичного поля.
4. Нижний край – основание мечевидного отростка грудины.
При облучении нескольких смежных полей расстояние между границами этих полей следует определять в зависимости от выбранного вида энергии излучения.Размеры поля облучения выбираются индивидуально при предлучевой подготовке с помощью УЗИ, компьютерного томографа, рентгеносимулятора.
Стандартное послеоперационное облучение проводится в режиме обычного фракционирования дозы (РОД 2 Гр, СОД 40 Гр) на молочную железу, грудную стенку и зоны регионарного метастазирования. При наличии в учреждении электронного пучка, у больных, подвергшихся радикальной резекции, зона послеоперационного рубца может дополнительно облучаться в дозе 12 Гр.
Рак молочной железы у мужчин
Рак молочной железы у мужчин лечится так же, как и рак молочной железы у женщин при центральной локализации опухоли. Следует помнить, что органосохраняющие операции у мужчин не выполняются. Во всех случаях производится мастэктомия.
Рак Педжета
При отсутствии опухолевого узла в молочной железе проводится только хирургическое лечение (мастэктомия по Madden или Patey). Допустимо выполнение широкой центральной резекции с послеоперационной лучевой терапией на молочную железу. При наличии опухоли в молочной железе болезнь Педжета лечится как рак соответствующей стадии.
Отечно-инфильтративный рак
1. При рецепторе положительной опухоли у больных в постменопаузе, лечение может быть начато с гормонотерапии: тамоксифен по 20 мг ежедневно или торемифен 60 мг либо ингибиторы ароматазы у больных в постменопаузы. Эффективность гормонотерапии оценивается не ранее чем через 3 месяца после начала лечения.В случае прогрессирования больная переводится на 2 линию гормонотерапии – ингибиоторы ароматазы или антиэстрогены, в зависимости от того, какой препарат использовался в первой линии гормонотерапии. При прогрессировании на второй линии гормонотерапии, больная переводится на 3-ю линию гормонотерапии – фулвестраном (режимы введения описаны выше). При прогрессировании на фулвестране пациентка переводится на химиотерапию. Принципы химиотерапии те же, что и при лечении метастатического рака молочной железы.
2. Лучевая терапия по радикальной программе (РОД 2 Гр, 5 фракций на молочную железу и регионарные зоны суммарной дозы 60). В промежутке между первым и вторым этапами может быть выполнена двусторонняя орхиэктомия (до начала лечения таким больным целесообразно выполнить трепан-биопсию для изучения гормонорецепторного статуса опухоли).
В дальнейшем – наблюдение либо паллиативная мастэктомия (при возобновлении роста опухоли или метастазов в лимфатических узлах).Профилактические мероприятия:
1. Избегать травматизации молочных желез.
2. При появлении вышеописанных жалоб своевременное обращение за медицинской помощью.
3. Своевременное лечение доброкачественных опухолей молочных желез.
Наблюдение, сроки и объем обследования
После окончания специального лечения в течение первых двух лет больные наблюдаются каждые 3 месяца, на третьем году – каждые 4 месяца, на 4-5-м году – 1 раз в полгода, затем 1 раз в год.
При наблюдении в течение первых 5 лет, раз в полгода необходим общий анализ крови, в последующем это исследование проводится 1 раз в год.
При каждом посещении необходим осмотр онкологом, онкогинекологом.
Рентгенологическое исследование легких в течение первых 3-х лет необходимо выполнять 1 раз в полгода, затем 1 раз в год.
В объем контрольного обследования входят: УЗИ молочных желез, послеоперационных рубцов, регионарных зон, печени.
Маммография противоположной молочной железы. Рентгенография ОГК.
Индикаторы эффективности лечения:
1. Маммография.
2. КТ-данные.
3. МРТ-данные.
4. Уменьшение размеров образования и увеличенных лимфоузлов.
5. Удовлетворительные показатели крови, мочи, биохимии.
6. Заживление послеоперационной раны.
7. Относительно удовлетворительное состояние больной.
8. Отсутствие отдаленных мтс при сцинтиграфии (ФЭКТ) скелета, по показаниям.
9. Отсутствие отдаленных мтс, ПЭТ по показаниям.
diseases.medelement.com