Таргетная терапия при раке молочной железы
Принцип таргетной терапии рака молочной железы, применяемые препараты и эффективность
Лечение рака молочной железы заключается в удалении массива злокачественных клеток, которая могла быть до этого уменьшена в размерах с помощью лучевой терапии или специальных препаратов (химиотерапия и гормонотерапия), с последующей профилактикой рассевания злокачественных клеток по кровеносному или лимфатическому руслу.
К сожалению, как химиотерапия, так и облучение различными изотопами, необходимые для профилактики рецидивирования и метастазирования карциномы, являются токсичными для организма методами. Улучшить их переносимость можно, если дополнять лечение препаратами, не действующими на здоровые клетки. На это рассчитана появившаяся не так давно методика – таргетная терапия рака молочной железы.
Суть методики

К 90-м годам двадцатого века ученые открыли и изучили большинство ключевых механизмов, регулирующих деление и выживаемость раковых клеток. Стало известно, что на их поверхности имеются особые рецепторы, сигнал от которых «включает» специфические ферменты и химические вещества, и таким образом карцинома постоянно растет, обходит иммунную защиту и может метастазировать.
Структур подобного строения в здоровых клетках нет. То есть, если организовать «адресную доставку» конкретно к опухолевым составляющим, можно остановить прогрессирование карциномы. Именно в этом и состоит суть таргетной терапии («таргет» в переводе с английского означает «мишень»).
Подобный вид лечения рака молочной железы является особым подвидом медикаментозной терапии, и может применяться как вместе с препаратами для «классической» химиотерапии, так и без них. Таргетная терапия не предполагает отказ от лучевой терапии или операции.
Большинство препаратов, применяемых для таргет-лечения, не уничтожают клетки карциномы молочной железы. Они подавляют механизмы, благодаря которым:
- или отдается команда к их делению;
- или ранее блокировалась их дифференцировка, из-за чего опухоль была менее дифференцированной, то есть – более быстро делящейся и злокачественной.
Виды таргетных агентов
Препараты для таргетной терапии при раке молочной железы позволяют длительно сдерживать рост опухоли или уменьшить массу находящихся в ней клеток. Такой перевод рака из крайне агрессивного и непредсказуемого состояния в хоть и злокачественное, но вялотекущее заболевание, является целью не худшей, чем полное излечение.
Агенты таргет-терапии, одобренные для лечения маммарной карциномы, разделяют на три больших группы:
- Средства, направленные на определенные «таргеты»-мишени. Это, например, антиэстрогены или анти-HER2-средства: Герцептин, Лапатиниб.
- Препараты, которые должны ухудшить условия существования опухоли. Это, к примеру, антиангиогенные средства (ангиогенез – это развитие новых сосудов, в частности, внутри опухоли).
- Лекарства, подавляющие передачу сигнала внутри массы раковых клеток. Большинство таргет-агентов еще проходят фазы клинических исследований.
Большинство данных препаратов относятся к классу моноклональных антител. Это молекулы, идентичные тем, которые образуются при вторжении в организм чужеродного агента.
Плюсы таргетной терапии
Применение подобного лечения:
- оптимально на ранних стадиях патологии, но также приносит хорошие результаты таргетная терапия, проводимая при раке молочной железы с метастазами;
- возможно, когда противопоказана химиотерапия;
- позволяет избежать коррекции уровня гемоглобина;
- обладает минимальными побочными действиями;
- в сочетании со стандартными видами терапии санкционирует значительное снижение риска появления подобной же опухоли после ее удаления и облучения ложа;
- увеличивает процент выживаемости.
Анти-HER2-терапия
HER2 расшифровывается как рецептор 2 типа к молекуле под названием «человеческий ростовой эпидермальный фактор». Особенностью такого рецептора (вещество белковой структуры, расположенное на опухолевых клетках) является способность распознавать большинство сигналов от молекул-активаторов роста. Когда подобных рецепторов появляется много (это наблюдается в около 30% случаев рака молочной железы), это значительно ухудшает выживаемость и чаще вызывает рецидивы, если применять только стандартные терапевтические методы.
Выходом является применение блокаторов HER2- фактора. Основным из них является трастузумаб (Герцептин). Такие лекарственные средства, заблокировав сигналы рака к делению, останавливают его прогрессию.
Герцептин
Механизмы, по которым работает этот препарат, остаются неизвестными. Можно только предположить, что опухолевые клетки гибнут из-за того, что средство действует подобно антителу.
Таргетная терапия рака молочной железы Герцептином эффективна и при метастатическом раке, и при большом количестве HER2- рецепторов. Препарат дает лучшие результаты при использовании у ранее нелеченных больных – 35%, тогда как эффективность его применения у женщин, получавших до этого химиотерапию – 15% (данные приведены для монотерапии). Он может быть использован как самостоятельно, так и в комбинации с другими препаратами.
Для терапии рака груди Герцептин используется уже много лет. Полученные за это время данные свидетельствуют, что он требует длительного применения: до достижения ремиссии онкопатологии его применяют в комбинации с 1-2 цитостатиками (препаратами для химиотерапии), позже женщины должны получать трастузумаб в виде монотерапии. Даже если на фоне применения Герцептина неоперированный рак прогрессирует, отменять препарат не стоит, так как он повышает выживаемость: получавшие его женщины при прогрессировании прожили (в среднем) еще 20,1 месяцев, тогда как те, кому его отменили – всего 13,4 месяца.
Герцептин эффективен для лечения HER2-позитивного рака на любых его стадиях. Он увеличивает выживаемость при этом крайне агрессивном опухолевом процессе на 40%.
Применение трастузумаба после радикальной операции, когда признаков метастазов нет, но возможные микрометастазы уничтожить нужно, одобрено FDA с 2006 года. Наилучший эффект его достигается, если он применяется совместно с таксан-содержащей терапией. Сейчас ведутся исследования, какая продолжительность применения данного препарата для таргетной терапии оптимальнее: 9 недель, 6 месяцев или год.
Герцептин эффективен и перед проведением радикального вмешательства и радиотерапии для сокращения объема операции. До его введения в неоадъювантную терапию ремиссия достигала 23-34%, а в случае HER2-позитивного рака – 10-15%. С применением трастузумаба частота достижения лечебной морфологической ремиссии составила 43-54%.
Герцептин:
- уменьшает размеры метастазов;
- позволяет сохранять достаточное качество жизни при неоперабельной опухоли;
- уничтожает те единичные опухолевые клетки, которые успели распространиться за пределы груди;
- не ингибирует иммунные силы организма;
- вдвое снижает вероятность развития рецидива после удаления опухоли;
- интактен для желудочно-кишечного тракта;
- только изредка может гриппоподобные симптомы;
- с большой осторожностью применяется у женщин с заболеваниями сердца.
К сожалению, некоторые типы маммарных карцином могут быть резистентны к Герцептину изначально, или эта нечувствительность может выработаться в процессе лечения. Это объясняется или появлением других путей, по которым опухоль начинает обмениваться сигналами, или изменением HER2-рецепторов, на которые действует препарат. В случае резистентности эффективным является дополнение таргетной терапии Лапатинибом. Это молекула, которая блокирует сразу несколько путей стимуляции клетки рака, помогает преодолеть резистентность к трастузумабу (это было доказано).
Пертузумаб
Это новый блокатор HER2-рецепторов, блокирующий несколько путей передачи сигналов роста, проходящих через эти рецепторы. Доказано, что пертузумаб может быть применен в случае неэффективности приема Герцептина, но оптимальный результат достигается при одновременном применении этих двух средств. К тому же, такая терапия хорошо переносится, не производит токсичного действия на сердце.
Trastuzumab-DM1
Это средство представляет собой смесь Герцептина с производным другого препарата – Мэйтензина. Оно совмещает анти-HER2-воздействие и одновременную доставку токсичного для раковой клетки вещества непосредственно к ней.
Плюсом таргетной терапии Trastuzumab-DM1 является его эффективность в монотерапии, без препаратов для классической химиотерапии, что улучшает переносимость.
В настоящее время сравнивается эффективность этого средства с комбинациями других таргетных препаратов, применяемых в случае, когда при мспользовании Герцептина наблюдается прогрессирование рака.
Антиангиогенная таргетная терапия
Еще в 1971 году было доказано, что сосуды, образующиеся внутри опухоли и обеспечивающие ее питание, стимулируют ее рост и обеспечивают метастазирование, прорастание в соседние ткани. Получается, что образуется «порочный круг»: новые сосуды вызывают опухолевый рост, а это, в свою очередь, приводит к появлению новых сосудов.
Во время изучения этого феномена найдена молекула, выделяемая внутренней оболочкой этих «новых сосудов». Она названа VEGF – эндотелиальный ростовой фактор. После данного открытия учеными было начато изобретение препаратов, блокирующих VEGF, тем более, что этот фактор, в отличие от HER2, имеется практически в любом типе маммарного рака.
Анти-VEGF-терапия на сегодняшний день доказала свою эффективность, но она меньше, чем у Герцептина и подобных лекарств. Используется, в основном, препарат Бевацизумаб, являющийся моноклональным антителом. Уже через полгода применения Бевацизумаба плотность сосудов в опухоли значительно уменьшается, но после его отмены уже с третьей недели отмечается повторное усиление неоангиогенеза. В результате, сделаны выводы о необходимости более длительного применения подобной терапии.
Исследования анти-VEGF-препаратов продолжаются.
Анти-PARP-препараты
Не каждый рак груди имеет HER- и VEGF-рецепторы. Выделяют также крайне агрессивные типы карциномы. Это:
- трижды негативный рак – нечувствительный к Герцептину, эстрогенам и прогестеронам, встречающийся в 10-20% случаев;
- BRCA1-ассоцированный тип, отличающийся высокой степенью злокачественности при отсутствии рецепторов к эстрогенам, прогестерону.
Пока на эти виды карцином действуют только препараты для классической химиотерапии, но ведутся разработки ингибиторов PARP (полиАТФ-рибозно-полимеразные). Сама PARP восстанавливает разрывы цепочек ДНК в опухолевых клетках, что позволяет раку развиваться дальше. Если ее заблокировать, разрывы генома не восстанавливаются, возникает генетическая нестабильность карциномы, и она гибнет.
На данный момент анти-PARP-препарат Инипариб проходит клинические испытания, но первые их результаты обнадеживают: уменьшилась скорость прогрессирования высокозлокачественных карином, увеличилась выживаемость.
Таким образом, таргетная терапии в лечении рака молочной железы – это та «соломинка», которая позволяет поддерживать лучшее качество жизни как женщин с метастатическими опухолями, так и излечить неинвазивный рак железы, обнаруженный на ранних стадиях.
Исследования, проводимые в этой области, позволяют рассчитывать, что вскоре женщины с высокозлокачественными типами данной опухоли также смогут надеяться на увеличение продолжительности жизни и улучшение ее качества. На сегодняшний день трудность заключается в недостаточности достоверных онкобиомаркеров, которые бы позволили изобрести новые виды агентов для таргетной терапии.
ginekolog-i-ya.ru
Таргетная терапия при раке молочной железы
 Рак молочной железы – одно из наиболее распространенных онкологическое заболеваний у женщин. В структуре онкологических заболеваний у женщин в нашей стране рак груди занимает лидирующее место. Каждая 8-я женщина в России в течении жизни заболеет раком молочной железы. В возрасте от 45 до 55 лет рак груди является основной причиной смерти у женщин в нашей стране.
Рак молочной железы – одно из наиболее распространенных онкологическое заболеваний у женщин. В структуре онкологических заболеваний у женщин в нашей стране рак груди занимает лидирующее место. Каждая 8-я женщина в России в течении жизни заболеет раком молочной железы. В возрасте от 45 до 55 лет рак груди является основной причиной смерти у женщин в нашей стране.
Стандартные (классические) методы лечения
В лечении рака молочной железы традиционно используются:
- Радикальное хирургическое лечение
- Лучевая терапия
- Химиотерапия
В последние два десятилетия им на смену пришли новые методы, базирующиеся на достижениях иммунологии и генетики – иммунотерапия и генотерапия.
При применении классических методов лечения происходит неспецифическое воздействие как на раковые клетки, так и на окружающие их здоровые ткани организма. Для хирургиеского лечения даже принят за основу принцип «иссечения в пределах здоровых тканей», однако, и он не гарантирует от того, что часть раковых клеток с током межклеточной жидкости и лимфы не оказалась в окружающих тканях. При лучевой терапии жесткое рентгеноское излучение на пути к опухоли проходит сквозь кожу, клетчатку, мышцы, легкие, в дополнение к первичному опухолевому очагу. При химиотерапии препараты обладают в большинстве своем цитотоксическим действием, угнетая возможность размножения и восстановления быстроделящихся клеток, а также нарушая функции и вызывая частичную гибель клеток печени, почек, сердца.
Несмотря на наличие побочных эффектов, грамотно и своевременно проведенная комбинированная терапия, включаяющая резекцию первичного очага опухоли, подавление периферических очагов с помощью препаратов химиотерапии и лучевой терапии, а также гормонотерапия для профилактики рецидивов и отдаленных метастазов, позволяет улучшить прогноз 5-летней выживаемости больных до 85-90%.
Таргетная терапия как одна из последних технологий в лечении рака груди
Последние два десятилетия привели к прорыву в области лечения рака молочной железы – в клиническую практику вошли препараты точечного воздействия на измененные раковые клетки. Они получили название «таргетных» - или препаратов цели (англ.target). Как синоним используется термины “молекулярная таргетная терапия” и „иммунная таргет-терапия“. Таргетная терапия вызывает только гибель опухолевых клеток, практически не оказывая неблагоприятного воздействия на остальные ткани организма, и, как следствие, практически не вызывает побочных эффектов.
Таргетные препараты могут применяться как самостоятельно, так и в сочетании с другими методами лечения болезни рак груди. при этом они используются и с профилактическими и с лечебными целями, включая пациенток с распространенными, метастатическими формами болезни.
Таргетные препараты воздействуют на молекулярные структуры – наружные и внутриклеточные рецепторы, белки, которые продуцирует клетки опухоли, а также разрастающиеся вокруг опухоли кровеносные сосуды. Эти «мишени» очень функционирования опухолевых клеток, и их поражение приводит к гибели клеток опухоли. С 1990 года уже зарегистрировано около 15 таргетных препаратов.
Таргетная терапия в большинстве случаев переносится существенно лучше, чем препараты химиотерапии и гормонотерапии. Типичные для химиотерапии побочные эффекты (снижение числа форменных элементов крови, мукозиды, алопеция и др.) возникают только у 4% больных. Но, как и другим препаратам, средствам таргетной терапии свойственны некоторые побочные эффекты. К наиболее частым побочными действиям относятся озноб или лихорадка, но они без труда купируются противовоспалительными нестероидными препаратами, а рецидив возникает у менее 3% больных. Хотя бы один нежелательный симптом развивается у 84% пациентов, из них лишь 14% сталкиваются с тяжелым осложнением. Среди наиболее значимых осложнений можно назвать нарушение функции сердца. Поэтому назначать средства таргетной терапии может только врач после тщательного обследования состояния здоровья пациента.
Препараты
Препараты таргетной терапии могут использоваться как самостоятельно, так и в комплексе с традиционными способами лечения злокачественных новообразований. Под действием препаратов на определенные молекулы рост и деление раковых клеток блокируется. Некоторые препараты могут не только остановить рост опухолевых клеток, но и запустить процесс их уничтожения. Сочетание этих препаратов с другими методами лечения дают возможность уменьшить лучевую нагрузку или дозу химиотерапии. Очень важно знать, что все препараты таргетной терапии могут быть использованы у всех пациенток. Обязательным является проведения тестов на определение рецепторной чувствительности – иммуногистохимического исследования кусочков ткани опухоли, полученного во время биопсии или при проведении хирургического лечения. С помощью иммуногистохимии уточняется количество эстрогеновых, прогестероновых и HER-2-рецепторов на клетках опухолевых тканей.
Наиболее часто при лечении рака груди используются несколько классов таргетных препаратов, в том числе блокирующие рецептор человеческого эпидермального фактора роста–2 и тормозящих рост кровеносных сосудов около опухоли, воздействующих на клеточные рецепторы эстрогена, ингибирующие один ключевых ферментов система эстрогенов - ароматазу, а также угнетающие PARP – белок.
Селективные модуляторы эстрогеновых рецепторов.
Препаратами таргетной терапии, впервые внедренными в клиническую практику, стали вещества, избирательно блокирующие рецепторы эстрогенов на поверхности опухолевых клеток. К ним относят тамоксифен, торемифен (Фарестон), фулвестрант (Фазлодекс). В отличие от собственных гормонов, которые обратимо связываются с рецептором и активируют в опухолевых клетках процессы роста и размножения, селективные блокаторы связываются с рецепторами эстрогенов необратимо, что значительно снижает уровень эстроген-рецепторов в клетке и в конечном итоге вызывает ее гибель. К этим препаратам чувствительны опухоли с большим количеством эстрогеновых рецепторов - ER–позитивные опухоли.
Таргетные препараты другого класса, к которым также чувствительны ER–позитивные опухоли, представлены “ингибиторами ароматазы” - экземестаном (Аромазин), летрозолом (Фемара), анастрозолом (Аримидекс). Ароматаза - основной фермент, участвующий в выработке эстрогенов. Снижение активности ароматазы резко снижает уровень синтеза эстрогенов и подавляет жизнедеятельность опухолевых клеток, которым необходим эстроген как естественный стимулятор роста. Применение ингибиторов ароматазы ограничено женщинами, находящими в менопаузе, поскольку в функционирующих яичниках количество ароматазы таково, что его невозможно подавить лекарственными препаратами.
Селективные блокаторы ростовых факторов включают бевацизумаб (Авастин), панитумумаб (Вектибикс), цетуксимаб (Эрбитукс), трастузумаб (Герцептин). Бевацизумаб является блокатором ангиогенеза - фактора роста сосудов, применение которого позволяет затормозить развитие сосудистой сети вокруг опухолевых клеток и тем самым замедлить рост опухоли. Панитумумаб и цетуксимаб блокируют на опухоли рецепторы к эпидермальному фактору роста и тормозят прогрессирование опухоли.
Мишенью для трастузумаба (герцептина) является рецептор человеческого эпидермального фактора роста (англ. human epidermal growth factor receptor, сокращенно - Her-2). Уникальной особенностью Her-2 опосредование большинства сигналов активаторов роста, передающихся к опухолевым клеткам. По сравнению с другими таргетными препаратами трастузумаб имеет существенно большую эффективность в отношении подавления (супрессии) опухолевых клеток. Кроме того, трастузумаб стимулирует иммунную систему к атаке на клетки, имеющие высокую концентрацию Her-2.
Перспективными препаратами таргетной терапии являются ингибиторы (блокаторы) PARP–белка, которые принимают участие в восстановления поврежденной ДНК, которая очень активная в опухолевых клетках. Блокада PARP–белка включает программу “клеточной смерти” (апоптоз). Основными препаратами данной группы являются Олапариб, Инипариб, Велипариб. Блокаторы PARP–белка применяются в тех случаях, когда клетки опухоли не имеют основных рецепторов – эпидермального фактора роста Her-2, эстроген-рецептора ЕR, прогестеронового рецептора PR - “три-негативные опухоли”.
Прогноз
Таргетная терапия рака молочной железы может использоваться как с профилактической целью при возможном рецидиве заболевания, так и для контролирования распространения метастазов. Применение этих инновационных препаратов настолько эффективно, что пациент может жить долгие годы с онкологическим заболеванием, при этом качество его жизни весьма удовлетворительно. По прогнозам специалистов, молекулярная терапия – это начало пути. И, возможно, настанет время, когда можно будет говорить о полной излечимости злокачественных образований даже на поздних стадиях.
Из препаратов таргетной терапии наибольшее распространение в мире получает трастузумаб (герцептин), поэтому рассмотрим его применение наиболее детально.
Трастузумаб применяется в лечении HER-2-позитивного рака груди на 2, 3-й и 4-й стадиях. HER-2-позитивными является примерно 20-25% всех опухолей. Чаще всего они характеризуются быстрым, прогрессивным течением. Герцептин эффективен при лечении как метастатических форм рака, так и ранних форм рака молочной железы. Особенно эффективен герцептин при метастазах рака груди, которые продуцируют избыточные количества HER2-белка. Герцептин применяется изолированно и в сочетании с химиотерапией, применяясь одновременно или последовательно. Совместно с герцептином, как правило, используются такие химиопрепараты, как 5-фтроурацил, таксотер, таксол, навелбин, кселода, гемзар. В отличие от препаратов химиотерапии, которая проводится определенным числом курсов, герцептин может приниматься в течение неопределенного времени, особенно при метастатических формах рака молочной железы.
Действие герцептина на клетки опухоли приводит к следующему:
- уменьшению размеров метастатических очагов и уничтожение недиагностирующихся одиночных опухолевых клеток, распространившихся за пределы собственно молочной железы. - снижению риска рецидива рака молочной железы после хирургического лечения.
Важно: герцептин применяется строго внутривенно капельно. При этом первая доза герцептина вводится в течение 90 мин. а вторая и последующие – не менее 30 мин. Как правило, герцептин назначается один раз в 1 – 3 недели.
Герцептин в отличие от обычных химиопрепаратов практически не обладает побочными эффектами: препарат не вызывает нарушений со стороны желудочно-кишечного тракта и не подавляет иммунную систему. В редких случаях герцептин вызывает симптомы, характерные при простуде.
Диагностика и составление индивидуального плана лечения.
Для того чтобы определить лучший план лечения рака груди, необходима комплексная диагностика.
therapycancer.ru
Таргетная терапия при раке молочной железы
Таргетная терапия (от английского слова the target – мишень) – системная терапия направленная против опухоли, отдаленных микрометастазов или метастазов. Некоторые авторы называют ее иммунотерапией или биологической терапией рака.
Таргетная терапия основана на действии моноклональных антител, которые специфически связываются с особыми рецепторами на поверхности раковой клетки. Эти антитела аналогичны обычным человеческим антителам, которые в продуцируют B-лимфоциты. Однако B-лимфоциты не продуцируют антитела против молекулярных рецепторов расположенных на раковой клетке. Препараты моноклональных антител (monoclonal antibody – MAB) являются сверх-высокотехнологичными современными лекарствами.
Таргетная терапия может применяться как в комплексном радикальном лечении рака груди (адъювантный режим), так и в лечении метастатической болезни (лечебный режим)
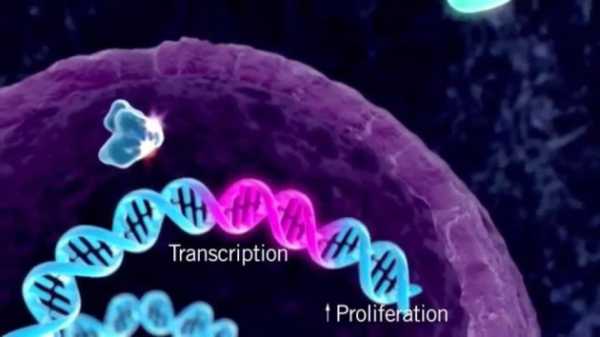
Принцип действия
Опухоль – заболевание генетического аппарата клетки. Как правило, для проявления злокачественных свойств, в геноме клетки должно случиться минимум 4 структурных поломки. Существуют как общие изменения в генах, провоцирующие появление опухоли, так и индивидуальные, характерные только для определенных видов опухолей. Для рака груди характера следующая «поломка»: установлено, что у женщин, страдающих раком молочной железы, может произойти активация гена HER2, из-за чего на поверхности опухолевых клеток увеличивается количество рецепторов HER2. Подобное явление было замечено разными исследователями у 15–30% больных раком молочной железы.
В норме рецепторов HER2/neu на поверхности эпителиальной клетки около 20 тыс. На клетках рака молочной железы их количество может увеличиваться в 100 и более раз (это явление называется гиперэкспрессией). В случае гиперэкспрессии рецепторы HER2 на мембране нарушают нормальный клеточный цикл и вынуждают клетки бесконтрольно делиться.
Все специалисты, занимающиеся проблемой рака молочной железы, отмечают необходимость определения уровня рецепторов HER2/neu в опухоли для прогноза течения заболевания и эффективности химиотерапии. Важность этого теста обусловлена и тем, что при всех других благоприятных условиях, таких как небольшой размер опухоли, отсутствие метастазов в лимфатические узлы, чувствительность опухоли к гормональному лечению, гиперэкспрессия HER2/neu делает прогноз менее благоприятным. И это является сигналом к еще более внимательному подходу в выборе терапии.
Герцептин (трастузумаб)
В настоящее время широко применяется в клинической практике препарат, обладающий способностью блокировать отрицательное влияние гиперэкспрессии HER2/neu – герцептин (трастузумаб). Он представляет собой моноклональное антитело, которое специфически связывается с рецептором HER2/neu на поверхности раковой клетки и блокирует его.
Ведутся активные исследования целой группы таких лекарств. Многие ученые полагают, что за этими средствами будущее онкологии.
Читайте также: 25 мифов о раке молочной железы
Методы определения чувствительности к таргетной терапии против гиперэкспресии HER2/neu
Существует множество методик определения как активности гена, несущего информацию о рецепторе HER2/neu, так и количества самих рецепторов на поверхности клетки.
Иммуногистохимический метод
Основной – иммуногистохимический метод, техника которого заключается в специфическом окрашивании клеточной стенки с гиперэкспрессией HER2/neu. Преимущества этого метода – простота выполнения и невысокая стоимость, а также возможность проведения исследования даже через несколько лет после операции. Операционный материал фиксируется в формалине и может длительное время сохраняться в парафиновых блоках для последующих исследований. Оборотная сторона этого метода – возможные ошибки, так как метод субъективный и требует наличия опытного персонала, выполняющего не менее 300 подобных исследований в год.
Метод FISH-гибридизации
Второй метод, также признанный стандартным, — это так называемый метод FISH-гибридизации, показывающий количество генов в ядре опухолевой клетки, участвующих в производстве рецептора HER2/neu. Если происходит увеличение этих генов (явление, называемое амплификация), то вероятность гиперэкспрессии очень высока. Преимущества метода – очень высокая чувствительность и меньшая зависимость от квалификации персонала. Отрицательная сторона – дороговизна и необходимость наличия сложного оборудования.
По вышеназванным причинам первый метод является основным, а второй используется для принятия решения в спорных случаях.
Сегодня необходимость определения статуса HER2/neu не подлежит сомнению.
www.mammologia.ru
Лечение рака молочной железы: таргетная терапия, как и чем победить карциному груди?
Онкологические заболевания являются одной из самых серьезных проблем современной медицины. Среди женщин особенно часто распространена опухоль молочной железы. Это заболевание подразумевает формирование в груди очага раковых клеток, которые начинают активно делиться, формируя злокачественные новообразования. Чаще всего патологические образования в молочных железах относятся к типу «карциномы».
Способы лечения и используемые препараты
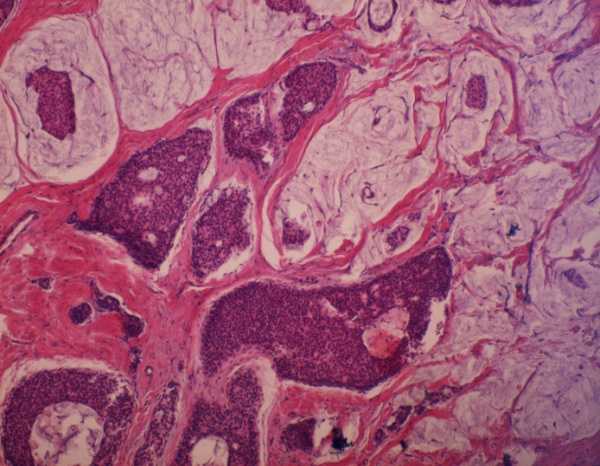
Карциномы формируются в участках организма, где есть эпителиальная ткань. Новообразования могут располагаться в молочных протоках, в отделах, образующих молоко, а также в участках, где отсутствует железистая ткань. Карциномы со временем могут распространяться по всему организму в виде развившихся метастазов.
Рак груди – не только женская проблема. Есть случаи данного заболевания и у мужчин, однако, мужчины редко подозревают у себя эту болезнь и часто обращаются за помощью слишком поздно.
Поскольку рак груди провоцируют различные факторы, то это заболевание распространяется все больше. Несмотря на усилия врачей и ученых, лечение рака молочной железы все еще является трудным делом.
Удастся ли вылечить карциному – зависит от многих обстоятельств. На это влияют индивидуальные особенности организма пациентки, течение заболевания, но самым основным аспектом является стадия развития рака. На начальных стадиях удается достаточно успешно лечить данную патологию, но этого нельзя сказать о запущенных случаях. На последней стадии болезни врачам приходится бороться за продление жизни больного, а вот возможности полного излечения почти нет.
Поэтому так важно своевременно обнаружить болезнь, чтобы лечение рака груди было успешным.
Лечение рака молочной железы проводится с помощью разных методов. Обычно эти методы используют в сочетании друг с другом, в зависимости от картины болезни. Основные методы лечения рака молочной железы таковы:
- Оперативный метод.
- Химиотерапия.
- Радиотерапия.
- Гормонотерапия.
- Таргетная терапия.
Каждый из способов лечения карцином имеет свои особенности, и прежде чем остановить выбор на одном из них, врач должен провести полную диагностику и удостовериться в его целесообразности.
к оглавлению ↑Нетрадиционная медицина
Чтобы победить болезнь, больные нередко обращаются к самым разным способам лечения. Иногда, не зная, что делать, и не доверяя традиционным методам, пациенты обращаются к народным средствам.
Несмотря на то, что есть истории о преодолевших опухоль с помощью народной медицины, следует понимать, что это очень большая редкость. Вылечить рак, используя только травы и настои, без терапевтического воздействия практически невозможно. Однако врачи не запрещают использовать данные методы. Лекарственные сборы оказывают полезное влияние на состояние организма, укрепляют иммунитет, что очень важно в процессе лечения такого серьезного заболевания. Единственным условием является согласование используемых средств с лечащим врачом, поскольку применение некоторых трав может лишь ухудшить клиническую картину.
к оглавлению ↑Основные лекарственные средства
Методы, которые используются при борьбе с опухолью, можно разделить на основные и поддерживающие. Основные позволяют полностью победить опухоль, и применяются они в тех случаях, когда исцеление возможно. Поддерживающее лечение предназначено для продления жизни пациента, если его форма болезни не лечится. Однако такое деление является условным, поскольку почти все методы основной терапии (кроме хирургического вмешательства) могут использоваться для поддерживающего лечения. Аналогичны и препараты, применяемые в обоих случаях.
Препараты, используемые при химиотерапии:
- Антиметаболиты. Данные средства создают негативные условия для деления клеток, что вызывает некроз и отмирание патологических образований (Азатиоприн и Азацитидин).
- Алкилирующие средства. Они предназначены для разрушения белков, способствующих развитию опухолевых клеток (Циклофосфамид).
- Антибактериальные препараты, направленные на уничтожение раковых клеток, а также возбудителей инфекционного процесса. Под их воздействием разрушаются клеточные мембраны патологических клеток, что ведет к их гибели (Доксициклин).
- Цитотоксические противоопухолевые препараты (Доксорубицин, Карбоплатин).
Препараты, применяемые в гормональной терапии:
- Антиэстрогены. Их действие заключается в блокировке деятельности эстрогеновых рецепторов. Основным препаратом данной группы является Тамоксифен.
- Ингибиторы ароматазы. Они препятствуют выработке женского гормона эстрогена (Герцептин).
Лекарственные средства, предназначенные для симптоматической терапии:
- болеутоляющие и противовоспалительные (Ибупрофен, Аспирин, Индометацин Морфий, Димедрол и т.д.);
- витамины (Триовит);
- кроветворные (Эритропоэтин, Рекормон и т.д.).
Оперативный метод
Чаще всего лечение рака молочной железы осуществляется с помощью операции. Именно хирургическое вмешательство позволяет вылечить рак. Однако это не означает, что этот метод не подразумевает использования других. Для подготовки к операции применяются другие варианты лечения, они же позволяют закрепить полученный результат и избежать рецидивов.
Операции по удалению опухоли бывают нескольких видов. Это:
 Органосохраняющая операция. Иначе ее можно назвать лампэктомия или квардрантоэктомия. В этом случае удаляется злокачественная опухоль, но при этом врачи стремятся сохранить как можно больше здоровой ткани. Кроме этого, данное хирургическое вмешательство позволяет добиться сохранности внешнего вида и функционирования молочной железы. Данный тип операции возможен не всегда, а лишь в тех случаях, когда раковая опухоль находится на ранней стадии развития. Для случаев метастатического рака этот вариант лечения не подходит.
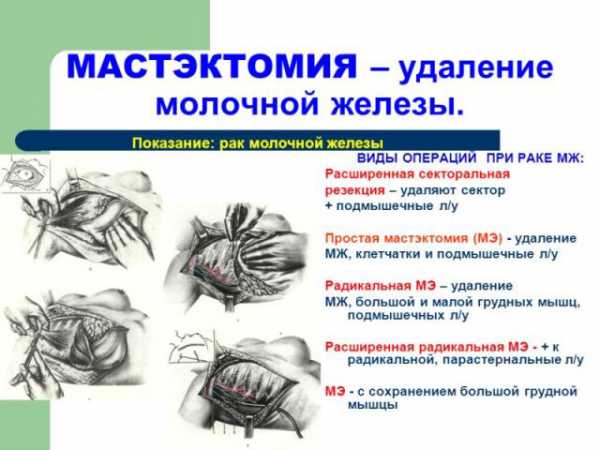
Органосохраняющая операция. Иначе ее можно назвать лампэктомия или квардрантоэктомия. В этом случае удаляется злокачественная опухоль, но при этом врачи стремятся сохранить как можно больше здоровой ткани. Кроме этого, данное хирургическое вмешательство позволяет добиться сохранности внешнего вида и функционирования молочной железы. Данный тип операции возможен не всегда, а лишь в тех случаях, когда раковая опухоль находится на ранней стадии развития. Для случаев метастатического рака этот вариант лечения не подходит.- Простая мастэктомия. Данный вид операции подразумевает удаление молочной железы, другие ткани, а также лимфоузлы в этом случае не затрагиваются. Делать ее приходится также, когда сформированы карциномы.
- Расширенная мастэктомия. Такой способ лечения требует удаления не только пораженной молочной железы, но и лимфоузлов, находящихся в подмышечной впадине. Иногда нужно делать ампутацию прилегающей мышцы или ее части. Этот вариант операции используется нечасто, лишь в тех случаях, когда более щадящее лечение не целесообразно.
Мастэктомия является радикальным способом лечения, который применяется на более поздних сроках болезни.
 После любой операции может потребоваться дополнительная терапия – чтобы закрепить результаты и избежать повторного заболевания. Из эстетических соображений женщины могут использовать протезирование груди, чтобы не выглядеть больными и не переживать из-за своего внешнего вида. Именно по этой причине предпочтение отдается органосохраняющей операции.
После любой операции может потребоваться дополнительная терапия – чтобы закрепить результаты и избежать повторного заболевания. Из эстетических соображений женщины могут использовать протезирование груди, чтобы не выглядеть больными и не переживать из-за своего внешнего вида. Именно по этой причине предпочтение отдается органосохраняющей операции.
Однако нельзя сказать, что использование операции целесообразно в любом случае. На последней стадии развития опухоли с помощью операции вылечиться нельзя, поскольку это уже формирование метастатического рака. Поэтому в самых тяжелых ситуациях врачи предпочитают использовать другое лечение рака груди, выполняющее роль поддерживающей терапии.
к оглавлению ↑Консервативные методы терапии
В традиционной медицине широкое распространение получили неоперативные методы лечения рака молочной железы. Они могут применяться как самостоятельно, так и в комплексе с хирургическим лечением.
к оглавлению ↑Химиотерапия
Нередко лечение рака молочной железы осуществляется с помощью химиотерапии (препараты платины, таксаны и т.д.). Такое лечение подразумевает использование препаратов, которые уничтожают опухолевые клетки. Для того чтобы выбрать такой вариант медицинского воздействия, необходимо тщательно изучить картину болезни.
Опухоль груди и карциномы, конечно, являются показанием для назначения химиотерапии, но это не означает, что она подходит всем пациентам. Врач должен учесть форму протекания болезнь, место расположения карциномы, активность размножения раковых клеток, возраст больной и многие другие обстоятельства, прежде чем делать подобные назначения.
Химиотерапия позволяет не только бороться с заболеванием. Ее можно использовать в качестве поддерживающего лечения, для подготовки к оперативному вмешательству, для закрепления полученных результатов. Негативная сторона химиотерапии заключается в наличии побочных эффектов, поскольку такая терапия очень агрессивна и влияет не только на опухоль, но и на здоровые ткани и органы.
У многих пациенток при химиотерапии отмечаются нарушения в работе ЖКТ, снижение иммунной защиты организма, выпадение волос.
В результате поражения яичников может наступить бесплодие, что является основным из факторов, по которым этот способ лечения не назначают молодым женщинам. Однако, данные последствия не имеют значения, если пациентка хочет победить болезнь.
к оглавлению ↑Использование радиотерапии
Другое название этого метода лечения – лучевая терапия. В ходе него очаги раковых клеток и карциномы облучаются ионизирующими лучами. Данный метод лечения очень эффективен на начальной стадии болезни, а также в роли поддерживающей терапии. Также его используют перед хирургическим вмешательством и после него.
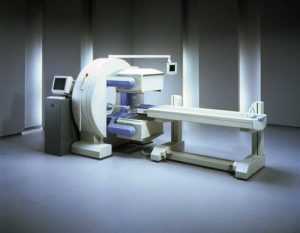 Поскольку в настоящее время используются новые технологии, есть возможность сделать воздействие лучей минимальным. Поэтому радиотерапия очень популярна. У этого способа лечения меньше побочных эффектов и осложнений, чем у химиотерапии, что позволяет делать эти процедуры для профилактики. Тем не менее, радиотерапия имеет и ряд ограничений.
Поскольку в настоящее время используются новые технологии, есть возможность сделать воздействие лучей минимальным. Поэтому радиотерапия очень популярна. У этого способа лечения меньше побочных эффектов и осложнений, чем у химиотерапии, что позволяет делать эти процедуры для профилактики. Тем не менее, радиотерапия имеет и ряд ограничений.
Ее не назначают для лечения рака груди, если пациентка уже подвергалась воздействию ионизирующих лучей в области других органов, поэтому радиотерапия нецелесообразна при лечении метастатического рака. Также противопоказанием может стать наличие некоторых заболеваний, например, сердечной недостаточности.
к оглавлению ↑Гормонотерапия
Этот метод воздействия на опухоль считается новым. Поскольку функционирование молочных желез находится под влиянием гормонов, то и формирование рака груди нередко обусловлено особенностями гормонального фона женщины. Обычно опухоль молочных желез и карциномы возникают из-за избытка эстрогена в организме больной. При наличии в раковых клетках гормональных рецепторов болезнь развивается быстрее.
Поэтому гормонотерапия основывается на использовании препаратов, которые блокируют развитие таких рецепторов, либо препятствуют излишней выработке гормонов.
Для назначения гормонотерапии необходимо провести определенное обследование, чтобы убедиться, что такая терапия окажется результативной. Если рак не является гормонозависимым, такой способ лечения не имеет смысла. Однако в остальных случаях гормонотерапия дает высокие результаты. Осуществляют ее двумя разными способами: с только помощью специальных препаратов (Тамоксифен, Герцептин) либо совместно с хирургическим путем. Выбор препарата обусловлен особенностями пациентки, в частности ее менопаузальным статусом. Хирургический способ заключается в удалении яичников.
Преимуществом метода является малое количество побочных эффектов и их незначительность.
Кроме этого, гормональная терапия очень проста в использовании и позволяет женщине жить практически обычной жизнью. Именно поэтому гормонотерапию так широко применяют и в профилактических целях и в комплексном воздействии. Ограничением может стать наличие сопутствующих заболеваний, а также негормональное происхождение опухоли.
к оглавлению ↑Особенности таргетной терапии
Таргетная терапия – это новое направление в лечении злокачественной опухоли молочных желез. Данный метод лечения считается наименее агрессивным, поскольку его использование позволяет воздействовать лишь на патологические клетки, не задевая при этом здоровые участки.
 Таргетная терапия основывается на использовании специальных препаратов, воздействующих непосредственно на опухоль (Вотриент, Нексавари др.) Это является ее неоспоримым преимуществом. Поэтому таргетная терапия может быть использована и в качестве самостоятельного метода лечения, и как часть комплекса воздействий. Но есть у нее и ограничения. Таргетная терапия не используется для пациентов, страдающих серьезными заболеваниями сердца, поскольку применяемые препараты влияют на этот орган. Поэтому прежде чем лечить пациентку таким способом, врач должен провести соответствующее обследование.
Таргетная терапия основывается на использовании специальных препаратов, воздействующих непосредственно на опухоль (Вотриент, Нексавари др.) Это является ее неоспоримым преимуществом. Поэтому таргетная терапия может быть использована и в качестве самостоятельного метода лечения, и как часть комплекса воздействий. Но есть у нее и ограничения. Таргетная терапия не используется для пациентов, страдающих серьезными заболеваниями сердца, поскольку применяемые препараты влияют на этот орган. Поэтому прежде чем лечить пациентку таким способом, врач должен провести соответствующее обследование.
Лечить рак молочной железы очень сложно. На выбор методов влияют многие обстоятельства, при том что большая их часть обладает большим количеством побочных эффектов. В некоторых случаях побороть заболевание невозможно, но необходимо продолжать лечение, чтобы продлить свою жизнь.


Статья помогла вам?
Дайте нам об этом знать - поставьте оценку
(No Ratings Yet) Загрузка...dlyagrudi.ru