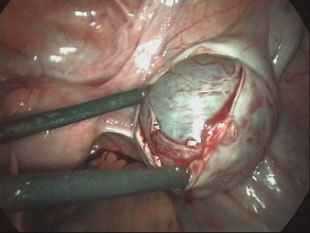
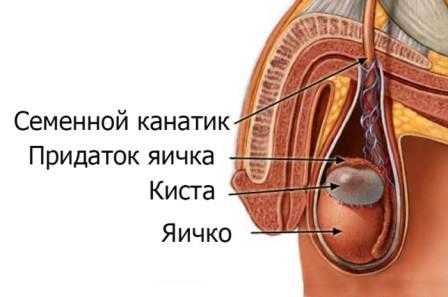
Транспозиция яичников
Транспозиция яичников: что это, как проводится, методы
Транспозиция яичников – это изменение высоты органа для сохранения его гормональной функции. При раке шейки матки или раке самой матки пациентка проходит лучевую терапию. Повышение яичников дает возможность уберечь их от облучения. После такой операции возможен забор созревших яйцеклеток для будущей беременности. Если лучевая терапия не дала положительных результатов, то проводится удаление шейки матки или матки.
Удаление происходит двумя способами:
- лапароскопией;
- лапаротомией (полостная операция).
Так как в большинстве случаев транспозиция яичников происходит во время лапароскопии, то именно об этом методе мы поговорим более детально.
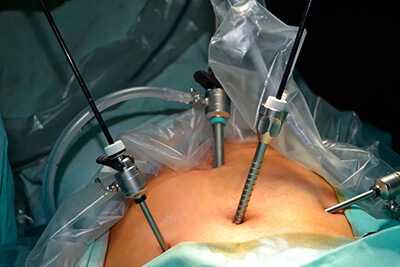
Транспозиция яичников лапароскопическим методом
Транспозиция лапароскопией набирает все больше популярности благодаря своей простоте. Зачастую ее проводят в виде амбулаторной процедуры, что дает возможность не отклоняться от графика лечения пациентки. Плюсом лапароскопии является и то, что после транспозиции возможно сразу же проводить облучение. При этом органы уже не попадают под облучение. Главным преимуществом является быстрое восстановление организма, чем при проведении полостной операции.
В транспозиции нет смысла, если при лечении рака шейки матки и тела матки нет необходимости проводить лучевую терапию.
Проведение транспозиции
Перед началом операции необходимо пройти консультацию у онколога, который решит, на какую высоту необходимо поднимать яичники. Далее вся операция транспозиции лапароскопическим методом проходит в такой последовательности:
- Врач отделяет ножку от маточной трубы (у каждой пациентки длина сугубо индивидуальна).
- Используя лапароскопический зажим, яичник перемещают в необходимую полость брюшины.
- Орган фиксируют к каналам брюшной стенки.
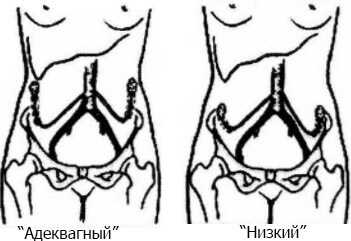
Уровни транспозиции
Главным минусом такого метода является то, что врач не может контролировать функционирование яичников, а также его достаточное кровоснабжение. Это чревато тем, что будет нарушена функция органа и, как следствие, нулевой результат операции. А ведь главной причиной транспозиции считается сохранение функциональности. Если при процедуре будет нарушен кровоток органа, то необратимым будет его некроз.
В настоящее время врачи используют лапароскопический зажим, в который встроен оптопара с инфракрасным диапазоном. Оптопара подает сигнал на приемник, и по его амплитуде врачи понимают величину кровотока ножки яичника. Если при этом амплитуда пульсации падает, то врач принимает решение о перенесении органа в другое место. Фиксация придатка в заданном месте не возможна. Новой областью закрепления может быть брюшина или подреберье. Такой метод позволяет определить максимальную длину растяжения ножки яичника с сохранением нормального кровоснабжения и его функционирования.
Суть измерения кровоснабжения:
- Во время лапароскопии врач подводит к ножке придатка зажим с приемником.
- Далее он проводит инструментом по всей длине органа, наблюдая за изменением показаний кровотока артерии.
- Когда показания достигнут критической отметки, яичник фиксируется.
Благодаря такому методу сохраняется функционирование, полноценное кровоснабжение и не требуется повторное хирургическое вмешательство.
При обычной лапароскопии без использования зажима с открытым инфракрасным диапазоном сохраняется функция органа во время лучевой терапии лечения опухолей. Однако возможно осложнения в виде нарушения кровоснабжения из-за слишком сильного вытягивания питающей ножки.
При использовании зажима в лапароскопии для операции транспозиции сохраняется нормальное питание органа и его функция. Также есть возможность перенести яичник в другое место для фиксации, что отменяет повторную операцию по восстановлению функции.

Экстирпация матки с транспозицией яичников
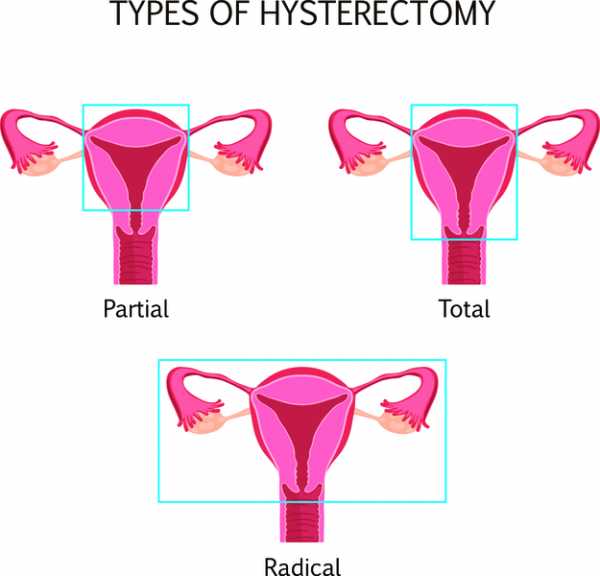
Экстирпация матки – это операция по удалению тела/шейки матки лапароскопическим или лапаротомическим методом, вследствие поражения их раком. Хирургическое вмешательство осуществляется в случае негативных результатов лучевой терапии. Довольно часто применяется расширенная экстирпация матки. При этом удаляются яичники, маточные трубы, верхняя часть влагалища, кардинальная, пузырно-маточная и крестцово-маточная связка, а также обтураторные, крестцовые и повздошные лимфоузлы.
Такая операция применяется при:
- осложнениях;
- кровотечениях;
- рецидивах болезни;
- цистите;
- ректите и др.
Противопоказания для применения расширенной экстирпации матки:
- возраст пациентки;
- ожирение последних стадий;
- наличие тяжелых заболеваний;
- сильное увеличение опухоли.
Когда есть возможность сохранения функции придатков, то предпочтительней метод экстирпации матки с транспозицией яичников. Тогда они вместе с маточными трубами, всеми примыкающими сосудами и нервными окончаниями перемещаются выше своего первоначального расположения. Благодаря этому, лучевая терапия позитивно влияет на их функцию. В процессе проведения яичники получают долю облучения, которая в среднем составляет от 90 до 130 сГр. А вот общая доза воздействия на опухоль составляется не менее 4 тыс. сГр. К тому же органы поддаются не прямому эффекту облучения, а рассеянному. В противном случае процедура грозит быстрому их истощению или полному прекращению работы функций. Дальнейший забор яйцеклетки для будущей беременности станет невозможным. 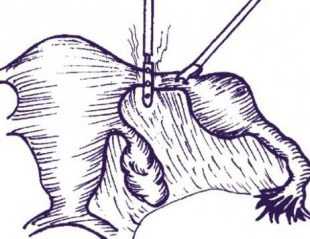
Тубэктомия при транспозиции
Тубэктомией считается удаление поврежденных или инфицированных маточных труб пациентки, вследствие чего нарушается их функционирование или вовсе существует угроза здоровью женщины.
Тубэктомия назначается в таких случаях:
- наличие опухоли маточной трубы;
- внематочная беременность;
- разрыв маточной трубы;
- воспалительные процессы хронического характера;
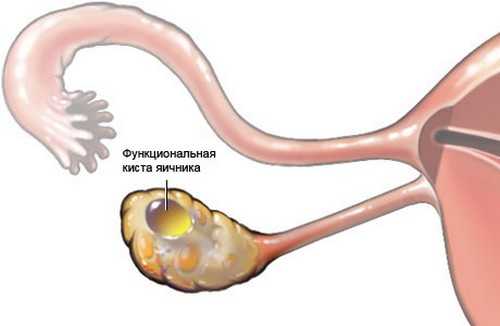
- киста яичника, перекрут ножки;
- болезнь Крона.
Если область облучения большая, то врач принимает решение перенести яичники в переднюю верхнюю ость подвздошной кости для сохранения их функции. Маточная труба отделяется ввиду того, что не может растягиваться до необходимой длины. Яичники в свою очередь более мобильны.
oyaichnikah.ru
Латеральная лапароскопическая транспозиция яичника
RANCISCO FURTADO, WILLIAM KONDO Перевод с английского Введение: Транспозиция яичников за пределы таза, с целью из защиты от излучения было впервые описано в 1958г. Данная процедура назначается пациентам у которых диагностированы злокачественные процессы требующие применения радиотерапии без удаления яичников. Процедура выполненяется лапаротомическим или лапароскопическим методом по выбору хирурга-гинеколога или наличия у него соответствующих навыков. Цель этой статьи состоит в том, чтобы описать технику латеральной транспозиции яичника лапароскопическим методом. Хирургическая техника: пациент располагается в положении Тренделенбурга, под общей анестезией. После создания пневмоперитоненума устанавливаются 4 троакара: 10мм троакар через пупок, 10мм троакар в надлобковой области и два 5мм троакара в подвздошной области с двух сторон. Яичники полностью отделяются от матки и фаллопиевых труб с разделением утеро-овариальной связки и рассечением мезовариума. Брюшина вдоль связки тазового дна может быть также рассечена, яичники перемещаются латерально и подшиваются в параколических выемках.
Две титановые клипсы прикрепляются к яичникам с целью отметить головную и хвостовую части.
Это позволяет определять постоперационную локализацию яичников, для последующего программирования облучения таза. Ключевые слова. Лапароскопия, Транспозиция яичников, рак, радиация
Заключение: Латеральная транспозиция яичников может быть выполнена благополучно и эффективно. У лапароскопического подхода есть некоторые преимущества, по сравненияю с открытым хирургическим вмешательством, включая сокращение сроков пребывания в больнице, уменьшение послеоперационных болей, меньшие разрезы и более быстрое восстановление. По этим причинам мы считаем лапароскопию золотым стандартом для латеральной транспозиции яичников.
ВВЕДЕНИЕ
Лучевая терапия — один из методов, применяемых при лечении онкологических пациентов, особенно в случае болезни Ходжкинса, опухолях мочеполовой системы и нижних отделов кишечника. В зависимости от локализации и стадии болезни излучение может направляться локально или на более широкий участок.
Это очень эффективная терапия для пациентов с ранними стадиями новообразований, но может приводить к потере функции яичников и потребности в долгосрочной гормональной терапии для молодых женщин. Роль гинеколога становится очень важной в случае попытки сохранения яичниковой функции, а следовательно и в обеспечении качества жизни пациента и в некоторых случаях возможности беременности в будущем. Перемещение яичников из области облучения, с целью сохранения яичниковой функции было впервые описано в 1958. С сообщалось о многих методах, и они были выполнены во время проведения лапаротомии или как отдельная процедура. Среди них латеральная транспозиция яичников (норма успеха до 83 %), траспозиция яичников за матку, защита яичников свинцовым щитом, экстериоризация яичников под кожу через боковой доступ, и гетеротопическая транспозиция. В последнее время хирургические методы прогрессируют и развитие методик минимально инвазивной хирургии позволяет проводить латеральную транспозицию яиников лапароскопически более эффективно, с сокращением пребывания в больнице, более ранней мобилизацией, ранее возврату к нормальной активности и уменьшению затрат.
Цель данной статьи состоит в том, чтобы описать технику лапароскопической латеральной транспозиции яичников.
ХИРУРГИЧЕСКАЯ ТЕХНИКА
Операция была выполнена под общей анестезией. Пациент размещается в положение Trendelenburg для литотомии с фиксацией обеих ног.
Катетер Foley был вставлен в мочевой пузырь для непрерывного контроля мочеотделения во время операции. Пневмоперитонеум создавался с помощью иглы Вереша и внутрибрюшное давление поддерживалось на уровне 12-14мм рт.ст. 10-миллиметровый троакар для прямой оптики был помещен в пупок, 10-миллиметровый троакар был расположен в надлобковой области, и два 5-миллиметровых троакара были помещены в передне-верхнем отделе подвздошной области билатерально. Процедура началась с тщательного осмотра брюшной полости, поиска возможных метастазов, включая печень и диафрагму. Утероовариальные связки были электрокаутеризованы и разделенны. (ил. 1A, 2A и 2B)
Та же самая процедура была выполнена на мезовариуме.
Рассечение было продолжено до связок тазового дна, обращая особое внимание на то, чтобы оставить ножку сосуда, расположенную в связке неповрежденной. Яичники были мобилизованы на передне-верхний уровень подвздошных гребней. В случае недостаточной мобилизации, расслабляющийся разрез мог быть сделан на брюшине, ниже яичника.
При это технике не возникает необходимости пересечения фаллопиевых труб, т.е. увеличивается вероятность будущей беременности при желании пациента. Яичник был закреплен к брюшине двумя швами нерассасывающейся нитью (ил. 1B и 2C). Нижний край яичника отмечается сосудистыми металлическими кровоостанавливающими клипсами с двух сторон (ил. 1B и 2D), для облегчения их поиска во время процедуры облучения.
ПРОДОЛЖЕНИЕ
Измерение уровня ФСГ производится перед хирургическим вмешательством. Функция яичников оценивается контролем периодичности менструальных циклов пациента и возможными симптомами яичниковой дисфункции.
После операции важно выполнить допплеровское УЗ исследование тазовой области, чтобы гарантировать присутствие кровотока в перемещенных яичниках. Контроль яичниковой функции проверяется измерением ФСГ спустя 30 дней после операции и спустя 30 дней после завершения радиотерапии.
ОБСУЖДЕНИЕ
Появление лапароскопии стало одним из наиболее важных новшеств в современной хирургии и множество процедур, которые ранее требовали лапаротомии, теперь могут быть сделаны минимально инвазивным доступом. Пациенты, подвергающиеся лапароскопической хирургии, нуждаются в более коротком сроке госпитализации, получают меньшие операционные разрезы, испытывают менее интенсивные после операционные боли, более быстрого восстановления и более быстрый возврат к радиотерапии, не усложняя последующую терапия чем пациенты, прошедшие через операцию традиционным брюшным доступом. Лапароскопический подход может применяться при транспозиции яичников.
Сохранения финкции яичников обязательно показано для молодых пациенток в преклимактерическом периоде с гормононезависимыми гинекологическими новообразованиями или негинекологическим раком, требующими облучения тазовой области. Яичники перемещались в разные стороны; по данному вопросу не было достигнуто полного согласия. Обычно они размещались настолько выше и латеральнее насколько это возможно, но яичники могут также быть перемещены саггитально позади матки или в любой отдаленный участок. Другие методы включают защиту яичников с помощью свинцового экрана (это менее эффективно чем латерализация яичников, у тому же этого защищает от облучения угрожаемые лимфоузлы), экстериоризацию яичников под кожей через боковой разрез (эта техника была связанный с формированием кисты яичников), и гетеротопическая яичниковая трансплантация (внедрение яичника к средне-переднюю часть кисти, с формированием сосудистого анастомоза). Согласно Treissman и соавт., подвешивание яичников с пересечением яичниковой связки позволяет адекватно мобилизовать яичники. В некоторых случаях дополнительный расслабляющий разрез брюшины ниже яичника может быть необходим. Эта лапароскопическая техника проста, поскольку нет необходимост диссекции слепой кишки и фаллопиевы трубы могут быть подтянуты на уровень передне-верхней части подвздошных гребней. Латеральная транспозиция яичников лапаротомическим доступом имеет целью сохранение яичниковой функции в 83 % пациентов после облучения тазовой области. Успешное сохранение яичниковой функции зависит от двух факторов: доза радиации полученной яичником и возрастом пациента. В исследовании Huang и соавт., у восьми из четырнадцати пациентов (57.1 %) был яичниковая недостаточность после лапароскопической овариопексии. Среди пациентов, старше 40 лет, у 6 из 7 пациентов (85.7 %) развивалась недостаточность функции яичников после хирургического вмешательства, в то время как среди пациентов в возрасте младше 39 только 1 из 7 пациентов (14,3 %) имел яичниковый дисфункцию. Таким образом, яичниковый отказ случается не только, потому что соответствующие сосуды разрушаются во время процедуры, но также и потому что яичники у пациентов старшего возраста больше чувствительны к химиотерапии и радиотерапии. Возможные осложнения транспозиции яичников перекрут сосудистой ножки, повреждение мочеточника, кровотечение во время операции, формирование функциональной кисты яичника и последующее рецидив на перемещенном яичнике.
В этой рукописи мы описали технику латеральной транспозиции яичника лапароскопическим методом. Помимо вышеупомянутых преимуществ минимально инвазивной процедуры, вмешательство лапароскопическим методом теоретически вызывает меньше спаем по сравнению с лапаротомией, поскольку это простая и миниально инвазивная лапароскопическая техника — золотой стандарт для выполнения латеральной транспозиции яичника.
www.endosurgical.ru
Транспозиция яичников при раке шейки матки в процессе комбинированного лечения
УДК 618.14-006: 618.11
ТРАНСПОЗИЦИЯ ЯИЧНИКОВ ПРИ РАКЕ ШЕЙКИ МАТКИ В ПРОЦЕССЕ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ
Ю.С. СИДОРЕНКО О.Е. ЛЕВЧЕНКО П.А. КРУЗЕ
Фиксация оставленных яичников к круглой маточной связке позволяет сохранить овариальную функцию не только во время лучевой терапии рака шейки матки 1В, благодаря их транспозиции, но и после нее, ввиду сохранения сосудов яичника в физиологическом положении. Этот метод препятствует хирургической и лучевой кастрации.
Ростовский
аучно-исследовательский онкологический институт
Ключевые слова: рак шейки матки, мобилизация сохраненных яичников.
e-mail: rnioi@list.ru
Введение. В настоящее время отмечается рост заболеваемости раком шейки матки среди молодых социально активных женщин (до 35 лет), что составило в последние годы 20% от общего количества заболевших [1,2,3,4]. Наряду с радикализмом лечения онкологических больных преследуется цель повышения качества жизни. Так, при раке шейки матки Ib стадии у репродуктивных женщин, рекомендуемой операцией является расширенная гистерэктомия с сохранением яичников и выведением их из зоны облучения для предотвращения развития посткастрационного синдрома.
К сожалению, после удаления матки функция яичников может страдать ввиду вероятной редукции в них кровотока. Уже давно доказано, что существует 3 типа кровоснабжения яичников. Один подразумевает равномерный приток крови к гонадам из ветви маточной и яичниковой артерии, при другом, питание происходит преимущественно из ветви маточной артерии, а третий характеризует преобладание кровоснабжения из яичниковой артерии [5]. Таким образом, является нецелесообразным использование органосохраняющих операций при третьем типе кровоснабжения, так как при пересечении собственной связки яичника возникает резкое угнетение в нем кровотока, вплоть до полной ишемии яичниковой ткани [6]. В связи с этим необходимо проводить оценку типа кровоснабжения яичников до операции (с помощью изучения ультрасонографиче-ских параметров, таких как скорость кровотока, индекс резистентности), что позволит определить тактику оперативного вмешательства [7], обеспечивающую адекватное кровоснабжение и как следствие, функционирование оставленных желез.
С 2003 года в РНИОИ применяется хирургическая методика мобилизации сохраненных яичников в процессе комбинированного лечения (Сидоренко Ю.С., Неродо Г.А., Крузе П.А., патент № 2254064).
Цель. Сохранить функцию оставленных интраоперационно яичников, применяя модифицированную методику.
Материалы и методы. Данный способ мобилизации сохраненных яичников применялся у 47 женщин репродуктивного возраста больных раком шейки матки Ib стадии (гистотип соответствовал плоскоклеточному раку) с 2003 по 2009 годы. Возрастной промежуток составлял от 20 до 40 лет, большинству больных было от 31 до 35 лет (35%).
Пациенткам проводилось комбинированное лечение, включающее расширенную гистерэктомию с фиксацией сохраненных яичников к круглым маточным связкам и последующим выведением половых желез из зоны облучения при проведении дистанционной гамма-терапии на область удаленной опухоли и зону регионарного метастазирования. Облучение осуществлялось в статическом режиме на аппарате АГАТ-С, с двух диаметральных ромбовидных полей - надлобкового и ягодично-крестцового, размерами 13х13 см (14х14 см). Ежедневное фракционирование разовой дозы составило 2Гр., суммарная очаговая доза варьировала: 40-46 Гр.
Пациенткам, после комбинированного лечения по данной методике, осуществлялась оценка состояния яичников с помощью анкетного опроса, ультразвукового сканирования с допплеро-метрией (с использованием аппаратов ALOKASSD-630 и HDI 1500 /ATL, USA/) до операции, а также после лечения через 3, 12 и 24 месяцев. Особое внимание уделялось определению гормонального статуса радиоиммунологическим методом, включающего изучение динамики гонадотропных и половых гормонов через 12, 24 месяцев.
С целью контроля расположения яичников в брюшной полости при проведении лучевой терапии и для подтверждения их локализации в малом тазу после лечения все яичники интраопе-рационно помечались рентгенконтрастными танталовыми скрепками. С помощью обзорной рентгеноскопии на аппарате PHILIPSBVPULSERA выполнялась визуализация яичников.
Результаты и обсуждение. Операция заключалась в выполнении расширенной гистерэктомии с трубами, выделении тканевого стебля, содержащего сосуды, питающие яичник и максимальной длины круглой маточной связки, из которой формировалось ложе для оставленных яичников. С этой целью круглая маточная связка натягивалась, ее брюшина Т-образно надсекалась и разворачивалась (рис. 1, а). Следующим этапом сохраненный яичник укладывался в подготовленное ложе. Для этого культя собственной связки яичника подшивалась к брюшине круглой маточной связки в дистальной части разреза и помечалась танталовыми скрепками (рис. 1, б).
Танталом д
а) Т- образное рассечение круглой связки
6) Яичник со скрепкой
Рис. 1. Формирование ложа для сохраненного яичника из круглой маточной связки
Далее, несколькими швами, яичник фиксировался к развернутым краям брюшины круглой маточной связки. Аналогичные манипуляции выполнялись на втором яичнике.
На конце круглых маточных связок фиксировались две лигатуры (выведенные на кожу), с помощью которых на втором этапе комбинированного лечения проводилась временная мобилизация яичников из зоны облучения (рис. 2).
Рис. 2. Лигатуры, выведенные на кожу с целью мобилизации
Во время проведения лучевой терапии подтягиванием верхней лигатуры яичники, меченные танталовыми скрепками, выводили из зоны облучения. Их расположение контролировалось рентгенологически (рис.3).
Ромбовидное поле облучения
Рис. 3. Расположение яичников во время сеансов лучевой терапии
После завершения лучевого лечения натягиванием нижней лигатуры, яичники возвращались в малый таз (рис. 4).
Рис. 4. Расположение яичников после лучевой терапии
Таким образом, яичники, оставаясь в ранее созданном ложе, находились в анатомически выгодном положении, имитирующем связочный аппарат половых желез, что способствовало их адекватному кровоснабжению и функционированию (рис. 5).
Фронтальная проекция \ Аксиальная проекция ^
Рис. 5. Общий вид яичников в ложе с лигатурами, создающими мобильность.
В качестве клинической оценки общего состояния больных после лечения использовалась модификация анкеты «Климакс» с вычислением индекса Куппермана. Данная анкета позволяла судить о восстановлении функции яичников у большинства женщин (90%).
При оценке топографического расположения яичников с помощью допплеровского исследования после окончания лучевой терапии, яичники проецировались на область подвздошных сосудов в результате хирургической фиксации к круглым маточным связкам.
На этапах наблюдения размеры яичников незначительно варьировали, оставаясь в пределах нормы, а к концу исследования (через 24 месяца) у всех пациенток размеры половых желез практически не отличались от первоначальных.
При ультрасонографии яичники визуализировались в виде образований овальной формы, средней эхоплотности, однородной структуры без патологических изменений с эхонегативными включениями линейной формы (изображение танталовых скрепок).
Средняя максимальная артериальная скорость в паренхиме яичников составила 8,4б±1,б1 см/сек, что практически не отличалось от скорости кровотока в интактных гонадах (нор-ма-8,12±0,6). Незначительная редукция кровоснабжения в исследуемых яичниках после их мобилизации объяснялась нами лигированием яичниковой ветви маточной артерии.
Несмотря на небольшое снижение скорости стромального кровотока (до 77%) по отношению к исходным значениям, цветовое допплеровское картирование отобразило наличие цветовых локусов не только в центре, но и по периферии яичника, что подтверждает адекватность кровоснабжения и способствует поддержанию гормонопродуцирующей функции гонад.
Выводы. Наосновании проведенных нами исследований, установлено, что применение данной методики по мобилизации сохраненных яичников в процессе комбинированного лечения позволяет не только предупредить лучевую кастрацию гонад, но и сохранить полноценное их функционирование.
Литература
1. Козаченко, В.П. Рак шейки матки / / Современная онкология. - 2001. - Т.2. - №2. - С. 2-4.
2. Урманчеева,А.Ф. Заместительная гормонотерапия и злокачественные опухоли // Журнал акушерства и женских болезней / А.Ф. Урманчеева, М.М. Бурнина. - СПб. - 2001. - Вып. 1. - Т. ХПХ. - С 58-62.
3. Чиссов, В.И., Старинский, В.В., Петрова, Г.В. Злокачественные новообразования в России в 2008 году. М.: МНИОИ им. Герцена. 2010. 256 с.
4. Гусейнов ,К.Д. Оценка эффективности использования лекарственной терапии в комбинированном лечении больных раком шейки матки 1Ъ2-Ш стадий: автореф. дис. ... канд. мед. наук. С-Пб, 2003. 20 с.
5. Федотова, Т.А. Хирургическая методика, направленная на физиологическое сохранение яичников у пациенток молодого возраста с ранней онкологической и неопухолевой патологией гениталий: дис. ... канд. мед. наук. Ростов-на-Дону, 2001. 180 с.
6. Олейникова, Т.Ф. Аспекты опухолевой трансформации яичников, сохраненных после удаления матки: дис. ... канд. мед. наук. Ростов-на-Дону, 2006. 177 с.
7. Яценко, Н. В. Прогностические факторы развития рака яичника после гистерэктомии у женщин репродуктивного возраста: дис. . канд. мед. наук. Ростов-на-Дону, 2006. 142 с.
TRANSPOSITION OF THE PRESERVED OVARIES DURING COMBINED TREATMENT FOR CERVICAL CANCER
Fixation of the preserved ovaries to uterine round ligament allow to retain ovarian function, not only during postoperative radiotherapy of stage IB cervical cancer due to their transposition, but also after completing pelvic radiation because of preserved ovarian blood vessels in physiological place. This method prevents surgical and radiologic castration.
Key words: cervical cancer, mobilization of the preserved ovaries.
Y.S. SIDORENKO N.E. LEVCHENKO P.A. KRUZE
Rostov Cancer Research Institute Ministry of Health Service end Social Development, Rostov-on-Don, Russia
e-mail: rnioi@list.ru
cyberleninka.ru
Транспозиция яичников у больных раком шейки матки молодого возраста
кровоизлияний, вызванные эррозией сосудов, приводившей к образованию в центральной части опухолей полости, заполненной геморрагическим содержимым и некротическими массами. При выраженном торможении под влиянием РИ значительно увеличивалась толщина капсулы (до 300 мкм). Обращало на себя внимание обилие цитоплазмы в опухолевых клетках, а также накопление коллагеновых волокон в межклеточных пространствах (подтверждено окраской по Ван-Гизону), что привело к их значительному увеличению. Митозы практически не встречались. Кровоизлияния и некрозы наблюдались редко и на небольших участках. Морфометри-
ческие исследования показали, что в тканях опухоли животных опытной группы значительно снижались площадь, занятая клетками опухоли, в 1,6 раза, плотность их расположения -в 1,9 раза, число фигур митозов - в 1,5 раза. размеры участков некроза и кровоизлияний - в 3 раза. Одновременно площадь нормальной соединительной ткани увеличилась в 32 раза по сравнению с контролем.
Вывод. Применение микроволнового резонансного излучения по алгоритмам активационной терапии позволило добиться торможения роста саркомы 45 более чем на 80% у половины подопытных животных.
ТРАНСПОЗИЦИЯ ЯИЧНИКОВ У БОЛЬНЫХ РАКОМ шейки матки молодого возраста
А.В. ТАРХОВ, С.Э. КРАСИЛЬНИКОВ, А.В. ГЕРАСИМОВ, Е.В. БАБАЯНЦ, Н.А. АФАНАСЬЕВА, А.П. КУЛИДЖАНЯН, В.Г СИСАКЯН
ГБУЗ НСО «Новосибирский областной онкологический диспансер»
Актуальность. Рак шейки матки является одним из наиболее распространенных злокачественных новообразований у женщин. Несмотря на достигнутые в последние десятилетия успехи в лечении опухолей данной локализации, отмечается неуклонный рост заболеваемости, особенно среди молодых женщин в возрасте до 40 лет. Выявление инвазивного рака шейки матки требует незамедлительного противоопухолевого лечения, которое редко ограничивается только хирургическим этапом, а является, как правило, комбинированным или комплексным. Поэтому после оперативного этапа часто проводится лучевое, а возможно, и лекарственное лечение.
Цель исследования - поиск способов сохранения гормональной активности яичников, а следовательно, и обеспечения качества жизни пациентки и в некоторых случаях возможности реализации репродуктивной функции в будущем.
Материал и методы. Одним из методов сохранения функции яичников является их перемещение из области облучения - транспозиция. Отличительной особенностью расширенной экстирпации матки с транспозицией яичников является сохранение придатков матки (яичника
и маточной трубы) и их сосудисто-нервных связей, расположенных в воронко-тазовой связке. В результате транспозиции яичники перемещаются на питающей «ножке» в верхний этаж брюшной полости. При этом достигается их выведение из зоны послеоперационного облучения и предупреждение лучевой кастрации. В гинекологическом отделении Новосибирского областного онкологического диспансера транспозиция яичников при лечении больных раком шейки матки молодого возраста проводится с 2001 г. 32 пациенткам в ходе операции Вертгей-ма выполнена транспозиция одного или обоих яичников.
Результаты. Наблюдение за пациентками, которым выполнена транспозиция яичников, показало несомненные достоинства данного метода, заключающиеся в отсутствии явлений посткастрационного синдрома у оперированных больных, а следовательно, более легком течении послеоперационного периода, лучшей переносимости последующей противоопухолевой терапии. Выполнение транспозиции яичников, по результатам наших наблюдений, не приводит к значительному увеличению послеоперационных осложнений. У 1 больной транспозиция
для больных, которым на первом этапе лечения планируется лучевая терапия.
Выводы. Транспозиция яичников в ходе лечения рака шейки матки у женщин молодого возраста действительно позволяет улучшить качество жизни пациенток, сократить сроки социальной и психологической реабилитации.
яичников осложнилась развитием острого гнойного сальпингоофорита, что потребовало повторной операции. Одна пациентка умерла вследствие прогрессирования заболевания и развития уремии. Случаев метастатического поражения перемещенных яичников в нашей практике не было. В настоящее время в отделении внедряется лапароскопический доступ
определение цитокинов у больных, страдающих РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ, ДЛЯ ДИАГНОСТИКИ ЭНДОТОКСИКОЗА ДО И ПОСЛЕ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ
О.А. ТКАЧУК, В.Е. ВОЙЦИЦКИЙ, Ю.Э. НАРОВ, М.С. ЛЮБАРСКИЙ, Д.В. ХАБАРОВ
НГМУ, кафедра онкологии, г. Новосибирск НИИКиЭЛ СО РАМН, г. Новосибирск
Актуальность. В структуре онкологической патологии в России рак молочной железы (РМЖ) занимает первое место, заболеваемость РМЖ составляет 38,53 на 100000, а смертность - 24 тыс. женщин в год. Сегодня под наблюдением онкологов состоят 500 тыс. пациенток, страдающих РМЖ. Основной составляющей комплексного лечения РМЖ остается хирургический метод, но ближайшие послеоперационные осложнения удлиняют период восстановления после вмешательства, требуют значительного перенапряжения иммунитета и в результате истощают его, отдаляя тем самым сроки проведения адъювантной лучевой и химиотерапии. По литературным данным, про-воспалительные цитокины - интерлейкин- 1р (ИЛ-1Р), интерлейкин-2 (ИЛ-2), интерлейкин-8 (ИЛ-8) и интерлейкин-6 (ИЛ-6) принимают непосредственное участие в патогенезе анорексии, кахексии, являются чувствительными маркерами инфекционного эндотоксикоза и системной воспалительной реакции. Определение ИЛ-6 в настоящее время начинает использоваться для ежедневного мониторинга этих процессов.
Цель исследования - определение уровня ИЛ-1Р, ИЛ-2, ИЛ-8 и ИЛ-6 у больных РМЖ в пред- и послеоперационном периодах.
Материал и методы. Исследовали три группы женщин с РМЖ после радикальных операций на молочной железе - первая груп-
па получала стандартное антибактериальное, анальгетическое послеоперационное лечение; вторая группа - детоксикационное лечение и лимфотропное введение антибиотиков и анальгетиков; в третьей группе вводились препараты для коррекции вторичного иммунодефицита, разрешенные для применения в онкологии, а также анальгетики и антибиотики - лимфотроп-но. Во время научного исследования цитокино-вого профиля крови у 95 пациенток с РМЖ было проведено определение концентрации четырех провоспалительных цитокинов - ИЛ-1Р, ИЛ-2, ИЛ-8 и ИЛ-6. Определение концентрации интерлейкинов в сыворотке крови выполняли с использованием тест-систем РгоСоп IL1-beta, РгоСоп ^6, РгоСоп ^2, РгоСоп ^8 производства ООО «Цитокин» (С.-Петербург) по инструкции производителя. Результаты им-муноферментного анализа регистрировали на вертикальном фотометре Multiskan МСС 340 в при длине волны 492 нм.
Результаты. У пациенток третьей группы, где проводилась коррекция вторичного иммунодефицита в раннем послеоперационном периоде, динамика снижения уровня провос-палительных цитокинов в сыворотке крови была статистически значимой - уровень ИЛ- 1р у них снизился на 29,1 %; ИЛ-2 - на 31,1%, ИЛ-8 - на 32,4%, а содержание ИЛ-6 - на 35,3 % по отношению к исходному (до операции). Это до-
cyberleninka.ru