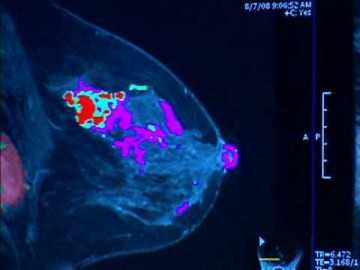
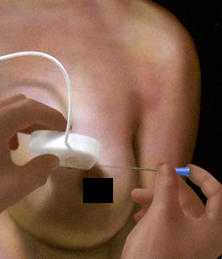
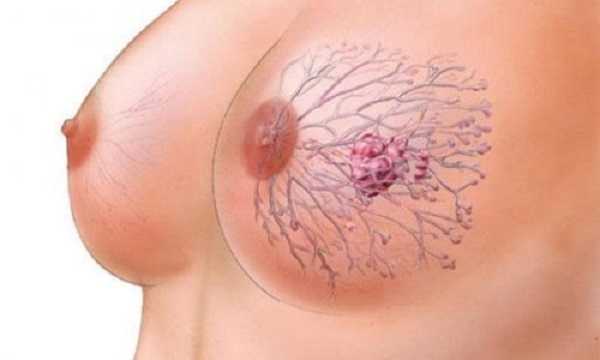
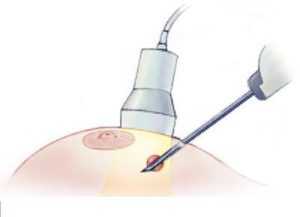
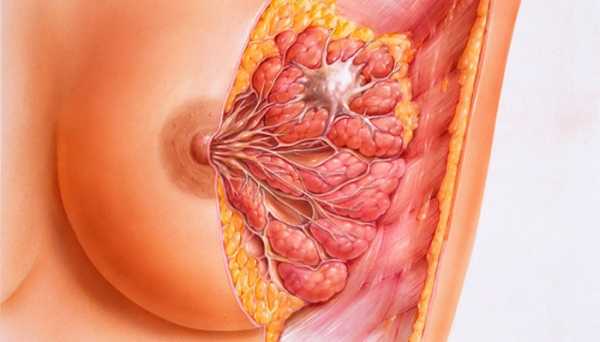
Патогенез рака молочной железы
67. Рак молочной железы. Эпидемиология. Этиология. Патогенез. Клиника.
Рак молочной железы — злокачественное новообразование, развивающееся из клеток эпителия протоков и/или долек паренхимы железы.
Эпид-я. РМЖ на 1 месте в структуре онкологической заболеваемости женщин. На 2 месте в мире. На 5 месте в Бел. Самые высокие показатели - в США.Самую низкую заболеваемость регистрируютв странах Африки.Заболеваемость РМЖ увеличивается с возрастом,начиная с 40 и достигая пика в 60-65 лет. Для женщин 70 лет ежегодный риск заболевания РМЖ в 3 раза выше, чем для женщин в возрасте 40 лет, а ежегодный риск смерти от РМЖ в 5 раз выше, чем для женщин 40 лет.
Этиол-я. Доказана наследственнаяая предрасположенность к РМЖ. Исходя из этого, выделяют:
• спорадический рак (около 68%); нет случаев рака молочной железы у обоих родителей в 2 поколениях;
• семейный РМЖ (около 23%).Случаи РМЖ у одного или нескольких кровных родственников;
• генетическое предрасположение к раку в результате наличия мутаций генов BRCA1/BRCA2 (около 9%). Отмечают случаи РМЖ у кровных родственников, а также ассоциированный рак (первичная множественность — поражение яичников, толстой кишки).
Группы риска по раку молочной железы зависят от следующих этиологических факторов:
1. Гормональные факторы:
а) эндогенные - гиперэстрогенемия в результате:
- особенностей менструального цикла (раннее менархе до 12 лет; поздняя менопауза после 55 лет)
- детородной функции (нерожавшие, 1-ые роды после 30 лет; аборты до 18 лет и после 30 лет)
- особенностей лактации (гипо- и агалактия)
- особенностей половой жизни (ее отсутствие, позднее начало, фригидность, механические способы контрацепции)
б) экзогенные:
- заместительная терапия гормонами в пред- и постменопаузе сроком более 5 лет.
- длительный прием комбинированных оральных контрацептивов: более 4 лет до первых родов, более 15 лет в любом возрасте.
2. Факторы образа жизни и окружающей среды
- географическое расположение и питание (высококалорийная диета, избыточное потребление животных жиров, малая физическая активность)
- злоупотребление алкоголя (увеличивают риск на 30%)
- курение (до 16 лет – увеличивает риск в 2 раза)
- стресс
- радиация (облучение) и травмы молочных желез
3. эндокринно-метаболические нарушения: ожирение, атеросклероз, заболевания надпочечников и щитовидной железы
4. индивидуальный анамнез:
- возраст старше 40 лет
- ранее перенесенный рак молочной железы или рак яичников
5. Предшествующие заболевания молочных желез
- атипическая гиперплазия молочных желез
- пролиферирующие заболевания
6. Семейный анамнез: генетические факторы:
- наличие у ближайших родственников рака молочной железы, рака яичника, колоректального рака
- связь с наследственными синдромами (Cowden, BLOOM)
- мутации генов BRCA-1; BRCA-2
Патогенез. Вследствие воздействия факторов – активация пролиферативных процессов, акт-я продукции ФСГ- увелич. фолликула – увелич. эстрогены – пролиферация слизистой матки, эпителия протоков железы.
Факторы защиты: ранняя беременность, первый ребёнок мальчик, долг. вскармливание.
Клинические проявления РМЖ.
Первичные симптомы:
1) безболезненное плотное образование различных размеров, округлой или неправильной формы, с бугристой поверхностью, незначительным ограничением подвижности (если не прорастает в грудную стенку). Молочная железа часто деформирована (увеличена или уменьшена, имеет локальное выбухание, срезанный контур).
2) кожные симптомы: а) симптом морщинистости – кожу над опухолью указательным и большим пальцами собирают в широкую складку, появляющиеся при этом морщинки в норме расположены параллельно; при раке параллелизм морщинок нарушается, они конвергируют к одному участку (положительный симптом «морщинистости»)
б) симптом площадки – при приеме, аналогичном предыдущему, появляется уплощенный участок фиксированной кожи
в) симптом втяжения (умбиликации) – при приеме, аналогичном предыдущему, появляется легкое втяжение
г) симптом лимонной корки – лимфатический отёк кожи, виден визуально
д) утолщенная складка ареолы (симптом Краузе)
е) изменение цвета кожи над опухолью
ж) раковая язва – не глубокая, плотнее окружающих тканей, имеет подрытые, выступающие над поверхностью кожи края и неровное дно, покрытое грязноватым налетом
3) симптомы со стороны соска: изменения формы и положения соска, втяжения соска и ограничение его подвижности вплоть до полной фиксации (симптом Прибрама – смещение опухоли вместе с соском – результат прорастания опухолью выводных протоков железы), геморрагическое отделяемое из соска
4)Увеличение подмышечных лимфоузлов.
5) Изолированный отёк.
6) Невралгия.
Вторичные симптомы: изьязвление кожи, кровотечения, присоединение вторичной инфекции, метастазы в кости (позвоночника, таза, бедро, рёбра), метастазы в печень, лёгкие, плевру.
Физикальное обследование: ассиметричность, увеличение в объёме, различные уровни сосков, выделения из сосков, изменения кожи, пальпация стоя и лёжа, симптомы см. выше.
Осмотр. Осмотр молочных желез следует проводить при достаточном освещении, на некотором расстоянии от пациентки, стоящей сначала с опущенными руками, а затем — с поднятыми кверху.
Осмотр позволяет выявить локальную или тотальную гиперемию кожи молочной железы; гиперемия может распространяться на кожу грудной или брюшной стенки, верхнюю конечность. В большинстве случаев сочетается с локальным или тотальным отеком молочной железы, который обозначается как симптом «лимонной корки». Наличие изъязвлений кожи, узелковых уплотнений, корочек, свищей, распада тканей также присущи опухолевому процессу. При пальпации исследуют:
1) размеры (диаметр) — принято отмечать до 1 см, до 2 см, от 2 до 5 см, свыше 5 см; измерения обычно производят с помощью линейки или циркуля;
2) анатомическая форма — узловатая, местно-распространенная, или локально-инфильтративная, диффузно-инфильтративная (занимающая либо большую часть, либо всю молочную железу);
3) консистенция — плотная, плотноэластическая, бугристая;
4) локализация — центральная, наружные квадранты (верхний и нижний), внутренние квадранты (верхний и нижний).
При пальпации регионарных л. у. в подмышечной, подключичной и надключичной зонах важно установить:
а) отсутствие уплотненных и увеличенных л.у.;
б) наличие увеличенных или уплотненных л.у.;
в) расположение увеличенных л.у. в виде цепочки или конгломерата спаянных между собой узлов;
г) наличие или отсутствие отека верхней конечности.
Совокупность анамнестических сведений, данных осмотра и пальпации является условием определения клинической формы РМЖ: узловатой, местной инфильтративной, диффузной инфильтративной или осложненных (инфильтративно-отечной, инфильтративно-лимфангитической, язвенной).
Отдельно рассматривается так называемая «оккультная» форма РМЖ, для которой характерно сочетание микроскопической первичной опухоли с крупными метастатическими поражениями регионарных лимфатических узлов, чаще подмышечных.
Особый интерес представляет рак Педжета — своеобразная форма РМЖ, поражающая сосок и ареолу. По преобладанию тех или иных клинических симптомов при раке Педжета различают экземоподобную (узелковые, мокнущие высыпания на коже ареолы), псориазоподобную (наличие чешуек и бляшек в области соска и ареолы), язвенную (кратероподобная язва с плотными краями) и опухолевую (наличие опухолевидных образований в субареолярной зоне или в области соска) формы.
studfiles.net
Причины и механизм развития рака молочной железы
Рак груди занимает первое место по заболеваемости среди всех «женских» раков во всем мире (без учета рака кожи). Выделяют несколько этиологических факторов, участвующих в патогенезе заболевания. К ним относят: возраст, наследственность, питание, алкоголь, ожирение, образ жизни, отсутствие физической активности, а также эндокринные факторы (эндогенные и экзогенные).
Уплотнения в груди, выявленные при маммографическом исследовании, и ранее перенесенные доброкачественные заболевания грудной железы также рассматриваются как одни из причин возникновения заболевания. Однако до сих пор выяснить четкую зависимость и причинно-следственные связи в патогенезе рака молочной железы довольно тяжело.
Эпидемиология
Заболеваемость выше в странах западного мира по сравнению со странами Африки, Южной Америки и Азии. Считается, что каждая десятая англичанка в течение жизни столкнется с этим заболеванием. На него приходится четверть всех «женских» раков Англии и США.
Общая патофизиология (патогенез) рака
Организм человека состоит из нескольких триллионов клеток. Клеточный цикл — рост, созревание, деление и смерть этих клеток — находится под строгим контролем. В детском организме деление клеток ускоренно, что позволяет ему расти. В зрелом возрасте они делятся, чтобы заменить изношенные или повреждённые клетки. Клеточное деление и рост контролируется ДНК (дезоксирибонуклеиновая кислота) или, точнее, генами, которые расположены в ядре клетки.
Рак возникает, когда клетки определенного участка тела организма начинают бесконтрольно делиться. Все типы раков, вне зависимости от их происхождения, возникают в результате нарушения клеточного деления, что приводит к появлению опухолей.
Помимо этого раковые клетки приобретают некоторые «жульнические» свойства:
- Их продолжительность жизни увеличивается, и вместо того, чтобы умереть, они продолжают расти и делиться, способствуя появлению новых ненормальных клеток.
- Они приобретают способность проникать в другие ткани — то, что здоровые клетки не делают. Это свойство называется метастазирование.
- Они требует новую сеть кровеносных сосудов, чтобы удовлетворить их потребность в питательных веществах. Процесс образования новых сосудов называется ангиогенез, который является уникальным для раковой опухоли.
Что заставляет нормальную клетку стать раковой?
Нормальная клетка может стать раковой, если в ее ДНК возникнут повреждения в результате какого-либо воздействия. Так как ДНК регулирует клеточный цикл (рост, функционирование и смерть клетки), любые повреждения в ней приведут к изменениям этого цикла.
Большинство нормальных клеток, если у них возникает повреждение в ДНК, либо занимаются его «ремонтом», либо умирают. В раковых клетках повреждения ДНК не ремонтируются, а передаются появившимся в результате деления новым ненормальным клеткам, которые рождаются изначально уже раковыми.
Патофизиология рака груди
Раковая опухоль возникает из нормальных клеток этого органа. Существует множество причин (этиологических факторов), которые повышают риск развития заболевания. Повреждения ДНК, возникшие в результате воздействия эстрогена и приводящие к развитию рака этого органа, были доказаны экспериментально. Некоторые люди наследуют дефекты в ДНК (генах BRCA1, BRCA2 и P53), с которыми связывают возникновение рака.
Иммунная система человека отслеживает раковые клетки (с поврежденной ДНК) и уничтожает их. Если она теряет способность выявить раковую клетку, выполнить свою защитную функцию — это приводит к возникновению опухоли.
Этиология рака молочной железы является многофакторной: одновременно в процессе участвуют несколько причин, которые могут действовать независимо друг от друга или взаимодействовать между собой. Ниже приведены этиологические (причинные) факторы, с которыми связывают появление рака молочной железы.
Этиологические факторы
География
На страны запада приходится более половины случаев рака молочной железы: 200 тыс. случаев на США и 320 тыс. на Европу. На долю этого рака приходится 3–5% всех смертей в западном мире, 1–3% в развивающихся странах. В Японии заболеваемость одна из самых низких. По последним данным, смертность в США составляет 2,3% и постоянно снижается, что связывают с улучшением методов скрининга (мероприятий, направленных на раннее выявление рака), а также с появлением новых вариантов лечения.
Возраст
Рак груди в возрасте до 25 лет практически не встречается. С возрастом заболеваемость постепенно растет. На 100 тыс. женщин в возрасте до 25 лет приходится менее 10 новых случаев, а к 45 годам этот показатель увеличивается в 100 раз. Это подтверждает тот факт, что женские половые гормоны участвуют в патогенезе рака. Другие злокачественные заболевания не имеют такой четкой корреляции с женским репродуктивным периодом.
Генетические факторы
Большое количество исследований показали, что 12% женщин с диагностированным раком груди имеют близкого родственника, страдающего этим недугом, а у 1% пациенток их может быть несколько.
Хотя подавляющее число раков молочной железы не наследуется, существуют гены, мутации в которых повышают вероятность развития заболевания. К ним относят гены BRCA1 и BRCA2, мутации в которых могут передаться от родителей к ребенку. Существуют и другие гены, которые связывают с раком груди (P53, P65 и ATM). Женщинам, у которых два или более близких родственников (мать и сестра, мать и дочь) имеют диагноз рак молочной железы, показан генетический скрининг, чтобы обнаружить мутации в этих генах до развития заболевания. При выявлении этих специфических мутаций женщине рекомендуют либо проходить регулярное профилактическое наблюдение, либо профилактическую двухстороннюю мастэктомию (при некоторых мутациях вероятность развития рака к 40 годам приближается к 80%).
Рекомендуем прочесть статью об определении онкомаркеров молочной железы. Как анализ на онкомаркеры используют в диагностике предрасположенности к раку груди, как проводится анализ, какие онкомаркеры важны в маммологии вы сможете подробнее прочесть в этой статье.Диета и алкоголь
Диета и алкоголь, как полагают, играют определенную роль в этиологии и патогенезе рака молочной железы. Существует четкая связь между фитоэстрогенами, а также злоупотреблением алкоголем и этим заболеванием. Согласно последних данных, риск заболеть возрастает прогрессивно дозе приема алкоголя, а также крепости напитка. Так, каждый 10 г прироста в ежедневном потребление спирта увеличивает риск на 9%.
Диеты с большим содержанием животных жиров способствуют появлению рака. Это происходит потому, что они богаты холестерином, являющимся предшественником в синтезе эстрогенов и других стероидных гормонов, которые стимулируют развитие рака.
Доказано, что клетчатка препятствует всасыванию кишечником эстрогена. Вероятно поэтому рак молочной железы не так часто встречается в развивающихся странах (Африке, Азии и Южной Америке), чем в западном мире. Соевые бобы и витамины также рассматривают как факторы диеты, которые уменьшают частоту этого заболевания.
Ожирение, образ жизни и физическая активность
Наряду с диетой физические упражнения могут снижать плазменные уровни гормонов. Замечено, что эти два фактора по отдельности или в комбинации, влияющие на массу тела у женщин в менопаузе, способны снижать риск развития рака. Каждые 5 кг лишнего веса повышают риск возникновения заболевания на 8%. Это объясняется тем, что жировая ткань является важным источником эстрогена, которые синтезируются из холестерина.
Эндокринные факторы
Эндогенные
Рак молочной железы чаще встречается у нерожавших женщин и у тех, кто не кормил ребенка грудью. Было установлено, что ранняя доношенная беременность, особенно если она сочетается с поздним менархе и ранней менопаузой, которые уменьшают продолжительность воздействия эстрогена, уменьшают риск развития этого рака. У женщины, имеющей трех и более детей, риск меньше в два раза, чем у той, которая бездетна. Это связывают с низким уровнем эстрогена во время беременности, соответственно, у многодетных женщин влияния эстрогена на железу меньше, чем у нерожавшей.
Экзогенные факторы
Гормон-заместительную терапию (ГЗТ) рассматривают как фактор, повышающий риск развития рака, особенно среди женщин, использующих эстроген и прогестерон в течение 5 лет и дольше. Тем не менее, ГЗТ имеет много преимуществ, таких как:
- облегчение сухости влагалища,
- зуд,
- снижение интенсивности головной боли,
- уменьшение перепадов настроения и депрессии,
- снижение риска развития остеопороза и патологических переломов.
Поэтому среди врачей ведется дискуссия, что должно превалировать в процессе принятия решения при назначении ГЗТ — вышеперечисленные преимущества или ее роль при раке молочной железы.
Тоже самое можно отнести и к оральным контрацептивам. С ними связывают незначительное увеличение риска рака молочной железы. Риск, как полагают, больше у тех, кто начал контрацепцию ранее 20-летнего возраста.
По аналогии с ГЗТ, важно отметить очевидные преимущества оральных контрацептивов в предотвращении нежелательной и несвоевременной беременности как метода планирования семьи, которые превалируют над незначительным увеличением риска рака груди.
Повышение плотности ткани
Это хорошо задокументированный фактор риска, наблюдаемый у женщин как во время репродуктивного возраста, так и после его завершения. Исследования показали, что женщины с > 75% увеличенной плотностью груди, выявленной при маммографии, имеют 5-кратное увеличение риска по сравнению с теми, у которых она составляет < 5%.
Доброкачественные заболевания
Наличие в анамнезе женщины таких доброкачественных заболеваний груди, как фиброзно-кистозной болезни (фиброаденоматоза) и фиброаденомы, увеличивает риск развития рака. Фиброаденоматоз с тяжелой дисплазией считается предраком, хотя и не всегда переходит в рак. Поэтому женщинам с этими заболеваниями необходимо тщательное наблюдение и скрининг (совокупность мероприятий, которые позволяют диагностировать рак груди на начальных стадиях). Это позволяет улучшить результаты лечения.
grudinfo.ru
Материалы конгрессов и конференций
МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
Е.Н. Имянитов ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, Санкт-Петербург
В развитых странах рак молочной железы (РМЖ) возникает у 1 из 10 женщин. Главной причиной роста заболеваемости РМЖ является заметное увеличение доли людей, достигающих пожилого возраста. Действительно, несмотря на относительно частую встречаемость РМЖ у молодых женщин, риск данного заболевания после 65 лет в 150 раз превышает таковой у лиц моложе 30 лет. Хотя известно несколько десятков факторов риска РМЖ, их можно условно разделить на две категории:
1) поведенческие или наследственные особенности, ассоциированные с гиперэстрогенией;
2) наследственная неполноценность систем обеспечения целостности генома [Singletary, 2003].
Женщины с такими врождёнными характеристиками как раннее начало менструаций и/или позднее наступление менопаузы подвергаются увеличенной эстрогенной нагрузке. Гиперэстрогении способствуют также особенности современного стиля жизни, в частности поздние роды, непродолжительное грудное вскармливание, переедание, низкая физическая активность и т.д. Примечательно, что эстрогены не только оказывают гиперпролиферативное воздействие на эпителий молочной железы, но могут выступать и в роли мутагенов, непосредственно воздействуя на структуру ДНК [Clemons and Goss, 2001; Singletary, 2003].
Наиболее привычным примером генетических дефектов, вызывающих неполноценность систем обеспечения целостности генома, являются РМЖ-ассоциированные зародышевые мутации в генах BRCA1, BRCA2, ATM, p53, CHEK2 и NBS1. Примечательно, что воспроизводимая взаимосвязь между риском РМЖ и хромосомной нестабильностью выявляется также посредством разнообразных фенотипических тестов [Imyanitov et al., 2004].
Развитие РМЖ реализуется через накопление разнообразных соматических мутаций. Наиболее характерны для РМЖ количественные хромосомные аномалии и нарушения метилирования промоторов антионкогенов. Другие типы соматических событий, в частности небольшие внутригенные повреждения, изменения длины микросателлитных повторов и т.д. встречаются в РМЖ относительно редко [Lerebours and Lidereau, 2002].
Знания о молекулярном патогенезе РМЖ позволили разработать новые подходы к лечению этого заболевания. В качестве наиболее наглядных примеров можно привести прогресс в области применения различных антагонистов эстрогенового каскада, а также использование моноклональных антител к онкобелку HER2 [Esteva et al., 2001].
Работа выполнена при поддержке грантов Минпромнауки России (раздел «Медицина», тема № 29 «Разработка технологий диагностики и лечения злокачественных новообразований») и Правительства Москвы (проект 15/04-Ген-М).
Список литературы:
1. Clemons M., Goss P. Estrogen and the risk of breast cancer. N. Engl. J. Med., 2001, 344, 276-285.
2. Esteva F.J., Valero V., Pusztai L., Boehnke-Michaud L., Buzdar A.U., Hortobagyi G.N. Chemotherapy of metastatic breast cancer: what to expect in 2001 and beyond. Oncologist, 2001, 6, 133-146.
3. Imyanitov E.N., Togo A.V., Hanson K.P. Searching for cancer-associated gene polymorphisms: promises and obstacles. Cancer Lett., 2004, 204, 3-14.
4. Lerebours F, Lidereau R. Molecular alterations in sporadic breast cancer. Crit. Rev. Oncol. Hematol., 2002, 44, 121-141.
5. Singletary S.E. Rating the risk factors for breast cancer. Ann. Surg., 2003, 237, 474-482.
rosoncoweb.ru
Этиология и патогенез рака молочной железы

Генетические, эпидемиологические, и лабораторные исследования подтверждают стохастическую модель развития рака молочной железы, в котором ряд генетических изменений способствуют динамическому процессу, известному как карциногенез.
Накопление генетических изменений, как полагают исследователи, соответствует изменениям фенотипа, связанным с озлокачествлением.
Последовательность карциногенеза рассматривается гистологически как появление изменений в нормальной ткани, которые в конечном счете приводят к гиперплазии и нарушению роста нормальной ткани.Самые серьезные их формы трудно отличить от карциномы из situ.
В пользу концепции о том, что рак молочной железы можно предотвратить, свидетельствуют широкие изменения показателей частоты случаев возникновения рака молочной железы, которые являются индикатором того, что некоторые переменные – экологические, социальные, поведенческие – влияют на частоту возникновения случаев рака молочной железы.
Исследования миграций подтверждают этот факт: что у японских эмигрантов в США увеличивается риск развития рака молочной железы – от частоты, характерной для Японии, до частоты, характерной для США в пределах двух поколений.
Эндогенные эстрогены
Многие из факторов риска для рака молочной железы, включая возраст наступления менархе, первых родов и менопаузы, предполагают влияние гормональных изменений на развитие болезни. Эстроген и прогестин вызывают рост и пролиферацию клеток молочной железы, по видимому, из-з факторов роста, таких как преобразующий фактор роста (ПФР – альфа).
Женщины, у которых развивается рак молочной железы, имеют тенденцию к более высоким уровням эндогенного эстрогена и андрогенов. Удаление одного яичника также уменьшает риск развития рака молочной железы, но в меньшей степени, чем удаление обоих яичников.
Другие гормональные изменения также влияют на риск развития рака молочной железы. Увеличение рождаемости сопровождается увеличением риска в переходном периоде, и затем – долгосрочным сокращением риска; эта зависимость более характерна для женщин младшего возраста. Возраст наступления менархе также коррелирует с риском развития рака молочной железы.
Женщины с возрастом наступления менархе в 11 лет или ранее, имеют на 20 % больше риск развития рака молочной железы, чем женщины с возрастом наступления менархе в 14 лет или старше. Женщины, с поздним наступлением менопаузы также имеют увеличенный риск развития рака молочной железы.
Репродуктивные факторы риска могут взаимодействовать с большим количеством генетическим факторов. Кормление грудью связано с уменьшением риска развития рака молочной железы.
Многие исследования предполагают, что эндогенный эстроген и уровни андрогена выше у тех женщин, у которых развивается рак молочной железы. Уменьшить уровень эндогенного эстрогена можно путем поддержания идеальной массы тела, соблюдением диеты с низким содержанием жиров в периоде после менопаузы, и регулярными физическими упражнениями у подростков. Уменьшат ли такие меры, риск возникновения рака молочной железы у таких женщин, покажут только будущие исследования.
Генетические мутации
Унаследованный генетический профиль человека влияет на восприимчивость к мутагенам и факторам роста, которые «запускают» канцерогенный процесс. Пациенты с некоторыми генетическими синдромами, связанные с определенными изменениями в аллелях, составляют приблизительно 5 % от всех случаев диагностированного рака молочной железы.
Идентификация генов – факторов риска – обеспечивает понимание этиологии рака молочной железы и позволяет выработать профилактические мерыдля групп риска. У женщин, которые наследуют мутацию в BRCA1 или BRCA2, пожизненный риск развития рака молочной железы, яичников и прямой кишки увеличивается вдвое.
Мутации BRCA2 менее распространены чем мутации BRCA1; при этом мутации BRCA2 также связаны с повышенным риском возникновения рака молочной железы у мужчин, рака простаты, рака поджелудочной железы. Женщины – носительницы гена атаксии-телеангиэктазии (В), также имеют повышенный риск развития рака молочной железы
Другие Факторы Риска
Дополнительные факторы риска включают семейную историю возникновения рака груди или рака яичников в нескольких поколениях (родственники, особенно первой линии, как по стороне матери ,так и по стороне отца); ранний возраст наступления менархе и поздний возраст первых родов; наличие доброкачественных опухолей грудной железы, подтвержденных данными биопсий.
Шкала Гейла оценивает индивидуальный риск, основанный на этих факторах, для женщин в возрасте 40 лет или старше, регулярно проходящих маммографию.
Для женщин, имеющих в анамнезе диагностированный агрессивный рак молочной железы, протоковую карциному in situ или дольковую карциному in situ, риск развития новой опухоли молочной железы на 0.6 % выше ,с ежегодным повышением .
Для женщин ,проходивших облучение торакального отдела, особенно в возрасте до 30 лет, риск развития опухоли молочной железы на 1 % выше, начиная с периода спустя 10 лет после облучения .
Высокая плотность молочных желез – существенный фактор риска для развития рака молочной железы. Она также вызывает сушественные сложности в интерпретации маммограмм. Риск ложноотрицательных результатов маммографии возрастает в 3-6 раз для таких женщин.
Поведенческие факторы, такие как заместительная гормональная терапия в менопаузе, ожирение и потребление алкоголя связаны с увеличением риска развития рака молочной железы.
Риск развития рака молочной железы и риск смертности от него также зависит от географических, культурных, социальных факторов, этнической принадлежности пр.
Симптомы со стороны молочной железы могут указывать на диагноз рака молочной железы. Рак был диагностирован у 6.2 % пациенток с такими симптомами, у большинства из них – на стадии II или III. Из женщин, испытывающих симптомы со стороны молочной железы, требующих обращения за медицинской помощью, наиболее вероятно, у 10.7 % будет диагностирован рак. Диагноз ставится на основании результатов следующих обследований:
Американское общество по борьбе с раком и Американский Национальный Институт Рака
www.likar.info