Миома матки классификация
миома матки
миома матки. Клиника, диагностика, лечение.
67.Интерстициальная миома матки. Клиника, диагностика, лечение.
68.Клиника и лечение рождающегося субмукозного миоматозного узла.
69.Консервативные методы лечения миомы матки.
70.Оперативные методы лечения миомы матки. Показания.
Лейомиома (миома) матки – ограниченная доброкачественная опухоль, состоящая из гладкомышечных клеток и фиброзных соединительнотканных элементов.
Лейомиома может быть одиночной, но чаще выделяют множественные узлы. Изменения миометрия при развитии опухоли чаще возникают по средней линии, в области трубных углов и боковых отделах шейки, где имеются особенно тесные переплетения мышечных волокон. Лейомиомы обнаруживают и вне матки (в фаллопиевых трубах, влагалище, круглых и прямокишечно – маточных связках, вульве и ЖКТ).
Этиопатоганез:
►лейомиома появляется в результате локальной пролиферации гладкомышечных клеток. По мере роста в структуре лейомиомы начинают преобладать фиброзные элементы;
►лейомиомы развиваются из незрелых гладкомышечных клеток:
- сокращения матки, создающие области напряжения внутри миометрия, могут быть стимулом к росту этих малодифференцированных клеток;
- множество областей напряжения внутри миометрия приводит к развитию множественных миом;
►часто развитие лейомиомы связано с гормональным дисбалансом, в том числе с гиперэстрогенией;
►миомы могут возникать и у женщин с отсутствием гормональных нарушений;
►ведущим фактором в развитии миомы матки является нарушение метаболизма эстрогенов (преобладание эстрона и эстрадиола в фолликулиновой, а эстриола – в лютеиновой фазе цикла) и функции жёлтого тела;
►миома матки – гормонально зависимое новообразования. В её возникновении и развитии важную роль играют нарушения в системе «гипоталамус – гипофиз – яичники – матка»;
►развитие и рост миомы во многом обусловливаются состоянием рецепторного аппарата матки, нарушения в котором могут способствовать изменению характера роста опухоли (быстрый, медленный);
►изменение кровоснабжения;
►изменение иммунологической реактивности организма;
►наследственная предрасположенность;
►предрасполагающие факторы – преданемические состояния и железодефицитная анемия (нарушение окислительно–восстановительных процессов, имеющее место при этом, создаёт более благоприятные условия для роста миомы)
Классификация:
●по локализации:
- в теле матки (95 %)
- в шейке матки (5 %)
●по отношению к мышечной стенке:
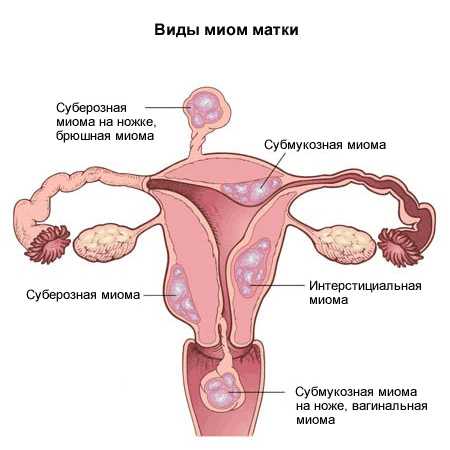
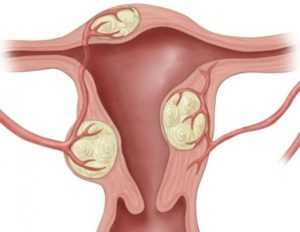
- субсерозные (подбрюшинные) миомы – берут начало из подбрюшинного слоя миометрия, часто связаны с ним тонкой ножкой и способны достигать значительных размеров,
- интрамуральные (межмышечные) миомы – берут начало из среднего слоя миометрия,
- субмукозные (подслизистые) миомы – берут начало из глубокого слоя миометрия, часто связаны с миометрием только тонкой ножкой и могут далеко выдаваться в полость матки и даже выпадать через цервикальный канал (родившийся субмукозный узел на ножке)
●по стадии развития:
- I стадия – образование активного зачатка роста,
- II стадия – быстрый рост опухоли без признаков дифференцировки (узелок, определяемый микроскопически),
- III стадия – экспансивный рост опухоли с её дифференцировкой и созреванием (макроскопически определяемый узелок),
●по морфологическим признакам:
- простая миома (развивается по типу доброкачественных мышечных гиперплазий),
- пролиферирующая миома,
- истинная доброкачественная миома
●дегенеративные изменения миомы:
- гиалиновая дистрофия – избыточный рост фиброзных элементов ведёт к гиалинизации фиброзной ткани и, в конечном счёте к кальцификации,
- кистозное перерождение,
- некроз – следствие нарушения кровоснабжения или инфекции.
- Красная дегенерация – особый вид некроза, возникающий чаще во время беременности. Очаг поражения имеет тусклый красноватый цвет, обусловленный асептическим некрозом с локальным гемолизом,
- мукоидное набухание,
- саркоматозное перерождение.
Симптомы миомы матки (значит. варьируют в зависимости от размеров, количества и локализации узлов):
☻Патологические менструальные кровотечения (обычно гиперменорея):
- сильное кровотечение возникает вследствие некроза эндометрия, покрывающего подслизистую миому, либо из–за растяжения полости матки с увеличением менструирующей поверхности и снижения сократительной способности миометрия при обширном растяжении интрамуральных миом,
- часто миомы сопровождаются полипами и гиперплазией эндометрия, что может вызвать патологическое кровотечение, Возможны и межменструальные кровотечения,
☻Анемия,
☻Боль:
- острая боль возникает из–за перекрута ножки миомы или некроза узла миомы,
- схваткообразные боли характерны для подслизистых миом, далеко выступающих в полость матки,
☻Сдавление органов малого таза – обычно возникает, если миоматозная матка или узел достигает размеров, соответствующих 10 – 12 неделям беременности и более:
- учащение мочеиспускания – при сдавлении маткой мочевого пузыря,
- задержка мочи- при ретроверсии матки вследствие миоматозного роста. При этом шейка матки сдвигается кпереди в область заднего уретровезикального угла и прижимает уретру к лонному сочленению,
- гидроуретер, гидронефроз, пиелонефрит – при сдавлении мочеточников расположенными внутрисвязочно узлами,
- запоры, затруднение дефекации – при крупных миомах задней стенки матки
☻Бесплодие:
- большие интрамуральные миомы, расположенные в области углов матки, часто перекрывают интерстициальную часть маточной трубы,
- эндометрий над субмукозной миомой может находиться в другой фазе цикла, что ведёт к уменьшению поверхности, пригодной для имплантации бластоцисты,
☻Самопроизвольные выкидыши и преждевременные роды.
Диагностика:
-- бимануальное исследование – определяется увеличенная матка с узловатой поверхностью, плотной консистенции,
-- гистероскопия (при подслизистой миоме),
-- гистеросальпингография (при подслизистой миоме),
-- зондирование полости матки,
-- ультразвуковое исследование,
-- лапароскопия,
-- необходима онкологическая настороженность в отношении больных миомой матки. Для исключения злокачественных новообразований необходимо использовать расширенную кольпоскопию, раздельное диагностическое выскабливание слизистой оболочки и тела матки.
Лечение:
1. Консервативное лечение – показано женщинам с межмышечной и подбрюшинной локализацией узлов опухоли и её размерами, не превышающими величину матки при 12 неделях беременности, заключается в гормонокоррекции:
→производные даназола (антагониста эстрогенов) – принимают в течение не менее 6 месяцев по 0.2 – 0.6 г в сутки,
→золадекс – угнетает выработку гонадотропных рилизинг–факторов в гипоталамусе (1 инъекция в месяц, курс 6 – 9 месяцев),
→гестагены (норколут и другие) – целесообразно применять при гиперэстрогении, возрасте более 40 лет и тому подобное. При приёме гестагенов возможны длительные менструации. Если пациентке более 40 лет, то можно использовать пролонгированные гестагены (депопровера): при этом развивается аменорея
→гормональные контрацептивы, длительное использование которых является также средством профилактики развития предопухолевых и опухолевых образований в женской половой сфере,
→витамин А (ретинола ацетат) – обладает нормализующим влиянием на систему «гипоталамус – гипофиз – яичники», а также антиэстрогенными свойствами,
2. Хирургическое лечение – показано при следующих состояниях:
- подслизистая миома матки,
- межмышечная локализация узла с центральным ростом и резкой деформацией полости матки,
- некроз миоматозного узла,
- подозрение на злокачественное перерождение миомы матки,
- сочетание миомы матки с опухолями половых органов другой локализации,
- большие размеры миоматозных узлов (боле 12 недель беременности),
- быстрый рост опухоли.
Виды хирургического лечения:
1. радикальное хирургическое лечение – показано при быстром росте и больших размерах опухоли, выраженной анемизации больной при отсутствии эффекта от гемостатической терапии, подслизистая миома матки, миома шейки матки, некроз узла, нарушение функции мочевого пузыря и прямой кишки. К радикальным методам относятся:
- надвлагалищная ампутация матки,
- экстирпация матки
2. консервативное хирургическое лечение – проводится женщинам молодого возраста. К консервативным методам относятся:
- миомэктомия – удаление одиночных или множественных миом с вскрытием полости матки,
- подслизистые одиночные узлы могут быть удалены влагалищным путём,
- родившийся подслизистый узел удаляют через влагалище (ножницами подсекают основание ножки и затем откручивают опухоль). После консервативных пластических операций достаточно велико число рецидивов опухоли;
3. полурадикальные методы оперативного лечения – применяют для сохранения менструальной функции у женщин в пременопаузе:
- дефундация матки – выполняется в тех случаях, когда расположение миоматозного узла позволяет сохранить тело матки без её дна;
- высокая надвлагалищная ампутация матки – тело матки отсекают значительно выше внутреннего зева, чем при обычной ампутации;
- лоскутный метод А. С. Слепых – при надвлагалищной ампутации матки выкраивают и оставляют лоскут эндометрия.
Миома матки. Причины, симптомы и лечение миомы
Миома матки (ММ) — моноклональный гормоночувствительный пролиферат, состоящий из фенотипически изменённых гладкомышечных клеток миометрия.
СИНОНИМЫ МИОМЫ МАТКИ
Лейомиома, фиброма, фибромиома.
КОД ПО МКБ-10 D25 Лейомиома матки. D25.0 Подслизистая лейомиома матки.D25.1 Интрамуральная лейомиома матки.D25.2 Субсерозная лейомиома матки.
D25.9 Лейомиома матки неуточнённая.
ЭПИДЕМИОЛОГИЯ МИОМЫ МАТКИ
ММ выявляют в среднем у 80% женщин (по данным аутопсийных исследований). Клинически ММ проявляется у 30–35% женщин в возрасте после 35 лет; в два раза чаще встречается у представителей чёрной расы.
ПРОФИЛАКТИКА МИОМЫ МАТКИ
Доказанное снижение риска развития ММ отмечено при длительном приёме комбинированных оральных контрацептивов, у часто рожавших женщин, у женщин, не подвергавшихся абортам и выскабливаниям слизистой матки, не болевшим воспалительными заболеваниями органов малого таза.
СКРИНИНГ
Проводят УЗИ органов малого таза 1 раз в год, начиная с 25летнего возраста.
КЛАССИФИКАЦИЯ МИОМ МАТКИ
По локализации выделяются следующие виды миомы:
- интрамуральная;
- субсерозная;
- субмукозная;
- педункулярная;
- интралигаментарная;
- паразитирующая.
Топографическая классификация:
- субмукозных узлов♦0 тип – миоматозный узел полностью в полости матки;♦I тип – менее 50% объёма миоматозного узла располагается межмышечно, большая его часть располагается в полости матки;
♦II тип – более 50% объёма миоматозного узла располагается межмышечно, меньшая его часть в полости матки;
- субсерозных узлов♦0 тип – миоматозный узел на ножке, расположен полностью в брюшной полости;♦I тип – менее 50% объёма миоматозного узла располагается межмышечно, большая его часть располагается в брюшной полости;
♦II тип – более 50% объёма миоматозного узла располагается межмышечно, меньшая его часть в располагается в брюшной полости.
Гистологическая классификация:
- простая;
- клеточная;
- митотически активная;
- причудливая;
- атипическая;
- липолейомиома;
- эпителиоидная;
- геморрагическая;
- сосудистая;
- миксоидная;
- миома с гематопоэтическими элементами.
Клиническая классификация:
- клинически незначимые миомы или миомы малых размеров;
- малые множественные миомы матки;
- миома матки средних размеров;
- множественная миома матки со средним размером доминантного узла;
- миома матки больших размеров;
- субмукозная миома матки;
- миома матки на ножке;
- сложная миома матки.
ЭТИОЛОГИЯ (ПРИЧИНЫ) МИОМЫ МАТКИ
Существуют две теории происхождения клеткипредшественника ММ. Одна подразумевает появление дефекта клетки во время онтогенетического развития матки вследствие длительного нестабильного периода эмбриональных гладкомышечных клеток, вторая предполагает возможность повреждения клетки в зрелой матке. Тот факт, что согласно аутопсийным исследованиям распространённость ММ достигает 80%, позволяет считать вторую теорию происхождения клеткипредшественника более правдоподобной.
ПАТОГЕНЕЗ МИОМЫ МАТКИ
Формирование зачатка роста миоматозного узла происходит следующим образом. Можно предполагать, что в ходе многократно повторяющихся циклов гиперплазии миометрия во время менструального цикла происходит накопление гладкомышечных клеток, в которых нарушается процесс апоптоза, и эти пролиферирующие клетки подвергаются воздействию различных повреждающих факторов. Повреждающими факторами могут выступать: ишемия, обусловленная спазмом спиральных артерий во время менструации, воспалительный процесс, травматическое воздействие при медицинских манипуляциях или очаг эндометриоза.
С каждым менструальным циклом количество повреждённых клеток накапливается. Часть клеток рано или поздно элиминируется из миометрия, из других начинают формироваться зачатки миоматозных узлов с различным потенциалом к росту. Активный зачаток роста на первых стадиях развивается за счёт физиологического колебания концентрации гормонов во время менструального цикла. В дальнейшем образовавшаяся кооперация клеток активизирует аутокриннопаракринные механизмы, обусловленные факторами роста, формирует локальные автономные механизмы поддержания роста (локальная продукция эстрогенов из андрогенов и образование соединительной ткани), и значение физиологических концентраций половых гормонов для формирования миоматозного узла перестаёт быть основным.
Пролиферативная активность клеток ММ обусловлена дисрегуляцией генов HMGIC и HMGIY, расположенных в хромосомах 12 и 6 соответственно, то есть в локусах наиболее распространённых хромосомных аббераций, характерных для этого образования. Продуктом экспрессии генов HMGIY и HMGIC признают белки, отнесённые к различным семействам группы высокоподвижных белков. Аберрантная экспрессия HMGIC и HMGIY белков чаще всего характеризует злокачественный процесс. В то же время дисрегуляцию этих белков вследствие хромосомных перестроек наиболее часто выявляют в различных доброкачественных мезенхимальных образованиях. Характер экспрессии HMGIC и HMGIY белков указывает на их участие в быстром росте эмбриональных тканей и тканей в культуре.
Моноклональный пролиферат гладкомышечных клеток миометрия, в которых за счёт дисрегуляции генов HMG активизирована программа клональной пролиферации ткани, на фоне нормального гормонального фона увеличивается в размерах, в то время как клетки неизменённого миометрия находятся в состоянии относительного покоя.
Значение гормонального фона для роста миоматозного узла до определённого этапа критично. С увеличением размера формирование аутокриннопаракринной регуляции роста и становление локальных автономных механизмов делают рост миомы относительно независимым. Здесь речь идёт в большей степени не о способности узла миомы автономно увеличиваться в размерах в условиях полного отсутствия гормонального влияния, а о невозможности значимого регресса размеров образования при лишении его гормональных стимулов. В наибольшей степени это связано с нарастанием в структуре узла доли соединительной ткани, а также за счёт локального синтеза эстрогенов из андрогенов.
КЛИНИЧЕСКАЯ КАРТИНА (СИМПТОМЫ) МИОМЫ МАТКИ
У 50–60% больных ММ протекает бессимптомно. Основными симптомами являются менометроррагия, бесплодие, сдавление смежных органов (мочевого пузыря, прямой кишки), хронические тазовые боли, острый болевой синдром при перекруте ножки миомы или нарушении питания в узле, железодефицитная анемия. Во время беременности (в 10–40%) — её прерывание, гипотрофия и анатомические повреждения плода, преждевременные роды, кровотечения в послеродовом периоде. Около 4% беременностей протекает на фоне ММ. При этом у 50–60% пациенток наблюдают незначительные изменения в размерах миоматозных узлов, у 22–32% — рост узлов, в то время как у 8–27% происходит их уменьшение. Большие узлы, как правило, растут в среднем на 12%, но не более чем на 25% за всю беременность. Маленькие миоматозные узлы, наоборот, имеют тенденцию стабилизироваться в размерах.
ДИАГНОСТИКА МИОМЫ МАТКИ
АНАМНЕЗ
Общий и гинекологический анамнез.
ФИЗИКАЛЬНОЕ ИССЛЕДОВАНИЕ
Бимануальное исследование включает определение размеров матки, миоматозных узлов, а также их локализацию.
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
Для диагностики анемии выполняют общий анализ крови.
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Ультразвуковой метод исследования с использованием трансвагинальных датчиков является рутинным методом исследования и широко применяется для первичной диагностики, а также для динамического наблюдения. С внедрением в хирургическую практику органосохраняющих методов лечения ММ особенно важными являются топическая диагностика миоматозных узлов, оценка их структуры. Значительно расширить диагностические возможности метода позволяет контрастирование полости матки жидкими средами при гидросонографии. Данная методика позволяет определить тип субмукозной миомы, его точную локализацию относительно внутреннего зева, маточных углов, оценить толщину миометрия до серозного покрова матки, а также выявить сопутствующую патологию эндометрия. Чувствительность гидросонографии для диагностики ММ составляет 100%.
С внедрением эмболизации маточных артерий (ЭМА) в лечение ММ важным является определение особенностей кровообращения в миоматозных узлах на основании данных допплерографии. Особенностью кровоснабжения доброкачественных миоматозных узлов является формирование перифиброидного сплетения, образованного радиальными, реже — дугообразными артериями, которые отдают внутрь узла терминальные артерии мелкого калибра.
При допплерографии скорость кровотока (Vmax) в пролиферирующей и простой миоме невысокая и составляет от 0,12 до 0,25 см3/c, а индекс резистентности (ИР) равен 0,50–0,56(± 0,86)–0,58–0,69(±0,34). Ультразвуковыми признаками саркомы матки являются неоднородность эхоструктуры узловых образований в миометрии и высокая скорость артериального кровотока в них (Vmax ≥ 0,40 см3/с) в совокупности с низким индексом резистентности (ИР ≤ 0,40 см3/с). Допплерография используется также для оценки эффективности ЭМА.
Ещё одним методом визуальной оценки кровотока в матке и миоматозных узлах является ангиография. Этот метод до настоящего времени не находил широкого применения, однако с началом эндоваскулярных вмешательств на матке его использование является обязательным перед проведением ЭМА, поскольку позволяет оценить особенности кровоснабжения органов малого таза и выявить патологический кровоток в миоме. По данным ангиографии саркома матки имеет патологический дихотомический тип кровоснабжения. Достоверными признаками злокачественного перерождения при саркоме матки считаются: обширные зоны с беспорядочно расположенными сосудами и мелкими лакунарными скоплениями контрастированной крови. Разъединённые сосуды вызывают образование сосудистых озёр в некротической ткани и указывают на быстрорастущую, злокачественную опухоль, склонную к центральному некрозу.
Золотым стандартом диагностики субмукозных миоматозных узлов является гистероскопия, при которой оценивают тип узла, расположение, размеры и возможность проведения трансцервикальной миомэктомии под эндоскопическим контролем.
Для оценки топографического расположения миоматозных узлов при гигантских ММ, а также для контроля за эффективностью ЭМА всё более широко применяют МРТ. Чувствительность метода без контрастирования относительно патологии миометрия и эндометрия составляет 67%, с контрастированием — 98%. Несмотря на достаточно широкий арсенал неинвазивных методов визуальной диагностики до настоящего времени не потерялала своей актуальности диагностическая лапароскопия, которую проводят в основном с целью дифференциального диагноза солидных опухолей яичников, забрюшинных опухолей и субсерозных миоматозных узлов.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальную диагностику субсерозных миоматозных узлов осуществляют с солидными опухолями яичников, забрюшинного пространства и брюшной полости. Необходимо проводить дифференциальный диагноз между ММ с проявлениями менометроррагий и аденомиозом, а также прерывающейся беременностью.
ПРИМЕР ФОРМУЛИРОВКИ ДИАГНОЗА
Миома матки, соответствующая 10 неделям беременности, с субмукозным расположением узла. Меноррагия. Анемия.
ЛЕЧЕНИЕ МИОМЫ МАТКИ
ЦЕЛИ ЛЕЧЕНИЯ
Устранение анемизирующих маточных кровотечений и других симптомов, связанных с увеличением матки. Сохранение органа и восстановление репродуктивной функции.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ
Маточное кровотечение, нарушение питания в узле, перекрут ножки узла, острое нарушение функции соседних органов (острая задержка мочи, гидроуретер и гидронефроз и др.). Плановая госпитализация для хирургического лечения.
НЕМЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ МИОМЫ МАТКИ
Неэффективно.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ МИОМЫ МАТКИ
Медикаментозное лечение целесообразно для узлов размерами до 3 см.
Назначают агонисты гонадотропинрилизинг гормона (ГнРГ) — депоформы по 3,75 мг 1 раз в 28–30 дней, в течение 6 циклов, начиная с первого дня очередного менструального цикла под контролем УЗИ 1 раз в 3 месяца. Также используют мифепристон или гестринон по 2,5 мг 2 раза в неделю в течение 3–6 месяцев. Если лечение проводят в перименопаузе, в последующем наступает естественная менопауза, а в репродуктивном возрасте необходим стабилизационный этап с использованием современной гормональной контрацепции (низкодозированные комбинированные оральные контрацептивы или внутриматочная гормональная система мирена ©).
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ МИОМЫ МАТКИ
- Радикальное: гистерэктомия лапаротомическим, лапароскопическим доступом. Наиболее простой метод с точки зрений технического выполнения. Лечение по принципу «нет органа — нет проблем». Этот метод неприемлем для женщин, желающих сохранить матку и реализовать репродуктивную функцию. В современной классификации лечебных подходов гистерэктомия должна быть рекомендована только при наличии строгих показаний. Таковыми являются: подозрение на саркому матки при быстром росте миомы (свыше 4 нед за 1 год), размеры ММ свыше 14–16 недель беременности, рост ММ в постменопаузе. Гистерэктомия показана также при шеечной ММ, нарушении питания в миоматозном узле, нарушении функции соседних органов, а также невозможности выполнения органосберегающих методов лечения или неэффективности медикаментозного лечения при ММ и менометроррагии, анемизирующей пациентку. Выбор операционного доступа определяется размером матки и локализацией миоматозных узлов. Оптимальным для выполнения гистерэктомии лапароскопическим доступом является размер матки не превышающий 11–12 нед. Ограничениями для использования лапароскопического доступа являются размер матки, превышающий 16–18 нед беременности, наличие низко расположенных миоматозных узлов, особенно по задней стенке матки, или наличие больших интралигаментраных миоматозных узлов. При выборе операционного доступа необходимо учитывать сопутствующую патологию яичников или шейки матки, наличие и выраженность спаечного процесса, соматические заболевания. У 30–55% пациенток репродуктивного возраста, перенесших гистерэктомию без придатков, развивается постгистерэктомический синдром, обусловленный гипоэстрогенным состоянием изза снижения овариального кровотока и нарушения рецепторных взаимодействий в системе яичники–миометрий–эндометрий. В качестве лечения постгистерэктомического синдрома у женщин детородного возраста должны быть использованы препараты ЗГТ (фемостон 1/5 ©, дивина ©, климонорм ©, цикло- прогинова © и др.) или тканеселективные модуляторы эстрогеновых рецепторов (ливиал ©). Назначение препаратов ЗГТ длительным курсом предусматривает контроль за состоянием молочных желёз (УЗИ и маммография до 2 раз в год), контроль за свёртывающей системой крови и липидным спектром крови.
- Консервативно-пластическое: традиционнооптимальной органосохраняющей операцией при субмукозной локализации ММ считают трансцервикальную миомэктомию с использованием механических, электро и лазерохирургических способов удаления. Возможность проведения трансцервикальной миомэктомии зависит от величины узла и от его формы. Возможно удаление субмукозных узлов 0 типа продолговатой формы и мягковатой консистенции до 10 см в диаметре механическим способом. Электрохирургическая миомэктомия безопасна при субмукозных узлах размерами до 5 см в диаметре. Для удаления подслизистых узлов 2го типа с выраженным интерстициальным компонентом и размерами свыше 5 см в диаметре необходимо проведение предоперационной подготовки агонистами ГнРГ. После второй инъекции препарата Гн- РГ происходит уменьшение миоматозных узлов на 35–40% в сравнении с исходными размерами. Помимо этого у ряда пациенток происходят переход 2го типа субмукозного узла в 1й, а также снижение перфузии крови в маточных артериях и возникновение медикаментозной атрофии эндометрия, что в целом значительно снижает хирургический риск и интраоперационную кровопотерю. Наряду с положительными моментами воздействия агонистов ГнРГ на матку известны и недостатки. Неблагоприятным является миграция субмукозных узлов 2го типа межмышечно, что затрудняет их поиск во время оперативного вмешательства. В таких случаях удаление субмукозных узлов невозможно. У молодых женщин также наблюдают возникновение тяжёлых климактерических проявлений, связанных с дефицитом эстрогенов. В результате электрохирургическая трансцервикальная миомэктомия противопоказана при неэффективности воздействия агонистами ГнРГ, величине миоматозных узлов свыше 5 см, длине полости матки более 10 см, при сочетанном расположении субмукозных миоматозных узлов с узлами другой локализации (особенно перешеечных) и аденомиозом. Также нецелесообразно проведение электрической резекции миоматозных узлов трансцервикальным доступом при наличии рубца после кесарева сечения или миомэктомии, маленькой и ригидной шейке матки у нерожавших пациенток. Рассматривая вопрос о проведении органосохраняющих операций при субсерозных миоматозных узлах, основным критерием эффективности миомэктомии следует считать формирование полноценного рубца на матке, который должен быть состоятельным при последующей беременности. Субсерозные узлы типов 0 и 1 небольших размеров не представляют сложности для миомэктомии — методом выбора в этих случаях является лапароскопический доступ. В тех случаях, когда интерстициальный компонент узла выражен, для уменьшения ложа узла и снижения кровопотери в момент операции показано проведение предоперационной подготовки агонистами ГнРГ. Уплотнение и утолщение псевдокапсулы миоматозного узла облегчают его энуклеацию и позволяют производить миомэктомию менее травматично и бескровно. Ложе удалённого субсерозного узла должно быть тщательно ушито. К сожалению, лапароскопический доступ не всегда позволяет провести адекватное сопоставление краёв раны, нередко при энуклеации субсерозного узла образуется обширная зона коагуляционного некроза, которая приводит к формированию неполноценной рубцовой ткани и наличию дефекта в слоях миометрия. Ошибка в топографической диагностике и переоценка технических возможностей в использовании лапароскопического доступа чревата несостоятельностью рубца на матке во время беременности и разрывом матки во время беременности и родов. Исходя из этого, определены чёткие противопоказания к проведению миомэктомии лапароскопическим доступом у пациенток, желающих сохранить репродуктивную функцию. Не следует производить лапароскопическую миомэктомию при больших размерах матки (более 12 нед беременности), наличии множественных интерстициальных миоматозных узлов, низком расположении (шеечноперешеечном) миоматозного узла, особенно по задней стенке, а также общем количестве миоматозных узлов свыше 4. Безальтернативным доступом у этих пациенток при выполнении миомэктомии является лапаротомия. Наличие противопоказаний к выполнению миомэктомий при субмукозных и субсерозных миоматозных узлах ранее не оставляло выбора в тактике, и большинство пациенток подвергалось гистерэктомии. С появлением эндоваскулярных методов лечения опухолевых образований и возможности проведения эмболизации маточных артерий (ЭМА) у больных с ММ появился новый безоперационный органосохраняющий метод лечения.
- Стабильнорегрессионное: эмболизация маточных артерий, лапароскопическая окклюзия маточных артерий. Клиническая эффективность ЭМА для ММ различной локализации заключается прежде всего в уменьшении размеров матки и нормализации менструальной функции. Меноррагия купируется с момента проведения ЭМА, объём кровопотери в менструацию уменьшается в 3–4 раза, что приводит к быстрому восстановлению показателей красной крови. Этот эффект обусловлен рядом факторов, среди которых выделяют следующие: снижение перфузии крови в бассейне маточных артерий в 2 раза, частичная закупорка мелких радиальных и базальных ветвей и полная редукция артериального кровотока в миоматозных узлах. Уменьшению кровопотери, безусловно, способствует восстановление сократительной способности миометрия вследствие уменьшения размеров миоматозных узлов, а также восстановление анатомических параметров полости матки после экспульсии или энуклеации субмукозных узлов. Объём матки и миоматозных узлов к году наблюдения сокращается в 2,5 и 3 раза соответственно. При субмукозной локализации миоматозных узлов, интерстициальной локализации с центральным и центрипетальным направлением роста выявлено несколько вариантов исхода. Возможна самопроизвольная экспульсия миоматозных узлов, миоматозные узлы могут выделяться в виде фрагментов некротизированной ткани или некротизированного детрита. При миграции узлов в полость матки после ЭМА и невозможности их самостоятельной экспульсии целесообразно проведение трансцервикальной миомэктомии механическим способом или методом резекции под контролем гистероскопии или УЗИ. Возможна миграция миоматозных узлов межмышечно. Данный эффект после ЭМА считается также благоприятным, поскольку наряду с уменьшением размеров миоматозных узлов происходит восстановление топографии полости матки и снижение кровопотери в менструацию. Уменьшение размеров ложа миоматозных узлов после ЭМА при их субсерозной локализации позволяет формировать полноценный рубец после миомэктомии. При больших и гигантских размерах ММ и миоматозных узлов у пациенток детородного возраста ЭМА выполняют как самостоятельный метод или как этап перед лапаротомической миомэктомией. Эндоскопическая окклюзия маточных артерий также приводит к снижению объёма циркулирующей крови в миометрии, однако не приводит к полной редукции артериального кровотока в миоматозных узлах. Данный метод целесообразно использовать перед выполнением эндоскопической миомэктомии, поскольку в значительной степени снижается объём кровопотери в момент энуклеации узлов, а сокращение миометрия после окклюзии обусловливает выделение миоматозных узлов в брюшную полость и уменьшение размеров их ложа.
- Временнорегрессионное: агонисты ГнРГ, мифепристон. Их роль существенна в лечении маленьких миоматозных узлов в составе двухэтапной схемы, у части больных перименопазуального возраста, а также в качестве профилактики рецидивов после миомэктомии. На первом (регрессионном) этапе, как правило, используют агонисты ГнРГ (лейпрорелин, бусерелин, трипторелин, гозерелин и др.), на втором (стабилизирующем) этапе — микро или низкодозированные комбинированные оральные контрацептивы с гестагенным компонентом третьего поколения по контрацептивной схеме или в пролонгированном режиме (новинет ©, регулон ©, линдинет ©, мерсилон ©, логест ©, марвелон © и др. по 1 таблетке на ночь с 5го по 25й день каждого менструального цикла или по 1 таблетке на ночь с 1го дня менструального цикла в течение 63–84 сут с последующим перерывом на 7 дней). Стабилизирующий этап может быть обеспечен применением внутриматочной гормональной рилизинг-системы мирена ©, особенно при отсутствии у рожавшей женщины ближайших повторных репродуктивных планов, а также применением дезогестрелсодержащего орального контрацептива чарозетты © в непрерывном режиме, особенно у курящих женщин старше 35 лет и пациенток с потенциально высоким риском тромбоэмболических осложнений.
- Другие методы: высокочастотный фокусированный ультразвук (дистантная тепловая коагуляция миоматозных узлов); электромиолиз, криомиолиз (внутриполостная деструкция узлов).
Лечение миомы, включая физиотерапию и фитотерапию 2007 г
ПРИМЕРНЫЕ СРОКИ НЕТРУДОСПОСОБНОСТИ
После оперативного лечения сроки нетрудоспособности колеблются в зависимости от доступа и выполненного хирургического объёма. При лапароскопической гистерэктомии он составляет от 10 до 24 дней, лапаротомической гистерэктомии — от 14 до 24 дней, лапароскопической миомэктомии — до 14 дней, гистероскопической миомэктомии — от 7 до 14 дней, лапаротомической миомэктомии — от 14 до 24 дней. При ЭМА срок нетрудоспособности составляет 7–14 дней.
ДАЛЬНЕЙШЕЕ ВЕДЕНИЕ
После гистерэктомии, лапароскопической и лапаротомической миомэктомии и ЭМА в течение 1 месяца продолжают профилактику тромботических осложнений (компрессионное бельё на ноги, назначение ацетилсалициловой кислоты, дипиридамола, пентоксифиллина). Антианемическую терапию проводят до нормализации показателей красной крови. У пациенток с развившимся постгистерэктомическим синдромом назначают препараты ЗГТ. После ЭМА контрольные УЗИ проводят через 1, 6, 12 мес, при возможности и необходимости беременности — через 12 мес.
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТКИ
Необходимо проведение планового УЗИ 1 раз в год, а у пациенток с выявленной ММ — 2 раза в год. Рекомендуют воздерживаться от инсоляции, бань, саун, массажей поясничной области и ягодиц.
ПРОГНОЗ
Благоприятный.
Миома матки
Миома матки – это доброкачественная опухоль, которая образуется из соединительной и мышечной ткани матки. Женщины с таким заболеванием встречаются часто. Статистика говорит, что ~16-18% женщин в возрасте >30 лет, страдают фибромиомой матки. До сегодня не существует единой теории развития миомы матки. Многие опытные исследователи связывают ее возникновение с гормональными нарушениями. Другие придерживаются теории об инфекционном развитии. С этой теорией образование миомы связывают с абортами, ВМС, инфекционными и воспалительными процессами. Не больше значение придается нарушениям иммунологической защиты. К возникновению миомы несомненна роль генетической предрасположенности.
Классификация миомы матки
По локализации:
- миома тела матки (приблизительно 95% случаев);
- миома шейки матки (5% случаев).
По отношению к миометрии:
- подслизистая или субмукозная;
- межмышечная или интерстициальная;
- подброшенная или субсерозная.
Если подслизистая опухоль находится в мышечном слое, используют термин «межмышечная миома матки с центрипетальным ростом». В полости матки, рост опухоли происходит по направлению к внутреннему зеву. Растущие миоматозные узлы приводят к раскрытию и сглаживанию маточного зева, поэтому опухоль выходит за приделы наружного отверстия матки.
Клиническая картина при миоме матки зависит от длительности заболевания, возраста женщины, размеров опухоли, локализации. Чаще миома матки маленьких размеров протекает бессимптомно, при этом отсутствуют нарушения менструального цикла и жалобы. Симптомами заболевания является кровотечение, интенсивная боль, нарушение функции соседних органов. Нередко беспокоят боли в пояснице, нижних отделах живота. При длительных болях, растет быстро опухоль.
Острые боли возникают при нарушениях кровоснабжения в опухоли. Такие опухоли могут привести к развитию некроза. Схваткообразные боли в момент менструации говорят о подслизистом расположении узла. При миоме матки, кровотечение носит характер гиперполименореи. Если множественная миома матки, то происходит увеличение полости матки и ее растяжение. За счет этого, в момент менструации теряется много крови.
Большая потеря крови возникает при миомах с центрипитальным ростом и также подслизистым расположением узлов. Для данной локализации характерны длительные кровотечения, наличие межменструальных кровотечений с развитием анемии. Как правило, миома, растет не быстро. А если быстро, то размер матки увеличивается к размеру 5-недельной беременности за один год.
Если такая ситуация существует, то говориться о злокачественности процесса. Функция соседних органов нарушается при больших размерах опухоли. Частым осложнением можно назвать перекрут узла, расположенного на ножке, некроз миоматозного узла. При некрозе – возникают острые боли, поднимается температура. Некроз миоматозного узла чаще всего подвергает субсерозные узлы.
Перекрут узла, расположенного на ножке – частое осложнение миомы. При этом нарушается питание опухоли, происходят дегенеративные и дистрофические изменения, отек. Существуют острые боли. Другим осложнением называется анемия.
Диагностика миомы матки
В момент ранних стадий, формирования опухоли, трудно поставить клинический диагноз миомы матки. Чаще диагноз устанавливается на амбулаторном приеме. Точные результаты получают с помощью ультразвукового сканирования матки. Такой метод очень популярный. Если возникают подозрение на деформацию полости матки или на наличие подслизистой миомы матки, то производят метросальпингографию или гистероскопию. При диагностике нужно учитывать день и фазу менструального цикла, проводить осмотры и УЗИ-сканирования в дни цикла.
Получены ультразвуковые сканирования, позволяют установить локализацию, состояние миоматозных узлов, размеры, объем оперативного вмешательства.
Как лечить миому матки?
Распространённые показатели миомы матки:
- длительное кровотечение, приводящие к анемии;
- быстрый рост опухоли;
- выраженный болевой синдром;
- большие размеры миомы;
- симптомы сдавления смежных органов;
- интралигаментарная опухоль;
- миома шейки матки;
- подслизистая миома матки;
- некроз миоматозного узла;
- бесплодие;
- центрипентальный рост миоматозного узла;
- перекрут ножки миоматозного узла;
- связь миомы матки с предраковым состоянием шейки матки;
- связь миомы матки с опухолью яичников;
- подозрение на злокачественное перерождение миомы.
Хирургическое лечение. Оно может быть: радикальным и консервативным.
К консервативным методам относятся:
- гистероскопическая миомэктомия;
- лапароскопическая миомэктомия;
- лапаротомия с миомэктомией.
Консервативное хирургическое лечение проводят у молодых женщин, независимо от расположения, числа узлов, величины.
Лапароскопическая миомэктомия.
Этот метод удаляет узлы с сохранением матки. Показаниями являются, узлы на ножке, интрамурально и субсерозно расположенные миоматозные узлы, диаметр которых – 2 см. Противопоказаниям – наличие больше 3 митматозных узлов.
Гистероскопическая миомэктомия.
Метод удаления узла влагалищным путем. Показания – расположенный субмукозно миоматозный узел. Противопоказания – подозрение на аденокарциному эндометрия или гиперплазию, инфекция отделов половых путей.
Лапаротомия с миомэктомией.
Применяется в том случаи, если отсутствует возможность проведения лапароскопических методов. После консервативного вмешательства возможен рецидив новых миоматозных узлов.
Гистерэктомия (удаление матки).
Во всех отношениях – это радикальный хирургический метод лечения. Такое вмешательство делается в том случаи, если все вышеперечисленные методы оказались не эффективными. Консервативное лечение миомы матки тормозит рост опухоли. Назначается в циклическом режиме по 5 мг каждый день с 16-го по 25-й день цикла на протяжении около шести месяцев каждый год. Также назначают электрофорез йодида калия на надлобковую область. С помощью, надежных методов контрацептива сокращается количество медицинских абортов. Чтобы своевременно обнаружить миому матки необходимо регулярно ходить к гинекологу.
Классификация миомы матки
16 Декабря в 11:05 2835
Миома матки классифицируется по следующим принципам:
1) по локализации в различных отделах матки: в 95% наблюдений опухоль располагается в теле матки и в 5% — в ее шейке (шеечная миома);
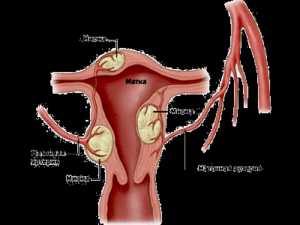
2) по отношению к мышечному слою матки различают три формы роста опухоли: межмышечную (опухоль располагается в толще стенки матки), подслизистую (рост миомы происходит по направлению к полости матки) и подбрюшинную (рост миомы происходит по направлению к брюшной полости). В тех случаях, когда подслизистая опухоль располагается преимущественно в мышечном слое (более чем на 1/3 объема узла), используют термин «межмышечная миома матки с центрипеталъным ростом» (рис. 1). При экзофитном росте миомы из нижних отделов тела матки или ее шейки опухоль может располагаться забрюшинно (забрюшинная миома матки) или между листками широкой связки (межсвязочная миома матки).
Различные формы роста миомы матки отличаются не только по морфологическому строению: подслизистые и межмышечные опухоли относятся к истинным миомам матки, так как соотношение в них паренхимы и стромы составляет 1:2, подбрюшинные — являются фибромиомами (в этих опухолях указанное соотношение достигает 1:3), но и по потенциальной способности к росту: активация обменных процессов наиболее выражена в подслизистых миомах, что обусловливает высокую тенденцию к их росту и увеличивает риск озлокачествления.
Среди подслизистых узлов миомы различают особую форму — рождающие опухоли, рост которых в полость матки происходит по направлению к внутреннему зеву. Длительное развитие рождающихся миоматозных узлов приводит к сглаживанию и расширению краев маточного зева и нередко сопровождается выходом опухоли за пределами наружного отверстия матки;
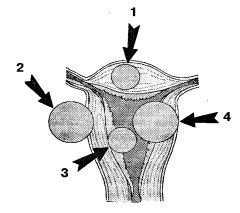
Рис. 1. Расположение узлов миомы по отношению к мышечному слою матки: 1 — межмышечное; 2 — подбрюшинное; 3 — подслизистое; 4 — центрипетальный рост
3) по морфогенетическому типу; в зависимости от функционального состоянию мышечных элементов выделяют три типа опухоли:
а) простая миома, развивающаяся по типу доброкачественной мышечной гиперплазии;
б) пролиферирующая миома, обладающая морфогенетическими критериями истинной доброкачественной опухоли миометрия (клетки мышечных волокон пролиферирующей опухоли не атипичны, однако в сравнении с простой миомой количество их на одной и той же площади значительно выше);
в) предсаркома; данный тип опухоли характеризуется наличием множественных очагов пролиферации миогенных элементов с явлениями атипии, неоднородностью ядер клеток, появлением на отдельных участках многоядерных клеток с крупными гиперхромными ядрами.
В простой миоме митозы отсутствуют, в пролиферирующей опухоли и предсаркоме митотическая активность повышена, вместе с тем соотношение числа нормальных и патологических митозов неодинаково: в пролиферирующей миоме количество патологических митозов не превышает 25%, в предсаркоме достигает 75%.
Избранные лекции по акушерству и гинекологии
Под ред. А.Н. Стрижакова, А.И. Давыдова, Л.Д. Белоцерковцевой
Смотрите также
- От чего образуется миома матки у женщин
- Как остановить маточное кровотечение в домашних условиях при миоме
- Почему растет миома матки

- Аборт и миома
- Диагностическое выскабливание матки при миоме

- Киста и миома в чем разница

- Центрипетальный рост миомы матки
- После удаления миомы матки реабилитация

- Резектоскопия миомы матки
- Жанин и миома
- Лечение миомы народными средствами рецепты которые помогли

