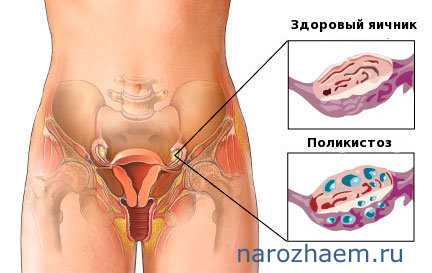
Гиперфункция яичников
Гиперфункция яичников
Гиперфункция яичников - явление очень редкое, в отличии от гипофункции, и наблюдается лишь у 10-15% женщин. При этом данное явление обычно характеризуется, как гиперадрогения или гиперэстрогения.
Гиперадрогения является физиологическим состоянием женского организма, при котором наблюдается повышенная продукция андрогенов. При гиперэстрогении – увеличивается концентрация эстрогенов в крови.
Чем может быть вызвана гиперфункция яичников?Причины, которые вызывают развитие данного состояния, следующие:
- Избыток гормона инсулина в организме. Именно данный гормон активирует синтез лютеотропного гормона, а далее и андрогенов в яичниках и надпочечниках.
- Наличие опухолевидных образований яичника, которые также могут синтезировать избыток андрогенов. Так, к примеру, клетки Лейдига, называемые лецдигомами, синтезируют гормон тестостерон.
- Ферментативная недостаточность. К примеру, недостаток в организме Зр-гидроксистероиддегидрогеназы приводит к избытку дегидроэпиандростерона.
Как проявляется гиперфункция яичников?
Симптомы гиперфункции яичников чаще всего скрыты, что не позволяет порой начать лечение своевременно. Чаще всего, женщины жалуются на нерегулярные месячные, а также меноррагию, которая обусловлена длительным повышением уровня эстрогенов в крови, что в свою очередь нарушает периодические колебания содержания прогестерона.
Однако, в большинстве случаев о гиперфункции яичников женщина узнает только после проведения лабораторных исследований. Так в крови и моче повышается уровень андрогенов. При этом тело женщины начинает приобретать мужские черты: увеличивается мышечная масса, наблюдается гипертрихоз.
Следствием данного нарушения является гипертрофия яичников. Данное явление проявляется, прежде всего, в увеличении их размера, что подтверждают результаты УЗИ.
Статьи по теме:| Лопнула киста яичника - симптомы Киста может спокойно находиться долгое время на органе, пораженном патологией. Но иногда она лопается, или иными словами, проходит ее разрыв. Как можно определить данное состоянии, каковы его симптомы и последствия, - об этом вы узнаете, прочитав нашу статью. | Болит яичник справа - причины Женщины часто сталкиваются с проблемой неприятных болей в области яичников. Согласно статистики, боли в правом яичнике возникают намного чаще, чем в левом. Это обусловлено строением внутренних органов организма. Так, каковы причины возникновения болей справа? Об этом вы узнаете, прочитав нашу статью. |
| Истощение яичников - лечение Преждевременное истощение яичников часто означает приход ранней менопаузы. Это патологическое состояние, и в большинстве случаев требует лечения для пролонгации функционирования репродуктивных органов до возраста, в котором обычно наступает естественный климакс. Подробнее об этом в нашей статье. | Киста желтого тела яичника Киста - патология, которая встречается довольно часто у женщин разного возраста, начиная от подростков, и заканчивая представительницами прекрасной половины человечества, достигших возраста менопаузы. В свою очередь, данные новообразования имеют множество форм. Сегодня мы поговорим о кисте желтого тела. |
womanadvice.ru
Гиперфункция яичников: что это, симптомы, лечение
Гиперфункция яичников — это состояние, которое характеризуется повышенной секрецией или усиленным действием андрогенов и возникает у 10-15% женщин. При наличии патологии происходит одновременное созревание нескольких яйцеклеток. На фоне этого увеличивается риск возникновения многоплодной беременности.
В большинстве случаев заболевание развивается у женщин старше 35 лет.
Причины возникновения
Среди главных факторов, которые способствуют развитию гиперфункции выделяют:
- Избыточное количество инсулина. Инсулин запускает производство андрогенов и лютеотропного гормона в придатках и надпочечниках.
- Опухолевые новообразования в яичниках, увеличивающие выработку андрогенов из клеток Лейдига, которые называются лецдигомами и отвечают за выработку тестостерона.
- Ферментивная недостаточность. Нехватка ЗР-HSD вызывает избыток дегидроэпиандростерона.
- Наследственная предрасположенность.
- Оральная контрацепция (противозачаточные таблетки).
В ряде случаев патология возникает у женщин, которые любят пить коровье молоко. Иногда на фермах в пищу животным добавляют гормоны роста. Именно поэтому у пациенток, употребляющих большое количество коровьего молока, происходят нарушения в гормональном фоне.
Гиперфункцию яичников можно вызвать искусственно, сделав инъекцию гормонального препарата. Такую стимуляцию выполняют во время протокола ЭКО для получения множества ооцитов.
Симптомы
Симптомы гиперфункции придатков обычно проявляются слабо или не возникают вообще. Именно это и мешает вовремя начать лечение. Часто женщины отмечают сбой менструального цикла, наблюдается меноррагия, возникающая из-за слишком высокого уровня эстрогенов в крови.
Чаще всего пациентка узнает о наличии патологии после сдачи анализов. В моче и крови превышается нормальный уровень андрогенов. Нередко на теле женщины появляются мужские признаки: увеличивается оволосение кожи, становится больше мышечная масса, на ультразвуковой диагностике видно увеличенные в размерах яичники.
Разновидности патологического процесса
Гиперфункция яичников может проявляться в виде гиперандрогении или гиперэстрогении.
При гиперандрогении происходит высокая выработка андрогена. Болезнь может быть выражена в различной степени, все зависит от особенностей конкретного организма. Большое количество половых гормонов наблюдается в период полового созревания. В периферической ткани андроген преобразуется в эстроген. У женщины появляется акне, гирсутизм, себорея, лишний вес, возможны сбои в менструальном цикле, овуляция не происходит, и возникает бесплодие.
При гиперэстрогении в крови пациентки появляется избыточное количество эстрогена. У девочек патология характеризуется ранним половым созреванием, сбоями в менструальном цикле, акселерацией. У женщин появляется меноррагия — продолжительное и обильное маточное кровотечение.
Диагностика
Диагностировать гиперфункцию яичников сложно, потому как она может протекать бессимптомно. Чем раньше будет поставлен диагноз и начато правильное лечение, тем больше шансов на выздоровление.
Существует несколько методов диагностики данного заболевания:
- Анализ мочи и крови, по которым определяют уровень гормонов.
- Ультразвуковое исследование малого таза. Является информативным методом диагностики и позволяет определить размеры яичников.
- Кольпоскопия придатка. Осмотр, выполняемый при помощи кольпоскопа. Иногда процедуру дополняют цитологическим исследованием.
Методы терапии
Лечение гиперфункции яичников может быть консервативным и оперативным.
Консервативное лечение включает в себя гормонотерапию. При этом пациентке назначают эстроген-гестагенные препараты и антиандрогены — препараты, которые подавляют избыточное выделение мужских половых гормонов. В случае отсутствия результата, врачи используют малоинвазивную терапию. Пациентке может назначается диатермокоагуляция или резекция.
Новым, но весьма эффективным методом избавления патологического процесса является терапия радиоволнами. Процедура щадящая, не затрагивает здоровые ткани яичников, без побочных эффектов и проводиться только тем женщинам, у которых новообразования (если есть) не преобразуются в злокачественные.
Помните! Перед началом лечения врач обязательно доложен определить причину, по которой произошел гормональный сбой.
Радикальным способом борьбы с гиперфункцией является оперативное вмешательство. Проводиться в следующих случаях:
- Когда все остальные методы не дали должного эффекта;
- При подозрении на наличие злокачественных опухолей;
- Быстрое ухудшение состояния пациентки;
- Если новообразования были обнаружены как доброкачественные, но потом переросли в злокачественные. Раковые опухоли будут давать метастазы, ведь высокий синтез гормонов является прекрасной средой для размножения злокачественных клеток.
После проведения оперативного лечения назначается гормональная терапия для стабилизации гормонального фона. Через некоторое время делаются анализы крови с целью оценки эффективности проведенной операции.
Здоровые яичники являются основным условием зачатия ребенка, благоприятного протекания беременности и материнства. Несвоевременное лечение гиперфункции яичников способно привести к бесплодию
.oyaichnikah.ru
Гиперфункция яичников, обстоятельства, диагностика, современные методы лечения
Лишь женщина способна подарить миру новую жизнь, исходя из этого заботиться о женском здоровье так важно. Репродуктивная система устроена сложно. Малейший сбой в ее работе может привести к бесплодию, и вызвать разные болезни.
Яичники, не обращая внимания на свой малый размер и вес, делают самую ключевую роль в организме женщины – формируют и дают питание яйцеклетке, без которой нереально оплодотворение. Крайне важно следить за здоровьем этого органа (как и всех остальных, но), исходя из этого женщинам рекомендуется каждый год посещать гинеколога.
Яичники – один из наиболее значимых органов женской репродуктивной системы. Тут начинается и созревает яйцеклетка, как раз исходя из этого деятельность яичников напрямую связана с менструальным циклом.
Яичники находятся в области малого таза слева и справа от матки. Их длина – около 40 мм, ширина – около 30 мм, и толщина – не более 10 мм. Само собой разумеется, размеры яичников, зависят от женского возраста.
Строение яичников сложное: внутри – мозговое вещество с множеством сосудов и капилляров, нужных для питания наружного коркового слоя, в котором образуются и зреют фолликулы. Как раз в фолликуле созревает яйцеклетка. Число развивающихся фолликулов в большинстве случаев от 6-7 до 25-30, но в середине цикла остается лишь один фолликул (реже 2), он называется доминантным. В нем увеличивается и развиваться яйцеклетка вплоть до овуляции (выхода яйцеклетки в матку), деятельность остальных фолликулов замирает.
Яичники делают три основные функции:
- Генеративную – возможность формирования яйцеклетки, готовой к оплодотворению.
- Вегетативную – развитие первичных и вторичных женских половых показателей.
- Гормональную – выработка яичниками гормонов, нужных для подготовки к зачатию и беременности женщины.
Яичники производят три вида гормонов:
- эстрогены,
- прогестерон,
- тестостерон (мужской гормон).
Эстрогены необходимы для оптимальной работы женских внутренних органов (матки, влагалища, и самих яичников), генерирования яйцеклетки и верного углеводно-минерального обмена. Это самые ответственные женские гормоны.
Прогестерон снабжает развитие и жизнеспособность плода, контролирует течение беременности.
Тестостерон нужен женщине для упрочнения физического строения тела (мускулы, связки), верного развития тела и опорной системы, помимо этого он участвует в ходе выработки женских гормонов.
От деятельности и здоровья яичников зависит возможность женщины зачать и выносить ребенка, данный малый по размеру орган делает большое количество работы в организме женщины.
Самые популярные патологии
К сожалению, практически все заболевания яичников, не вылеченных своевременно либо не поддающихся лечению, угрожают бесплодием. Особенно страшны бессимптомные болезни, в то время, когда женщину нет ничего, что тревожит. Исходя из этого женщинам рекомендуется посещать гинеколога не меньше 1 раза в год.
Часто встречаются патологии яичников у женщин независимо от ее возраста.
Воспаление
Начинается при попадании и развитии заразы в яичники, часто сопровождается развитием воспаления маточных труб и связок. Заразу смогут вызвать вирусы, микробы и простейшие организмы.
Воспалительный процесс в яичниках сопровождается рядом признаков:
- Боль внизу живота слева либо справа.
- Увеличение температуры тела до 38-39 градусов.
- Недомогание, головная боль, тошнота.
- Выделения из влагалища с неприятным запахом, их желтоватый цвет говорит о наличии гноя.
Воспаления яичников хорошо поддается лечению, по окончании анализов и осмотра доктор назначает антибиотики определенной группы (пенициллины, цефалоспорины и другие), и через некоторое время болезнь отступает. На протяжении лечения (в среднем до месяца) рекомендуется воздержание от половой близости.
Рак яичника
Самое непредсказуемое заболевание, поскольку практически не имеет признаков на ранней стадии. Рак яичников может пускать метастазы в другие близлежащие органы, исходя из этого заболевание опасно и непредсказуемо. Лечение назначает доктор-онколог по окончании УЗИ, томографии, анализов для подтверждения диагноза.
Потом проводится операция по удалению опухоли либо органа. Значительно чаще, при несвоевременном обнаружении рака яичника удаляются все органы репродуктивной системы женщины.
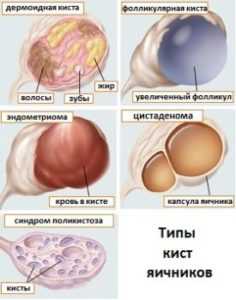
Киста
Заболевание очень сильно распространенно, имеет большое количество разных видов, значительно чаще удаляется хирургическим путем либо шепетильно отмечается доктором, пока не наступит ухудшение.
Заболевание часто протекает бессимптомно, выявляется при УЗИ. Из осложнений заболевания страшны перекручивание ножки кисты и разрыв ее стены. Они уже сопровождаются сильнейшими болями внизу живота, большой температурой и тошнотой.
При них требуется незамедлительная помощь (операция). Кисты способны как правило исчезнуть самостоятельно, а кое-какие смогут перерождаться в злокачественные образования.
Доброкачественные опухоли
Смогут развиваться в одной из частей яичника, характеризуются болевыми приступами в нижней части живота (тупая боль), или совсем не тревожат. При обнаружении назначается операция для удаления опухоли.
Гипофункция и гиперфункция яичников
Гипофункция яичников – это невозможность органа производить необходимое количество женских гормонов. Наряду с этим нарушается целый менструальный цикл: месячные бывают нерегулярно, овуляция случается существенно реже либо совсем отсутствует, исходя из этого появляются неприятности с зачатием ребенка.
Гипофункцию подразделяют на первичную и вторичную. Первичная – нарушение работы яичников на протяжении развития плода, другими словами врожденная. Вторичная гипофункция появляется на фоне негативных условий: стрессы, неправильное питание, воспалительные и инфекционные болезни половой системы, нарушение работы гипоталамуса и гипофиза.
Симптомами гипофункции смогут быть:
- при врожденной патологии – позднее начало менструаций, их нерегулярность, неправильное развитие молочных желез, видимая недоразвитость наружных и внутренних половых органов девочки, отсутствие либо малое количество волос на лобке и подмышках.
- При вторичной гипофункции – психические расстройства, нерегулярные месячные, их отсутствие, синдром климакса в раннем возрасте, уменьшение матки в размерах, бесплодие.
Гипофункция не есть заболеванием, в репродуктивном возрасте (не врожденная) она может появляться неожиданно и встречается частенько.
Гиперфункция яичников у женщин встречается существенно реже. При гиперфункции яичников вырабатывается большее число гормонов, чем нужно организму женщины, другими словами это противоположность гипофункции.
Нарушение гормонального фона не позволяет созревать фолликулам, исходя из этого овуляция не наступает, соответственно невозможна и беременность. Из-за не развития фолликулов яичники возрастают, начинают образовываться фолликулярные кисты.
Симптомы гиперфункции яичников выражены слабо либо отсутствуют совсем. Значительно чаще женщина подмечает сбой менструального цикла. При обследовании заметно кроме этого повышение яичников.
На протяжении гиперфункции преобладает один из вырабатываемых гормонов. При избытке андрогенов у женщин вероятно появление мужских показателей, при преобладании женских гормонов наступает преждевременное старение, женщина выглядит существенно старше своего возраста.
Диагностика и лечение
Диагностика гиперфункции затруднительна, потому, что она имеет слабовыраженные симптомы. Ее определяют по итогам лабораторных изучений. Анализы крови и мочи показывают увеличение андрогенов. Параллельно проводится УЗИ органов малого таза, которое как правило показывает большое повышение яичников.
Лечение начинают с выяснения обстоятельств, по которым вероятен гормональный сбой. Обстоятельствами возможно: лишний вес, нарушение работы гипофиза и гипоталамуса, опухоли яичников и многие другие. Все новообразования яичников удаляются хирургическим путем. После этого назначается терапия для нормализации выработки гормонов. Уровень женских гормонов показывает эффективность проведенного лечения.
Гипофункция и гиперфункция яичников не являются болезнями, но приводят к нарушению репродуктивной функции женщины. Гиперфункция обнаруживается по повышению яичников и увеличению уровня гормонов в крови и моче, исходя из этого нужно своевременно посещать доктора-гинеколога. Здоровые яичники являются главным условием зачатия ребенка, хорошего протекания беременности и материнства. Несвоевременное их лечение значительно чаще приводит к бесплодию.
О любых нарушениях менструального цикла необходимо вовремя информировать доктору, тогда возможно избежать не только гипо- и гиперфункции, но и более важных болезней яичников: доброкачественных и злокачественных опухолей, воспалений и других патологий.
Яичники у женщин
Киста яичника: причины, симптомы, лечение
koxur.ru
Патфиз ч.3
• Проявления. Первичная и вторичная эндокринная недостаточность яичников характеризуется сходными проявлениями. К основных проявлениям относят нарушения менструального цикла, аменорею, бесплодие.
† Нарушения менструального цикла. Проявляются дисфункциональными маточными кровотечениями. Их характеристика приведена в статье «Кровотечение маточное дисфункциональное» (см. приложение «Справочник терминов»).
† Аменорея — отсутствие менструаций более 6 мес у женщин с ранее периодическим их наступлением (вторичная аменорея), а также отсутствие менархе у девочек старше 16 лет (первичная аменорея). Характеристика аменореи изложена в статье «Аменорея» (см. приложение «Справочник терминов»).
† Бесплодие — отсутствие беременности в течение одного года регулярной половой жизни без использования методов предохранения от неё. Бесплодие регистрируется у 10–15% супружеских пар (из них около 30–40% является результатом мужского бесплодия). Характеристика бесплодия изложена в статье «Бесплодие» (см. приложение «Справочник терминов»).
ГИПЕРФУНКЦИЯ ЯИЧНИКОВ
Эндокринная гиперфункция яичников характеризуется гиперандрогенией или гиперэстрогенией (рис. 27–47).
Рис. 27–47. Виды гиперфункции яичников и её основные причины.
• Гиперандрогения — состояние, характеризующееся повышенной продукцией и/или эффектами действия андрогенов. Выявляется в разной степени выраженности у 10–15% женщин.
† Наиболее частые причины.
‡ Гиперпродукция люлиберина нейронами гипоталамуса и/или лютропина клетками аденогипофиза (например, при опухолях, гипертрофии или гиперплазии их). Избыток лютропина обусловливает гиперплазию внешней оболочки и зернистого слоя фолликулов, а также гиперплазию стромы яичников. Указанные изменения сопровождаются увеличением синтеза андрогенов в яичниках и появлением признаков вирилизации организма.
‡ Избыток андрогенных стероидов надпочечникового генеза, особенно в период полового созревания. Эти андрогены трансформируются в периферических тканях в эстрон, который активирует продукцию люлиберина. ЛГ же приводит к увеличению синтеза андрогенов яичниками. В тканях они превращаются в эстрон, что замыкает порочный круг, нередко самопотенцирующийся.
‡ Избыток инсулина в организме. Это активирует синтез лютеотропного гормона и далее — андрогенов как в яичниках, так и в надпочечниках.
‡ Опухоли яичника, продуцирующие избыток андрогенов (например, из клеток Ляйдига — лейдигомы, синтезирующей тестостерон).
‡ Недостаточность 3βгидроксистероиддегидрогеназы. Недостаточность этого фермента приводит к избыточный содержанию в организме дегидроэпиандростерона.
† Проявления: повышение содержания в крови андростендиона и тестостерона, увеличение показателя соотношения в крови гонадотропинов (ЛГ/ФСГобычно более 3), гирсутизм, аменорея, бесплодие, ожирение.
• Гиперэстрогения. Характеризуется избыточным образованием и/или эффектами эстрогенов в организме.
† Наиболее частая причина: повышение содержания в крови андрогенов яичникового и/или надпочечникового генеза. Андрогены в коже и жировой ткани трансформируются в эстрогены, что ведёт к увеличению их концентрации в крови.
† Проявления: повышение в крови и моче содержания эстрогенов, снижение уровня гонадотропных гормонов (по механизму обратной связи), преждевременное половое созревание девочек по изосексуальному типу, ускоренный рост организма (опережающий возрастную норму), нарушения менструального цикла, обычно в виде меноррагии. Последняя обусловлена длительно повышенным уровнем эстрогенов и нарушением периодических колебаний содержания прогестерона в крови.
ЭНДОКРИНОГЕННЫЕ НАРУШЕНИЯ ПОЛОВОГО РАЗВИТИЯ И ПОЛОВОЙ ФУНКЦИИ У ЛИЦ ГЕНЕТИЧЕСКИ МУЖСКОГО ПОЛА
Пубертатный период у мальчиков начинается в возрасте от 9,5 до 13,5 лет и продолжается около 3 лет. Увеличение яичек обычно является первым признаком полового созревания. К другим признакам полового созревания необходимо добавить акне, пубертатную гинекомастию и ряд др.
• Пубертатная гинекомастия — развитие молочных желёз у подростков (как правило, одностороннее и в виде субареолярного утолщения, протекает бессимптомно) — встречается у 60% подростков и обычно длится от 6 месяцев до двух лет.
• Варикоцеле — расширение вен семенного канатика — встречается у 15% подростков, чаще с левой стороны.
• Паховая грыжа у мужчин встречается в 5 раз чаще, чем у женщин; располагается, как правило, справа или с двух сторон.
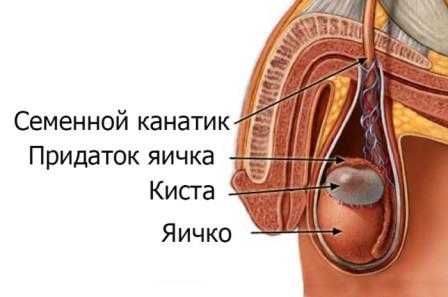
• Гидроцеле — заполненное жидкостью образование в оболочке семенного канатика, расположено в мошонке.
• Сперматоцеле — кистозное образование в составе придатков яичка, содержащее сперматозоиды.
Эндокриногенные нарушения полового развития и половой функции у лиц мужского пола проявляются следующими типовыми формами: преждевременное половое развитие, задержка полового развития, гипофункция яичек.
ПРЕЖДЕВРЕМЕННОЕ ПОЛОВОЕ РАЗВИТИЕ
Преждевременный (первичный) пубертат — состояние, характеризующееся появлением всех или отдельных вторичных половых признаков у мальчиков до 9летнего возраста. Нередко это сочетается с эмоциональными и поведенческими расстройствами, а также нарушением социальной адаптации. Различают истинное и ложное преждевременное развитие мальчиков.
• Истинное преждевременное развитие. Преждевременный пубертат является результатом гиперфункции гипоталамогипофизарной системы и характеризуется полным преждевременным половым развитием. Последнее включает вирилизацию и активацию сперматогенеза в яичках.
Причина: преждевременная активация секреции гонадолиберина нейронами гипоталамуса и, как следствие — гонадотропных гормонов аденогипофиза. Обычно развивается при опухолях в области заднего гипоталамуса, серого бугра, эпифиза, травматических повреждениях диэнцефальной области мозга, участвующей в синтезе гонадолиберинов; энцефалитах, состояниях и патологических процессах, повышающих внутричерепное давление (абсцессах, новообразованиях, гидроцефалиях, нарушении оттока ликвора и др.).
• Ложное пубертат у мальчиков. В отличие от первичного, ложное (вторичное) преждевременное половое развитие у мальчиков возникает в результате автономной гиперпродукции андрогенов или ХГТ. Характеризуется неполным преждевременным половым развитием: появлением признаков вирилизации, но без активации сперматогенеза.
В зависимости от соответствия или несоответствия полового развития генетическому полу преждевременное половое созревание подразделяют на изосексуальное (оно совпадает с генетическим полом и характеризуется признаками вирилизации мальчиков) и гетеросексуальное (не совпадает с генетическим мужским полом и сочетается с феминизацией мальчиков).
Наиболее частые причины: Андрогенпродуцирующие опухоли яичек (например, лейдигомы, синтезирующие тестостерон; сертолиомы и арренобластомы, образующие андрогены), гиперплазия клеток Ляйдига и синтез ими избытка тестостерона, увеличение содержания в крови андрогенов, секретируемых в коре надпочечников при их гиперплазии (чаще — врождённой) или поражении опухолью.
• Проявления преждевременного пубертата.
Проявления истинного и ложного преждевременного полового созревания являются результатом избытка в организме мужских половых гормонов. Это вызывает признаки вирилизации (появление лобкового и подмышечного оволосения, огрубение голоса, увеличение яичек и полового члена и др.; первые симптомы вирилизации могут наблюдаться уже в двухлетнем возрасте) и низкий рост (обусловлен преждевременным прекращением эпифизарного роста костей).
ЗАДЕРЖКА ПОЛОВОГО СОЗРЕВАНИЯ
Отсутствие у мальчиков признаков полового созревания к 14-летнему возрасту считается задержкой пубертата.
• Причины.
† Дефицит гонадолиберинов гипоталамуса и/или гонадотропинов аденогипофиза (при повреждении ядер гипоталамуса или гипофиза опухолями, в результате кровоизлияния или травмы, воспалительных процессов и др.).
† Сниженная выработка тестостерона яичками (в результате их травмы, роста новообразований, нарушения развития, воспаления яичек — орхита и т.п.).
† Пониженная чувствительность тканеймишеней к действию тестостерона.
• Проявления.
† Признаки евнухоидизма: недоразвитые яички и пенис, отсутствие или слабо выраженные вторичные половые признаки, женоподобный (девичий) голос, ожирение, диспропорция скелета (размах рук более чем на 6–8 см превышает рост, что обусловлено запаздыванием завершения эпифизарного роста трубчатых костей).
† Сниженное содержание тестостерона в крови (при нормальном уровне глобулина, связывающего половые гормоны).
МУЖСКОЙ ГИПОГОНАДИЗМ
• Причины тестикулярной недостаточности.
† Те же, что и при задержке полового развития мальчиков (см. выше).
† Дефекты яичек.
‡ Наследуемые или врождённые (первичные). Наблюдаются, например, у пациентов с различными вариантами синдрома Кляйнфелтера. При этом происходит снижение продукции андрогенов и нарушения сперматогенеза.
‡ Приобретённые (вторичные). Развиваются при травме, вирусном или бактериальном воспалении, нарушении кровообращения, воздействии радиации, ЛС (например, наркотиков, спиронолактона, циметидина) и других воздействий.
• Проявления. Половое развитие у мужчин не нарушено. В связи с этим телосложение и тембр голоса у них в диапазоне нормы. Наряду с этим выявляется снижение полового влечения, импотенция, бесплодие — неспособность мужчины к зачатию ребёнка на протяжении одного года регулярной половой жизни без использования контрацептивов и независимо от возможности совершения полового акта (не менее 35% случаев бесплодия обусловлено нарушением половой функции мужчин; характеристика мужского бесплодия приведена в статье «Бесплодие» приложения «Справочник терминов»).
НАРУШЕНИЕ ФУНКЦИЙ ШИШКОВИДНОЙ ЖЕЛЕЗЫ
Шишковидная железа (эпифиз) — небольшой (5–8 мм) конической формы вырост промежуточного мозга, соединённый ножкой со стенкой третьего желудочка. Паренхима органа состоит из пинеалоцитов и интерстициальных (глиальных) клеток. В интерстиции присутствуют отложения солей кальция, известные как мозговой песок. Орган снабжён многочисленными постганглионарными нервными волокнами от верхнего шейного симпатического узла и содержит значительное количество серотонина (синтезируется преимущественно в дневные часы).
Функция органа у человека изучена слабо, хотя железа у ряда позвоночных выполняет различные функции (например, у некоторых амфибий и рептилий эпифиз содержит фоторецепторные элементы — так называемым теменной глаз). Эпифиз у человека, скорее всего, — звено реализации биологических ритмов, в том числе околосуточных (см. статьи «Ритм околосуточный» и «Мелатонин» в приложении «Справочник терминов»).
НАРУШЕНИЯ ЭНДОКРИННОЙ ФУНКЦИИ ТИМУСА
Из эпителиальных клеток стромы вилочковой железы выделено несколько групп полипептидов, демонстрирующих in vitro и в некоторых случаях in vivo самые различные гормональные эффекты, в первую очередь на созревание и дифференцировку T–лимфоцитов. Характеристика этих гормонов приведена в статье «Гормоны тимуса» (приложение «Справочник терминов»).
| ГЛАВА 28. ПАТОЛОГИЯ НЕРВНОЙ СИСТЕМЫ |
Любой патологический процесс в нервной системе, ведущий к расстройству её деятельности, а также организма в целом, включая поведение и психику, начинается с повреждения гистологических элементов нервной системы, в первую очередь — нейронов (мембран, рецепторов, ионных каналов, вторых посредников, генетического аппарата). Именно на клеточном и молекулярном уровнях патологический процесс может быть либо купирован, либо стать инициальным звеном дальнейших нарушений нервной деятельности.
В то же время изучения нарушений жизнедеятельности отдельных нейронов недостаточно для понимания расстройств нервной системы в целом. Необходимо также изучать и оценивать межнейронные взаимоотношения (структурнофункциональные связи), складывающиеся как внутри отдельных нервных образований (ядер, нейронных сетей), так и между ними.
И наконец, формирование целостного представления о закономерностях расстройств нервной деятельности возможно лишь при системном анализе структурнофункциональной организации нервной системы у каждого конкретного пациента.
ОБЩАЯ ЭТИОЛОГИЯ
Общая этиология нарушений деятельности нервной системы рассматривает причины повреждения и условия, определяющие патогенный эффект причин её повреждения (факторы риска).
ПРИЧИНЫ ПОВРЕЖДЕНИЯ
Факторы, вызывающие повреждение элементов нервной системы, могут быть экзогенными и эндогенными.
• Экзогенные причины.
Экзогенные факторы имеют физическую, химическую, биологическую и психогенную природу.
† Физические (например, механическая травма, ионизирующая радиация, снижение или значительное увеличение pO2 во вдыхаемом воздухе).
† Химические (например, этиловый, метиловый и другие спирты; ядохимикаты: фосфорорганические соединения, применяемые в сельском хозяйстве, например, пестициды, в быту, например, хлорофос; нервнопаралитические отравляющие вещества, например, зарин; фармакологические препараты центрального действия, в том числе наркотики; токсины растительного происхождения, например, стрихнин, кураре).
† Биологические (например, нейротропные вирусы: возбудители бешенства, полиомиелита, герпеса; микробы: возбудители сифилиса, лепры; микробные токсины: ботулинический, дифтерийный, столбнячный).
† Психогенные (например, психотравмирующие ситуации, устрашающие образы, звуки, ощущения). Наиболее часто в клинической практике патогенную роль играет слово — как стрессорный раздражитель, а также другие воздействия, реализующие своё влияние условнорефлекторно, через вторую сигнальную систему.
• Эндогенные факторы.
Причины эндогенного характера, вызывающие повреждение нервной системы, перечислены на рис. 28–1.
Рис. 28–1. Эндогенные причины повреждения нервной системы.
ФАКТОРЫ РИСКА
К условиям, определяющим патогенность факторов, воздействующих на нервную систему (факторы риска) относят интенсивность, длительность, частоту и периодичность воздействия, а также состояние нервной системы в момент действия патогенного агента и состояние гематоэнцефалического барьера.
• Интенсивность, длительность, частота и периодичность воздействия. Значительные и труднообратимые нарушения нервной деятельности могут возникать не только под влиянием сильных, но и слабых патогенных факторов при определённых режимах их воздействия. Например, небольшие дозы алкоголя, наркотиков, ЛС при достаточной продолжительности и частоте их потребления способны вызывать грубые нарушения ВНД, движений, чувствительности и другие нейрогенные расстройства.
• Состояние нервной системы в момент действия патогенного агента. Состояние нервной системы в момент действия патогенного агента определяется её генетическими особенностями (например, типом ВНД) и предшествующими структурнофункциональными повреждениями. Клинические проявления последних к моменту действия данного патогенного фактора могут быть компенсированными (скрытыми) или носить характер следовых реакций, На таком фоне патогенность повреждающих воздействий увеличивается.
• Состояние гематоэнцефалического барьера. Патологическая проницаемость гематоэнцефалического барьера для экзо и эндогенных факторов может возникать при действии ионизирующей радиации, интоксикации спиртами, микробными токсинами, в условиях охлаждения организма, развития тяжёлых стрессовых ситуаций, различных шоковых состояний. Особое значение повышение проницаемости гематоэнцефалического барьера имеет для нарушения иммунной автономии головного мозга и развития вследствие этого состояний иммунной аутоагрессии с поражением нервной системы (например, рассеянного склероза, энцефаломиелита).
ОБЩИЙ ПАТОГЕНЕЗ РАССТРОЙСТВ НЕРВНОЙ ДЕЯТЕЛЬНОСТИ
В этом разделе рассмотрены механизмы повреждения нейронов и нарушения межнейронных взаимодействий, а также механизмы расстройств интегративной деятельности нервной системы.
ПОВРЕЖДЕНИЕ НЕЙРОНОВ
Механизмы повреждения нейронов могут носить специфический и неспецифический характер.
НЕСПЕЦИФИЧЕСКИЕ МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ НЕЙРОНОВ
Общие механизмы повреждения клеток рассмотрены в главе 4 «Патология клетки». Такие неспецифические механизмы повреждения нейронов представлены на рис. 28–2.
Рис. 28–2. Основные механизмы повреждения нейронов (неспецифические).
• Нарушения энергообеспечения. Возникают при уменьшении поступления в мозг глюкозы и кислорода, снижении активности ферментов биологического окисления, разобщении процессов окисления и фосфорилирования, нарушениях транспорта энергии и расстройствах процессов использования энергии.
† Уменьшение поступления в клетки глюкозы и кислорода.
Наиболее частые причины: гипоксемия, гипогликемия, анемия, снижение мозгового кровообращения, увеличение диффузионного пути глюкозы и O2 от микрососуда до нейронов (при отёке мозга).
Глюкоза является основным энергетическим субстратом нервных клеток. Аэробное расщепление субстратов обеспечивает образование примерно 80% энергии, потребляемой мозгом.
В норме головной мозг утилизирует около 20% глюкозы плазмы крови и всего потребляемого организмом кислорода.
Мозг чрезвычайно чувствителен к сокращению поступления кислорода.
Наличие в нервных клетках гликогена как резервного источника энергии лишь отчасти обеспечивает функционирование жизненно важных отделов нервной системы.
В конечном итоге дефицит глюкозы и кислорода приводит к гибели нервных клеток, в первую очередь нервных клеток коры головного мозга (корковые нейроны погибают при аноксии и при отсутствии глюкозы в течение минут).
† Снижение активности ферментов биологического окисления. Наиболее частые причины: ингибирование и/или денатурация ферментов (например, при отравлении цианидами и солями тяжёлых металлов, при эндогенной интоксикации), недостаточность ферментов (например, при генетических дефектах, авитаминозах B1, B2), нарушение компартментализации (например, при дезорганизации мембран митохондрий под воздействием ионизирующей радиации, высокой температуры, продуктов нарушенного обмена).
† Разобщение процессов окисления и фосфорилирования. Наиболее частые причины: избыток в нейронах Ca2+ и накопление жирных кислот.
† Нарушение транспорта энергии от мест образования макроэргических соединений до мест расходования энергии. Одна из наиболее частых причин: потеря нейронами BBфракции КФК при повреждении их мембран.
† Расстройство процессов использования энергии. Наиболее частая причина: снижение активности АТФаз (в условиях ацидоза, интоксикации, ионного дисбаланса).
• Расстройства синтеза белка.
† Наиболее частые причины: дефицит аминокислот, нарушения энергообеспечения, снижение активности ферментов протеосинтеза, распад синтезирующего белок органоида — шероховатой эндоплазматической сети (субстанции Ниссля).
† Проявления. Расстройства синтеза белка приводят к катастрофическим последствиям для всех стороны жизнедеятельности нервных клеток и — в итоге — к их гибели.
• Дисбаланс ионов и жидкости. Ионный гомеостаз нейронов обеспечивается работой энергозависимых калиевых, натриевых, кальциевых и других ионных каналов.
† Типичные проявления ионного дисбаланса (возникающие, например, при энергодефиците): накопление Na+ и Ca2+ в нейронах и избыток K+ во внеклеточном пространстве.
† Последствия: стойкая деполяризация плазмолеммы нейрона (приводит к прекращению нормальной функции нервных клеток), повышение осмотического давления в нейронах, их набухание и последующая гибель.
• Повреждение мембран нейрона. Этот процесс является универсальным механизмом большинства нарушений нервной деятельности.
† Наиболее частые причины: чрезмерное образование активных форм O2 и усиления СПОЛ, активации эндогенных фосфолипаз, механическое растяжение мембран, воздействие на мембраны амфифильных соединений.
† Последствия. Повреждение мембран возбудимых клеток быстро приводит к прекращению их функциональной активности (электрогенез), нарушению всех проявлений жизнедеятельности нервных клеток (например, синаптическая передача, синтез белка, аксонный транспорт и др.) и их гибели путём аутолиза и апоптоза (см. раздел «Гибель клетки» в главе 4 «Патология клетки»).
• Апоптоз. Важная роль апоптоза — генетически контролируемого процесса гибели нейронов — доказана для многих форм невропатологии, особенно для нейродегенеративных заболеваний (например, для болезней Паркинсона, Альцхаймера; старческой деменции; бокового амиотрофического склероза и др.).
† Причины: гипоксия нервной ткани любого типа, особенно действующая длительное время (например, при атеросклерозе церебральных сосудов; опухолях головного или спинного мозга, сдавливающих сосуды), внутриклеточный ацидоз (например, при значительной ишемии ткани мозга), избыточная генерация радикалов кислорода, липидов и других веществ в ткани мозга (например, в условиях гипоксии и/или гипероксигенации мозга, отравлении нейротоксическими агентами).
† Механизмы апоптоза изложены в разделе «Апоптоз» в главе 4 «Повреждение клетки».
Описанные выше механизмы повреждения нейрона тесно взаимосвязаны, они нередко потенцируют друг друга, образуя порочные круги (circulus vitiosus). Формирование таких порочных кругов — неспецифическая, стандартная реакция нейрона на разные патогенные воздействия.
СПЕЦИФИЧЕСКИЕ МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ НЕЙРОНОВ.
Патогенетическую основу большинства форм нарушений нервной деятельности составляют раздельные или сочетанные расстройства специфических для нейрона процессов метаболизма различных нейромедиаторов (рис. 28–3).
Рис. 28–3. Основные механизмы повреждения нейронов (специфические).
• Синтез нейромедиаторов. Наиболее частые причины нарушений синтеза нейромедиаторов: энергетический дефицит, дефицит субстратов синтеза, генетические дефекты ферментов синтеза, ингибирование ферментов синтеза.
• Аксонный транспорт нейромедиаторов. Наиболее частые причины нарушения аксонного транспорта рассмотрены далее (раздел «Механизмы нарушений межнейронных взаимодействий»).
• Секреция нейромедиатора (см. статью «Нейромедиаторы» в приложении «Справочник терминов»).
• Удаление нейромедиатора (см. статью «Нейромедиаторы» в приложении «Справочник терминов»).
• Взаимодействие нейромедиатора с его рецепторами (см. статью «Нейромедиаторы» в приложении «Справочник терминов»).
Реализация описанных выше неспецифических и специфических механизмов повреждения нейрона обусловливает нарушение восприятия, анализа, генерации и проведения возбуждения нейронами.
МЕХАНИЗМЫ НАРУШЕНИЙ МЕЖНЕЙРОННЫХ ВЗАИМОДЕЙСТВИЙ
Механизмы нарушений межнейронных взаимодействий приведены на рис. 28–4.
Рис. 28–4. Механизмы нарушений взаимодействия нейронов.
В основе нарушений межнейронных взаимодействий находятся расстройства физикохимических процессов и форм функционального взаимодействия нейронов.
РАССТРОЙСТВА ФИЗИКОХИМИЧЕСКИХ ПРОЦЕССОВ
Существует несколько вариантов расстройств физикохимических процессов, обеспечивающих межклеточные взаимодействия в нервной системе. К ним относятся нарушения мембранного электрогенеза (включая проведение ПД по аксонам), синаптической передачи (включая секрецию и рецепцию нейромедиатора), а также нарушения аксонного транспорта.
РАССТРОЙСТВА ФОРМ ФУНКЦИОНАЛЬНОГО ВЗАИМОДЕЙСТВИЯ НЕЙРОНОВ
Среди межнейронных функциональных взаимодействий выделяют жёстко детерминированную и вероятностностатистическую формы.
• Жестко детерминированная (жёстко программная) — стандартная форма ответной реакции определяется генетически запрограммированными особенностями реагирования нейронов на воздействия и наличием анатомических связей между нейронами, составляющими ту или иную функциональную совокупность (ядра, проводящие пути, нейронные сети и т.п.).
• Стохастическая (вероятностностатистическая) форма реакции нейронов означает, что один и тот же стимул может вовлекать в ответные реакции разные нейроны или вызывать неодинаковые ответы. Зависимость между воздействием и ответной реакцией носит вероятностный характер. В основе этой формы взаимодействия лежат изменчивость текущего функционального состояния нейронов и функциональная избыточность нейронов и связей между ними. Стохастичность межнейронного взаимодействия обеспечивает высокую функциональную пластичность, а также значительные компенсаторноприспособительные возможности нервной системы, предотвращающие возможность «случайных» патогенных последствий различных воздействий.
• В норме обе формы межнейронного взаимодействия сбалансированы и дополняют друг друга. Нарушение этого баланса приводит к расстройствам нервной деятельности. Например, в агональной стадии процесса умирания наблюдается переход нейронов дыхательного центра на жёсткопрограммный режим деятельности. Обеспечивая необходимый минимум лёгочной вентиляции, дыхательный центр утрачивает возможность реагирования на дополнительные воздействия. В условиях дефицита энергии дыхательный центр не реагирует на афферентные стимулы от синокаротидных рефлексогенных зон, рецепторов растяжения лёгких и других регионов. Такое состояние дыхательного центра обозначают как его «функциональная деафферентация».
МЕХАНИЗМЫ РАССТРОЙСТВ ИНТЕГРАТИВНОЙ ДЕЯТЕЛЬНОСТИ НЕРВНОЙ СИСТЕМЫ
Механизмы расстройств интегративной деятельности нервной системы заключаются в нарушениях функционирования одного или нескольких звеньев нервной системы: афферентного, центрального и эфферентного.
• Афферентные нарушения могут быть связаны с расстройствами восприятия различных воздействий и проведения сигнала от афферентных структур к нервным центрам.
studfiles.net