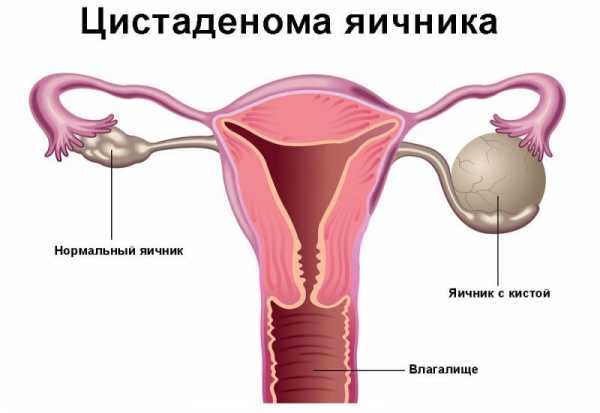
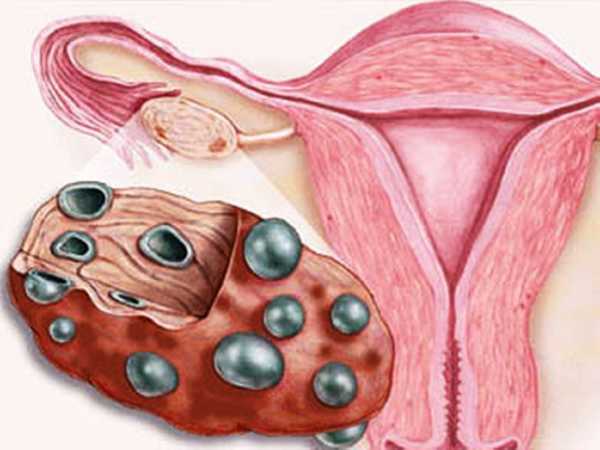
Функциональная недостаточность яичников
Особенности, возможные причины и пути лечения недостаточности яичников
Яичники — важнейшие органы женской половой системы. Начиная с подросткового возраста они активно функционируют до самой менопаузы. Недостаточность функции половых желез критическим образом отражается на общем состоянии здоровья и самочувствии женщины.
Работа яичников регулируется гипоталамо-гипофизарным комплексом посредством гормонов. Это сложный многоступенчатый механизм, и нарушение на любом этапе может его нарушить. Выделяют первичную и вторичную недостаточность функции яичников: первичная связана с патологией самих органов, вторичная — со сбоями в работе эндокринной регулирующей системы. Вторичная яичниковая недостаточность в большинстве случаев является следствием серьезных заболеваний аденогипофиза или гипоталамуса.
Первичная недостаточность функции яичников
Заболевание имеет множество названий: истощение половых желез, дисгенезия яичников, гипогонадизм, также оно известно как преждевременная менопауза. Суть его в том, что у молодых репродуктивно активных женщин проявляются признаки, характерные для постменопаузального периода.
С возрастом запас яйцеклеток в половых железах, заложенный еще в эмбриональном периоде развития, подходит к концу. Это естественное истощение, после которого наступает менопауза, заканчивается репродуктивный период в жизни женщины, угасает функция яичников. Случается, однако, так, что это событие происходит значительно раньше, чем ожидается.
Яичники молодых женщин иногда перестают нормально функционировать, прекращается циклическое созревание фолликулов. Заболевание может быть вызвано разными факторами. Разумеется, забеременеть при этом невозможно. Недостаточность функции яичников — одна из основных причин женского бесплодия (эндокринное бесплодие).
Можно выделить несколько разновидностей первичной яичниковой недостаточности:
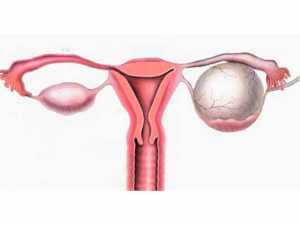
- Синдром преждевременного истощения половых желез. Патология вызвана генетическими нарушениями, агрессивными факторами среды (облучение) или травмирующими воздействиями на яичники (например, в ходе операции). При этом заболевании уменьшается или истощается число активных фолликулов.
- Синдром резистентных половых желез. В отличие от предыдущей патологии в резистентных яичниках находится достаточное количество фолликулов, которые потенциально могли бы созреть и овулировать. Проблема заключается в том, что половые железы невосприимчивы к действию гормонов. Гипофиз посылает фолликулам сигнал к развитию, но они по каким-то причинам не выполняют его. Развитие заболевания приводит к стабильному прекращению функции яичников.
- Дисгенезия половых желез. Под этим термином объединяется несколько генетических нарушений, связанных с нарушением структуры яичников.
Преждевременная недостаточность функции половых желез встречается достаточно часто. Так, каждый десятый случай аменореи вызван именно этой патологией.
Причины патологии
- врожденные генетические нарушения (в т.ч. наследственные), патологии беременности (гормональный дисбаланс, воспалительные заболевания у матери, вынашивающей девочку);
- аутоиммунные процессы, такие как аутоиммунный тиреоидит, ревматоидный артрит, в результате которых организм вырабатывает антитела к тканям половых желез;
- воздействие агрессивных внешних факторов (облучение, химические вещества, в т. ч. лекарства, лучевая терапия, химиотерапия);
- травмы яичников, повреждения во время оперативных вмешательств;
- хронические воспалительные процессы в половой системе, туберкулез половых желез.
Симптомы яичниковой недостаточности
Заболевание яичников протекает на фоне нарушенного гормонального фона организма и может сопровождаться характерными признаками климакса, вызванными снижением уровня эстрогена.
- При первичной недостаточности органа отмечается повышение уровня фолликулостимулирующего гормона (ФСГ), при вторичной, наоборот, отмечается падение уровня ФСГ и ЛГ (лютеинизирующий гормон, ответственный за овуляцию фолликула).
- Падает продукция эстрогенов патологическими яичниками.
- Недостаточность функции половых желез проявляется нарушением месячного цикла, отсутствием менструаций (аменореей).
- Повышенная потливость и приливы жара.
- Снижение сексуального желания, перепады настроения, нарушения сна, раздражительность, депрессии.
- Сухость слизистых оболочек наружных половых органов.
Врожденная гипофункция половых желез приводит к задержке полового созревания у девочек. Наблюдается недоразвитие половых желез, нестабильный цикл, олигоменорея или аменорея.
В тяжелых случаях заболевание сопровождается серьезными поражениями органов половой системы.
Диагностика
Несмотря на большое количество литературы, посвященной недостаточной функции половых желез, диагностика этого состояния вызывает существенные затруднения у специалистов. На основании одних лишь жалоб пациентки невозможно определить проблему. Необходимо точно установить первопричину заболевания, для этого проводится ряд исследований:
- ультразвуковое исследование яичников позволяет визуализировать структуру органов, оценить активность фолликулов;
- кариотипирование проводится для выявления серьезных генетических нарушений (многие генетические заболевания имеют характерные внешние проявления, по которым их можно диагностировать или хотя бы заподозрить);
- выявление аутоантител (антител, вырабатываемых организмом к собственным тканям) к половым железам;
- анализ крови на уровень гормонов.
Неинформативными являются такие методы как биопсия и лапароскопическая диагностика. Наличие фолликулов в яичнике, которое может быть обнаружено в ходе этих исследований, не гарантирует их нормального развития и созревания.
Диагноз преждевременной недостаточности половых желез ставится женщинам моложе 40 лет, у которых в течение 4 месяцев и дольше наблюдается нарушение функции яичников, а показатели гормонов не соответствуют норме.
Лечение заболевания
Полвека назад эндокринное нарушение функции яичников считалось неизлечимым заболеванием. Известно, однако, что у некоторых пациенток с синдромом резистентных яичников иногда происходят спонтанные овуляции фолликулов. 5-10% женщин, страдающих преждевременной недостаточностью половых желез, способны забеременеть даже через много лет после обнаружения заболевания.
Невозможно сказать, когда будет преодолен тот критический рубеж, после которого восстановление функции яичников будет невозможно. Также, к сожалению, невозможно достоверно предсказать, в какой момент может наступить овуляция.
Лечение направлено на восстановление нормального эндокринного и генетического статусов. Основной метод — гормональная терапия, призванная восполнить недостаток эстрогенов в организме пациентки. Дополнительно проводится профилактика остеопороза, который является распространенным осложнением заболевания, препаратами кальция и витамина Д.
Стимуляция овуляции медикаментозными методами в большинстве случаев не приносит положительных результатов.
Заболевания половой сферы, диагностированное бесплодие — серьезное испытание для женщины. Ведение таких пациенток требует от врача высокой профессиональной компетентности и тактичности.
Гипофункция яичников и ЭКО
Женщины, страдающие синдромом истощенных или резистентных яичников, могут забеременеть с помощью процедуры экстракорпорального оплодотворения (ЭКО), в ходе которой оплодотворенная донорская яйцеклетка помещается в полость матки пациентки.
Сначала проводится подготовительная гормональная терапия препаратами эстрадиола, прогестерона, гестагенов.
Эффективность ЭКО зависит от возраста, состояния здоровья женщины и техники проведения процедуры.
Гипофункция яичников — комплексная патология, которая требует пристального внимания и адекватного лечения. Во многих случаях заболевание не является неизлечимым, возможны спонтанные всплески активности половых желез, во время которых пациентка может забеременеть.
Будьте здоровы!
Важно знать! ×aginekolog.ru
Первичная яичниковая недостаточность как причина бесплодия
 Первичная яичниковая недостаточность - это форма эндокринного бесплодия, характеризующаяся нарушением функции яичников. Данная патология заключается в отсутствии фолликулов или нарушении их созревания в ответ на гормональную стимуляцию. Подробная информация о яичниках и их роли в репродуктивной системе женщины изложена в статьях – «Бесплодный брак. Репродуктивная система женщины.» и «Бесплодный брак. Физиология женской репродуктивной системы.»
Первичная яичниковая недостаточность - это форма эндокринного бесплодия, характеризующаяся нарушением функции яичников. Данная патология заключается в отсутствии фолликулов или нарушении их созревания в ответ на гормональную стимуляцию. Подробная информация о яичниках и их роли в репродуктивной системе женщины изложена в статьях – «Бесплодный брак. Репродуктивная система женщины.» и «Бесплодный брак. Физиология женской репродуктивной системы.» Частота встречаемости
Синдромы преждевременного истощения и резистентных яичников встречаются примерно у 10% женщин с отсутствием менструации. Дисгенезия гонад – данное заболевание встречается относительно редко - в 1 случае из 10 000.Виды яичниковой недостаточности:
• синдром истощения яичников (это генетическая патология, характеризующаяся преждевременным исчезновением циклических физиологических гормональных изменений в организме, что приводит к преждевременному наступлению климакса)
• синдром резистентных яичников (при этой патологии утрачен контроль эндокринной системы за функциональной активностью яичников) • дисгенезия гонад (ряд наследственных заболеваний для которых характерно нарушение структуры половых желёз)Причины возникновения бесплодия:
Причинами развития яичниковой недостаточности могут быть:• Генетические нарушения: приводящие к замещению яичников соединительной тканью, или же дефект гена, кодирующего функцию рецептора к ФСГ. Это явление приводит к резистентности (устойчивости) фолликулярного аппарата к данному гормону, что препятствует созреванию фолликула и овуляции.
• Аутоиммунные процессы в организме (аутоиммунный тиреоидит, ревматоидный артрит и др.), приводящие к появлению антител к тканям яичника.
• Ятрогенные причины (следствия ранее перенесенных видов лечения): лучевая терапия, оперативные вмешательства на яичниках, химиотерапия.
• Хроническое воспаление яичников, в особенности туберкулёза половых органов.
Механизм развития
Повреждение рецепторного аппарата фолликулов (особенно рецепторов к ФСГ) вследствие вышеуказанных причин приводит к отсутствию ответа на циклические выбросы ФСГ, прекращению роста фолликулов, отсутствию овуляции, дефициту эстрогенов, что по принципу обратной связи вызывает повышение секреции гонадотропных гормонов гипофизом.
Диагностика
Результаты клинического обследования Характерны жалобы на приливы, нерегулярный цикл или его отсутствие, бесплодие. Как правило, первичная яичниковая недостаточность является следствием генетических аномалий – потому, по клинической картине (аркообразное нёбо, крыловидные складки на шее, широкая грудная клетка) легко выявить наличие грубых генетических заболеваний. Что подтверждается при генетическом обследовании – кариотипировании. Женщины с истощёнными или резистентными яичниками имеют нормальный женский внешний вид, но УЗИ исследование выявляет отсутствие созревающих фолликулов.Лабораторно – инструментальные исследования:
• Кариотипирование – позволяет выявить грубые генетические заболевания. • Выявление аутоантител к яичниковой ткани – позволяет выявить причину яичниковой недостаточности, если она заключается в аутоиммунном поражении яичников. • Ультразвуковая оценка структуры яичников – данное исследование позволяет выявить активность фолликулов яичников.Лечение бесплодия
Стимуляция овуляции с целью лечения данного вида бесплодия не показана ввиду ее бесперспективности. Единственный метод достижения беременности - перенос оплодотворённой донорской яйцеклетки в полость матки. Для данного вида зачатия необходима донорская яйцеклетка, получаемая в процессе донации от здоровой женщины.
Донация складывается из двух этапов:
• подготовительный этап, цель которого - увеличение размеров матки, рост эндометрия, формирование рецепторного аппарата в матке.
• собственно цикл донации.
Подготовительный этап. Заместительную терапию половыми гормонами с целью профилактики и коррекции эстрогендефицитных состояний проводят при гонадотропной недостаточности. Производится следующими препаратами: эстрадиол, гестагены, дидрогестерон, прогестерон.
Собственно цикл донации сопровождается назначением гормональных препаратов: эстрадиол, прогестерон.
При положительном тесте на беременность заместительную терапию эстрогенами и гестагенами продолжают до 12 недель.Прогноз:
Эффективность переноса донорских эмбрионов достигает 25-30% за попытку. Эффективность не зависит от причины возникновения яичниковой недостаточности, а определяется возрастом женщины, «качеством» донорских яйцеклеток и адекватностью подготовки эндометрия к имплантации. Перед применением необходимо проконсультироваться со специалистом.Автор: Ткач И.С. врач, хирург офтальмолог
Вернуться к началу страницы
ВНИМАНИЕ! Информация, размещенная на нашем сайте, является справочной или популярной и предоставляется широкому кругу читателей для обсуждения. Назначение лекарственных средств должно проводиться только квалифицированным специалистом, на основании истории болезни и результатов диагностики.www.tiensmed.ru
Недостаточность яичников
Источник: «Спортивная медицина» Автор: Под ред. С.П. Миронова, 2013 г.
В современной гинекологии недостаточность яичников рассматривают во взаимосвязи с гипергонадотропной, нормогонадотропной и гипогонадотропной функциями центральных звеньев регуляции репродуктивной системы.
Эти термины не обозначают конкретных заболеваний, но их используют в качестве предварительных диагнозов, в известной мере определяющих методы дальнейшего обследования и лечения. Каждый из них включает целый ряд нозологических форм, различающихся по причинам, клиническим признакам, прогнозу и подходам к лечению.
Гипергонадотропная недостаточность яичников
Под гипергонадотропной недостаточностью яичников понимают количественный недостаток фолликулов, вплоть до их полного отсутствия, при котором циклическая деятельность яичников становится невозможной. Дефицит фолликулов может быть врожденным, но специфические клинические признаки возникают лишь в пубертатном периоде. Примером естественного гипергонадотропного состояния служит период постменопаузы. Общими признаками всех форм гипергонадотропной недостаточности яичников считают снижение концентрации эстрадиола и повышение содержания гонадотропинов [лютропина и фолликулостимулирующего гормона (ФСГ)] в крови. Среди клинических симптомов нередко присутствует первичная аменорея и задержка полового развития. В случае обнаружения повышенного содержания гонадотропных гормонов при вторичной аменорее больные, как правило, указывают на своевременное наступление менархе. Это свидетельствует о том, что нормальный возраст наступления менструаций не исключает грубых патологических изменений яичников.
Яичники, лишенные гамет, не могут в нормальном количестве синтезировать стероидные гормоны. Ниже перечислены причины развития гипергонадотропных состояний.
- Аномальный кариотип. Чаще всего его формирование связано с аномалиями половых хромосом. Возможны следующие варианты: тестикулярная феминизация (46 XY), синдром Шерешевского-Тернера (45 X0), мозаичные (45 X, 46 XX, 47 XXX) и смешанные (например, 45 X, 46 XY, 47 XXY) формы дисгенезии гонад. Дисгенезия гонад может быть следствием структурных аномалий хромосомы X: утраты части длинного или короткого плеча, изохромосомы по длинному или короткому плечу и др. Дисгенетические гонады обычно представлены соединительнотканными тяжами. Количество фолликулов в яичниках может варьировать от нормального до полного отсутствия, что, в свою очередь, манифестирует неизмененной репродуктивной функцией, вторичной или первичной аменореей. Классическая моносомия 45 Х0 характеризуется типичными внешними признаками (низкорослость, крыловидные кожные складки на шее и др.) Присутствие в кариотипе хромосомы Y может приводить к асимметрии в строении гонад, при этом одна из них представлена дисгенетическим семенником. В этом случае обычно отсутствуют низкорослость и другие стигматы, характерные для чистой дисгенезии. С практической точки зрения чрезвычайно важно, что присутствие хромосомы Y или ее части в хромосомном наборе резко повышает риск малигнизации дисгенетических гонад. Прогрессирующая вирилизация может оказаться симптомом гормонально активной опухоли. При первичной аменорее хромосомные аберрации обнаруживают примерно у 70% больных, но вторичная аменорея также нередко оказывается следствием хромосомных аномалий. Недостаточностью яичников сопровождаются некоторые хромосомные заболевания, связанные с аутосомами (например, синдром Дауна ).
При дисгенезии гонад в 20% случаев отмечают неполное развитие молочных желез и в 8% - однократные или повторные менструации, что нередко приводит к отсрочке начала обследования на неопределенный срок, в течение которого могут произойти необратимые изменения костной ткани. Продолжительность периода сохраненной менструальной функции пропорциональна числу интактных фолликулов. Беременность, наступившая у женщин с количественными или структурными аномалиями половых хромосом, лишь в 30% случаев заканчивается рождением здорового ребенка. Поскольку центральным звеном патогенеза всех форм гипергонадотропной первично-яичниковой недостаточности служит дефицит эстрогенов, у девочки нарушается формирование вторичных половых признаков и скелета. Могут возникать симптомы, характерные для климактерических расстройств (астения, раздражительность, депрессия, приливы, лабильность пульса и АД, атрофический кольпит и др.).
- Моногенные и полигенные наследственные аномалии. К агенезии или гипоплазии гонад приводит галактоземия, наследуемая по аутосомнорецессивному типу. Описаны формы аутосомно-доминантно и аутосомнорецессивно наследуемой дисгенезии гонад в сочетании с аномалиями развития глазных щелей или нейросенсорной глухотой. Помимо этого, существуют формы патологических изменений яичников, характеризующиеся наследственной предрасположенностью.
- Инфекционное, токсическое и радиационное поражение гонад. Недостаточность яичников могут вызвать прием цитостатических средств, овариоэктомия и резекция яичников.
- Аутоиммунный оофорит. Как правило, он сочетается с другими аутоиммунными заболеваниями и манифестирует вторичной гипергонадотропной аменореей.
- Синдром резистентных яичников характеризуется возникновением первичной или вторичной гипергонадотропной аменореи у женщин с сохраненным, но функционально неактивным фолликулярным аппаратом яичников. Среди причин этого заболевания выделяют секрецию гипофизом биологически неактивных гонадотропинов, нарушение рецепции ФСГ гранулезными клетками, ферментативные нарушения (например, дефицит α-гидроксилазы, при котором нарушается синтез эстрогенов) и др.
- Гонадотропинсекретирующая аденома гипофиза.
Обследование и ведение больных. Любая форма задержки полового развития, первичная, вторичная аменорея и нарушения менструального цикла требуют обязательного определения в крови содержания ФСГ и лютропина. Во всех случаях обнаружения повышенной концентрации гонадотропных гормонов необходимо соблюдать определенный алгоритм обследования. Выполняют УЗИ органов малого таза, кариотипирование, лапароскопию с биопсией гонад, рентгенографию области турецкого седла и определяют содержание антиовариальных антител. Существуют следующие принципы лечения гипергонадотропной яичниковой недостаточности.
- Оперативное удаление гонад с целью предотвращения их злокачественного перерождения у больных, в хромосомном наборе которых была обнаружена хромосома Y или ее фрагменты.
- Формирование вторичных половых признаков последовательным назначением эстрогенов и прогестагенов.
- Устранение эстрогенного дефицита с помощью заместительной гормональной терапии. Целесообразно назначать минимальные дозы эстрогенов в сочетании с прогестагенами с учетом конкретных клинических симптомов.
- При аутоиммунном оофорите менструальный цикл иногда можно восстановить с помощью назначения глюкокортикоидов.
- Хирургическое удаление или лучевая терапия аденомы гипофиза.
Гипергонадотропная недостаточность яичников у спортсменок
Особенности этого состояния у женщин, занимающихся профессиональным спортом, состоят в его исключительной распространенности среди этой категории пациенток и применяемых диагностических алгоритмах. Определенные фенотипические признаки при некоторых видах хромосомных нарушений (высокий рост, маскулинные черты и др.) могут служить критерием отбора девочек в спортивные группы, а в дальнейшем способствовать достижению более высоких спортивных результатов. В связи с этим до введения в Олимпийскую программу обязательного прохождения так называемого секс-контроля (кариотипирования) всеми участницами соревнований чемпионками нередко становились люди, имеющие смешанную форму дисгенезии гонад или тестикулярную феминизацию. В настоящее время такие патологические изменения у профессиональных спортсменок исключены. Остальные виды гипергонадотропной недостаточности яичников среди них регистрируют с той же частотой, что и в популяции, а более частое развитие первичной и вторичной аменореи объясняют другими причинами. Несмотря на то что среди причин задержки полового развития и аменореи у спортсменок доминирует гипоталамическая дисфункция, чрезвычайно важно помнить и о возможности существования гипергонадотропной первично-яичниковой недостаточности, поэтому прежде всего следует исключить это более тяжелое нарушение.
Гипогонадотропная недостаточность яичников
Гипогонадотропная недостаточность яичников - группа состояний, различных по этиологии и клиническим признакам и характеризующихся нарушением созревания фолликулов и снижением продукции гормонов в яичниках вследствие недостаточной гонадотропной стимуляции. Повреждение репродуктивной системы может происходить на уровне гипофиза, гипоталамуса или надгипоталамических структур ЦНС.
- Гипофиз.
- Первичный гипопитуитаризм - тяжелое заболевание, приводящее к инвалидности. Изолированный недостаток гонадотропных гормонов обнаруживают чрезвычайно редко. Обычно нарушается несколько тропных функций. Один из наиболее грозных симптомов - вторичная надпочечниковая недостаточность. Ниже перечислены возможные причины подобного нарушения.
- Послеродовой ишемический некроз. Необходимо учитывать, что гипопитуитаризм возникает при повреждении не менее 70% ткани гипофиза.
- Послеоперационный гипопитуитаризм, частота развития которого не превышает 3-4% и зависит от операционного доступа, размера и локализации аденомы. Гипопитуитаризм, развившийся после лучевой терапии, считают основным отдаленным осложнением (через 10 лет - в 50% случаев).
- Разрыв ножки гипофиза вследствие черепно-мозговой травмы.
- Гранулематозное или аутоиммунное поражение гипофиза.
- Синдром пустого турецкого седла.
- Опухоль гипофиза.
В связи с характерным анамнезом и клиническими признаками диагностика, как правило, не представляет затруднений. В неясных случаях можно провести пробу с тиролиберином или Гн-РГ. В ответ на их введение не происходит достаточного подъема концентрации соответствующих гормонов в крови. Лечение должно быть комплексным и направленным на компенсацию утраченных функций периферических эндокринных желез.
- Гипоталамус и надгипоталамические структуры ЦНС.
- Органические поражения гипоталамуса (аплазия и гипоплазия его отдельных участков, опухоли, воспалительные заболевания, черепно-мозговые травмы, разрыв сосудистых аневризм, гидроцефалия и др.). Признаками поражения гипоталамуса считают нарушения циркадных ритмов, пищевого поведения и терморегуляции, развитие несахарного диабета и атипичной гемианопсии. У большинства больных с изолированной гонадотропной недостаточностью установить органическую причину поражения гипоталамуса не удается.
- Врожденная ольфакторно-генитальная дисплазия.
- Хронические заболевания (особенно ЖКТ).
- Расстройства пищевого поведения (нервная анорексия).
- Депрессия.
- Психоэмоциональный стресс.
- Тяжелые физические нагрузки.
- Прием лекарственных препаратов.
Диагностика гипоталамической дисфункции не представляет труда. Тщательно собранный анамнез и полноценное физикальное обследование позволяют предположить наиболее вероятную причину нарушения. В крови обнаруживают низкую концентрацию лютропина, ФСГ, эстрадиола и прогестерона.
Этиотропное лечение направлено на устранение факторов, приведших к психоэмоциональному стрессу или снижению массы тела. Нередко в нем принимает участие психиатр. Патогенетическим лечением считают устранение гипоэстрогении и восстановление физиологических взаимоотношений в гипоталамо-гипофизарноовариальной системе с помощью назначения эстрогенных и комбинированных эстроген-гестагенных препаратов.
Гипогонадотропная недостаточность яичников у спортсменок
В то время как в общей популяции гипогонадотропная аменорея составляет 15-40% всех случаев аменореи, у спортсменок этот показатель превышает 90% и отражает высокую частоту гипоталамической дисфункции. Если повреждающий фактор спортивных тренировок начал действовать до наступления полового созревания, то нередко возникает задержка полового развития. Кроме того, недостаточная секреция гонадотропинов возможна и при таких менее выраженных нарушениях менструального цикла, как олигоопсоменорея, и даже при регулярных менструациях. Основными причинами нарушения гипоталамической функции у женщин-спортсменок принято считать дефицит жировой ткани и массы тела, психологический стресс и дефицит поступления энергии на фоне повышенных энергозатрат. Наиболее яркую клиническую картину отмечают при развитии ранее описанного синдрома «триада женщины-спортсменки», когда на фоне расстройств пищевого поведения и длительной аменореи прогрессирует остеопороз. Также существуют стертые формы недостаточности яичников, такие как хроническая ановуляция и недостаточность лютеиновой фазы на фоне сохраненного ритма менструаций, представленные широким спектром нарушений менструального цикла. Если женщина планирует беременность, то основной жалобой может быть бесплодие или привычное невынашивание.
Расстройство овуляции и недостаточность лютеиновой фазы - самые распространенные признаки недостаточности яичников у спортсменок, но, к сожалению, в большинстве случаев их диагностируют поздно. У 42% женщин с регулярным менструальным циклом, подверженных умеренным физическим нагрузкам, можно обнаружить недостаточность лютеиновой фазы, а у 16% - ановуляторные циклы, что в 4-5 раз превышает общепопуляционные показатели. Как известно, подобные нарушения в дальнейшем могут препятствовать реализации репродуктивной функции женщины, имеют системные последствия и обладают онкогенным потенциалом.
Нормогонадотропная недостаточность яичников
Синдром, включающий ряд различных по этиологии, патогенезу и клиническим признакам состояний. Нормальное содержание гонадотропинов при различных формах яичниковой недостаточности обнаруживают почти у всех женщин с сохраненным менструальным циклом и у значительной доли пациенток с аменореей. Факторы, приводящие к гипогонадизму, можно подразделить на внеовариальные и овариальные. К первой группе относят гиперпролактинемию (15%), избыточную массу тела (13,4%), дефицит массы тела (12,5%), надпочечниковую (8,4%) и овариальную (12%) гиперандрогенемию, первичный гипотиреоз (3%) и гипоталамическую недостаточность секреции Гн-РГ (менее 1%).
Поражения на овариальном уровне возникают при развитии нижеперечисленных состояний.
- Нормогонадотропная первично-овариальная недостаточность (19,2%). При этой форме овариальной недостаточности гипоталамо-гипофизарная регуляция функции яичников не нарушена, но существует дефект секреции эстрадиола доминантным фолликулом. Вторичные половые признаки развиты нормально, менархе может наступить несколько позже, чем у здоровых девушек, а основным симптомом чаще всего бывает ановуляция на фоне олигоопсоменореи или аменореи. Прекращению менструаций могут способствовать стрессовые факторы или снижение массы тела.
- Хронический неспецифический сальпингоофорит (11,2%)
- Генитальный эндометриоз (4,5%).
Клиническими признаками нормогонадотропной недостаточности яичников могут быть различные нарушения менструального цикла, вплоть до аменореи, бесплодие, гирсутизм и лакторея. В процессе обследования нередко обнаруживают поликистоз яичников.
Лечение зависит от того, какое заболевание лежит в основе яичниковой недостаточности. Для преодоления ановуляции и бесплодия используют антиэстрогенные препараты (кломифен). Перспективным считают кратковременное импульсное введение агонистов Гн-РГ под гормональным и эхографическим контролем за ростом фолликула. При обнаружении влияния внеовариальных факторов лечение должно быть направлено на их устранение. Кроме того, требуется восстановление нормальной массы тела. При адреногенитальном синдроме применяют глюкокортикоиды, при синдроме поликистозных яичников - эстроген-гестагенные препараты, синтетические агонисты Гн-РГ и антиандрогены, а при первичном гипотиреозе - тиреоидные гормоны. Повышенную концентрацию пролактина корректируют с помощью агонистов дофаминовых рецепторов (бромокриптин). Применение эстриола патогенетически обоснованно при нормогонадотропной первично-овариальной недостаточности, поскольку препарат способствует физиологическому процессу развития фолликула и не приводит к гиперстимуляции яичников.
Системные последствия недостаточности яичников у спортсменок
Диагностика функциональных изменений в центральных механизмах регуляции гипоталамо-гипофизарно-овариальной системы в клинической репродуктологии, к сожалению, представляет особую сложность. В то же время при несвоевременном обнаружении гормональной недостаточности возможно развитие тяжелых нарушений репродуктивного здоровья (бесплодие, невынашивание беременности, онкологические заболевания) и системных последствий (остеопороз, сердечнососудистые заболевания).
Как известно, за период полового созревания накапливается 48% скелетной массы, и дальнейший ее прирост продолжается до достижения возраста 30 лет. У спортсменок с задержкой полового развития этот процесс нарушен. Пролонгирование гипоэстрогенного состояния способствует более позднему закрытию зон роста, и минерализация костей задерживается. Если в период полового созревания по тем или иным причинам нарастание костной массы замедляется или останавливается, то в дальнейшем женщина никогда не достигнет пиковых значений плотности костной ткани, а ее потеря в перименопаузальном периоде начнется на фоне изначально пониженной плотности. При потере костной массы степень риска возникновения патологических переломов даже у юных спортсменок может достигать критических показателей.
По данным проспективных наблюдений, климактерический синдром у женщин, в молодые годы профессионально занимавшихся спортом, характеризуется большей частотой возникновения, более тяжелым течением и ранним (преждевременным) развитием остеопороза. Это связано с тем, что возрастная атрофия яичников начинается на фоне уже имеющейся недостаточности. Как правило, к моменту менопаузы такие женщины имеют достаточно длительный период гипоэстрогении. У многих из них в анамнезе есть указания на задержку полового развития и/или нарушения менструального цикла. В настоящее время существуют убедительные данные о том, что преждевременное развитие остеопороза в молодые годы необратимо даже на фоне полноценного лечения.
Оценка минеральной плотности костей у спортсменок показала, что ее значимое снижение можно наблюдать уже через 6 мес вторичной аменореи. У 50% женщин с нервной анорексией обнаружено значительное (до 2σ) отклонение минеральной плотности костей от нормы. Гипоэстрогения приводит к повышению активации новых единиц, ремоделирующих костную ткань, с одновременной утратой как соединительнотканных, так и минеральных элементов. Кроме того, снижение концентрации эстрогенов вызывает снижение активности 1α-гидроксилазы в почках, что ведет к нарушению продукции кальцитриола. Недостаточное поступление в организм кальция, белков и витамина D с пищей ускоряет развитие и усугубляет течение остеопороза. Обсуждают также роль в метаболизме костной ткани прогестерона, различных факторов роста и лептина. Наибольшие изменения отмечают в поясничных позвонках, в то время как трубчатые кости в меньшей степени подвержены влиянию гипоэстрогенных состояний. В литературе описаны клинические наблюдения, в которых минеральная плотность костей у спортсменок в возрасте 20-23 лет соответствовала таковой у женщин в возрасте 60-70 лет.
Парадокс состоит в том, что физические упражнения признаны одним из важнейших остеопротективных факторов, и, казалось бы, потери костной массы у спортсменок не должно быть. Действительно, в норме при регулярных физических нагрузках отмечают повышение костной плотности кортикального слоя функционально активных участков скелета (нижние конечности у легкоатлеток, фигуристок, балерин, позвонки у гребцов). Тем не менее при выраженном недостатке эстрогенов положительный эффект от физических упражнений нивелируется, и начинаются процессы резорбции кости, приводящие к остеопорозу.
Как известно, с хроническим недостатком эстрогенов нередко связано развитие сердечно-сосудистых заболеваний. Эстрогены обладают протективным влиянием на сосуды и сердце, во много раз снижая риск развития атеросклероза вследствие благоприятного влияния на обмен холестерина, липопротеидов, прямого уменьшения сосудистой резистентности и воздействия на репарацию поврежденной сосудистой стенки. Именно поэтому частота возникновения сердечно-сосудистых заболеваний возрастает у женщин после наступления менопаузы. Физические нагрузки per se также препятствуют развитию атеросклероза. Поскольку оценить результат влияния двух разнонаправленных факторов (гипоэстрогении и физических нагрузок) на состояние сердечно-сосудистой системы спортсменок сложно, достоверные данные по этой проблеме в литературе отсутствуют.
Повышенный риск развития онкологических заболеваний матки и молочных желез вследствие относительного или абсолютного недостатка прогестерона при нарушениях функций яичников связывают с эстрогенной стимуляцией тканеймишеней. Тем не менее убедительных данных о повышении онкологической заболеваемости среди женщин-спортсменок нет.
Принципы диагностики недостаточности яичников у женщин-спортсменок
После исключения хромосомно-генетических и органических нарушений и беременности, а также обнаружения признаков гипогонадотропной недостаточности яичников, имеющей непосредственную связь с физическими нагрузками, можно установить диагноз спортассоциированной аменореи и начать соответствующее лечение и профилактику отдаленных последствий.
Для «триады женщины-спортсменки» весьма характерны следующие признаки:
- жалобы на слабость, утомляемость, нерегулярные менструации или аменорею, боли в костях и нарушение осанки;
- объективно - сухость кожи и слизистых оболочек, ломкость волос и ногтей, при выраженных расстройствах пищевого поведения - брадикардия, аритмия, гипотензия, гипоплазия матки и молочных желез;
- при частой искусственно вызываемой рвоте - нарушение электролитного баланса (гипокалиемия, гипохлоремия), анемия, метаболический алкалоз, а при аменорее - снижение концентрации лютропина, ФСГ, эстрогенов и прогестерона (возможно повышение содержания тестостерона и кортизола);
- эхографически - признаки ановуляции, гипоплазии внутренних половых органов;
- рентгенологически - отставание костного возраста от паспортного, снижение σ (параметра стандартного отклонения).
Показатели денситометрии от -1 до -2,5 следует рассматривать как доклиническую форму остеопении, а отклонение σ более -2,5 свидетельствует о высоком риске возникновения переломов.
Ниже перечислены основные принципы диагностики «триады» и других репродуктивных расстройств и их последствий у спортсменок.
- Как можно более раннее обнаружение факторов риска, а не ярких клинических симптомов. Это связано с тем, что при развитии остеопороза высокой степени не всегда удается достичь желаемых показателей костной плотности даже при проведении комплексного лечения. Это обстоятельство автоматически определяет пациентку в группу риска дальнейшего тяжелого течения климактерического синдрома и постменопаузального остеопороза. Более того, выраженный остеопороз нередко приводит к инвалидизации даже юных спортсменок.
- Активное определение расстройств пищевого поведения и аменореи. Сама пациентка может не сообщить врачу об использовании ею нежелательных методов коррекции массы тела. Зачастую она считает похудание и аменорею весьма желанными состояниями. Кроме того, она может опасаться того, что назначенное лечение или восстановление менструального цикла повлияют на ее спортивные результаты, а также находиться в подавленном состоянии и не доверять врачу.
Целенаправленный подход к выделению групп риска. Следует учитывать следующие факторы:
- вид спорта;
- время максимально напряженных тренировочных режимов (период предсоревновательной подготовки);
- высокий уровень спортивного мастерства с повышенными требованиями к себе;
- начало тренировок в предпубертатном возрасте;
- низкая масса тела и ее значительные колебания в течение последнего года;
- чрезмерная озабоченность процессом питания, существование запретных продуктов и др.;
- особенности гинекологического анамнеза (возраст наступления менархе, нарушения менструального цикла, бесплодие);
- частые переломы в анамнезе, боли в костях, сколиоз и др.
Обнаружение каких-либо из перечисленных факторов риска должно направить диагностический поиск на прицельное определение расстройств пищевого поведения, репродуктивных нарушений и остеопороза.
- Вовлечение в диагностический процесс максимального числа женщин, занимающихся спортом. Оптимальные условия для скрининга создают во время медицинских осмотров накануне тренировочного года и/или соревнований. Именно поэтому становится очевидным, что основную роль в диагностике репродуктивных и связанных с ними расстройств у спортсменок выполняют врачи по спортивной медицине.
- Установление окончательного диагноза спортассоциированной аменореи должно происходить только после того, как будут исключены такие причины аменореи, как беременность, хромосомные нарушения или аномалии развития, опухоли или прием лекарственных препаратов. Гипоталамическая форма аменореи - диагноз исключения. При обнаружении нарушений репродуктивной функции женщину следует направить на консультацию к гинекологу.
- Слаженность работы врачей различных специальностей, преемственность на этапах диагностики, лечения и реабилитации, а также последующего диспансерного наблюдения. Это возможно только при знании указанного нарушения, понимании опасности его последствий и соблюдении принципов охраны репродуктивного здоровья каждой женщины.
Диагноз устанавливают на основании данных активного опроса, осмотра, антропометрии, физикального и гинекологического исследования, а также результатов инструментальных и лабораторных методов исследований.
Читайте также
sportguardian.ru
Овариальная недостаточность: лечение, симптомы, что это такое, причины, признаки
Овариальная недостаточность — патологическое состояние, которое проявляется исходным отсутствием, снижением или преждевременным прекращением овуляторной и секреторной функции яичников.
Овариальная недостаточность является результатом нарушения закладки, дифференцировки, развития, механизмов регуляции деятельности яичников или непосредственного их повреждения. Причины овариальной недостаточности многообразны.
Овариальная недостаточность — снижение секреции гормонов яичников, которая подразделяется на первичную (связанную с непосредственным поражением яичников) и вторичную (обусловленную снижением секреции гонадотропных гормонов, с симулирующих секрецию овариальных гормонов).
В некоторых случаях выделяют и третичную овариальную недостаточность, которая вызвана нарушением секреции гипоталамических гормонов, регулирующих секрецию гонадотропинов. Поскольку как клинического значения выделение третичной овариальной недостаточности не имеет, то обычно во вторичную неявно включают и третичную овариальную недостаточность.
Классификация овариальной недостаточности
- I. Первичная овариальная недостаточность (первичный гипогонадизм, гипергонадотропный гипогонадизм) является следствием патологии непосредственно яичников.
- II. Вторичная овариальная недостаточность связана со снижением или прекращением выработки гонадотропных гормонов и/или их стимулирующего влияния на функциональную активность яичников.
- III. Овариальная недостаточность, не связанная с поражением яичников и недостаточностью секреции гонадотропных гормонов (нормогонадотропный гипогонадизм).
Причины и патогенез овариальной недостаточности
Гипергонадотропная овариальная недостаточность может быть врожденной, в большинстве случаев обусловленной хромосомными и генетическими аномалиями, которые лежат в основе нарушения гонадной дифференцировки и полового развития. Приобретенные формы чаще всего связаны с инфекционным (корь, краснуха, герпес) и аутоиммунным поражением гонад, воздействием гонадотоксических (физических и химических), ятрогенных (овариоэкгомия, лучевая и химиотерапия) факторов.
В основе патогенеза гипергонадотропной недостаточности яичников лежит выраженный дефицит или полное отсутствие фолликулов и абсолютная эстрогенная недостаточность.
К наиболее распространенной врожденной патологии, обусловленной хромосомными аномалиями с нарушением закладки и дифференцировки яичников, относится дисгенезия гонад.
Для смешанной формы дисгенезии гонад характерны мозаичные варианты кариотипа с наличием Y-хромосомы (45XO/46XY, 45XO/47XXY и др.), при которых имеется асимметричное строение гонад: strek (стрек) — с одной стороны, а с противоположной стороны — тестикул.
Другим наследственным заболеванием, является синдром тестикулярной феминизации, обусловленный многочисленными мутациями гена-рецептора к андрогенам. Больные имеют мужской кариотип (46XY) и мужские гонады, но женский фенотип, что связано со структурным дефектом либо отсутствием рецепторов к андрогенам. Из-за отсутствия эффектов тестостерона и дигидротестостерона во внутриутробном периоде происходит дегенерация вольфова протока. При этом производные мюллеровых протоков не развиваются вследствие выработки яичками антимюллерова фактора. У таких больных уровень тестостерона в крови нормальный или сниженный, содержание эстрадиола — выше, чем у здоровых Мужчин.
Гипергонадотропная форма яичниковой недостаточности при аутоиммунном оофорите обусловлена индукцией Т-клеточной реакции с последующей стимуляцией В-клеточного ответа и выработкой антител против клеток гранулезы и теки, яйцеклетки, отдельных структур стероидпродуцирующих клеток яичников (цитоплазмы, мембраны), против рецепторов гонадотропинов и непосредственно к гонадотропинам. В случае образования аутоантител против примордиальных фолликулов фолликулярный аппарат яичников повреждается вплоть до его полного уничтожения и замещения соединительной тканью.
При образовании аутоантител к рецепторам гонадотропинов развивается синдром резистентных яичников.
К ятрогенным причинам гипергонадотропной овариальной недостаточности относятся лучевое воздействие, влияние цитостатиков (применяемых при онкологических заболеваниях различной локализации), овариоэктомия или резекция яичников по поводу эндометриоза и опухолевых заболеваний.
Причиной гипогонадотропной овариальной недостаточности могут явиться:
- патология гипофиза (опухоли, аутоиммунный гипофизит, гемохроматоз, гранулематозные процессы при саркоидозе, повреждение гипофиза при черепно-мозговой травме, геморрагический инфаркт либо ишемический некроз гипофиза, последствия хирургического и лучевого лечения аденом гипофиза);
- органическая патология гипоталамуса (опухоли гипоталамуса и метастазы опухолей, энцефалиты, менингиты, гранулематозные и аутоиммунные процессы, черепно-мозговые травмы, сосудистые аномалии);
- функциональные нарушения секреции ГРГ.
При патологии гипофиза неэффективная регуляция функции яичников и развитие симптомов гипогонадизма обусловлены недостаточной секрецией гонадотропинов, а при гипоталамической недостаточности — нарушением частоты и амплитуды импульсной секреции ГРГ.
Функциональные нарушения секреции ГРГ чаще всего обусловлены стрессовыми психогенными воздействиями, чрезмерными физическими нагрузками (профессиональный спорт) и снижением веса ниже «критического» уровня (например, при нервной анорексии).
К наиболее распространенным экстрагонадным причинам относятся ожирение, первичный гипотиреоз, гиперпролактинемия (функциональная и органическая). Наиболее значимыми овариальными факторами являются эстрогенпродуцирующие и андрогенпродуцирующие опухоли, синдром поликистозных яичников, генитальный эндометриоз.
Симптомы и признаки овариальной недостаточности
Клиническая картина определяется недостатком секреции эстрогенов и/или прогестерона.
Клинические проявления гипоэстрогении и гипопрогестеронемии
| Вегетативные нарушения: | Вегетативные нарушения:
|
| Кожа:
| Кожа и придатки: |
| Подкожная жировая клетчатка: | Подкожная жировая клетчатка: |
| Сердечно-сосудистая система: | Мышечная система: |
| Мочеполовая система:
| Мочеполовая система:
|
| Эндокринная система:
| Эндокринная система:
|
| Нервная система:
| Нервная система:
|
Общими важнейшими проявлениями любой формы женского гипогонадизма являются гипоэстрогенемия, гипоплазия матки и яичников и бесплодие.
Другие клинические симптомы связаны с возрастом, в котором развилась овариальная недостаточность, и с особенностями конкретного заболевания. При врожденном дефиците фолликулов специфические признаки развиваются со времени пубертатного периода и проявляются отсутствием или недостаточностью полового развития, недоразвитой маткой, первичной аменореей, высоким ростом и удлиненными конечностями.
После полового созревания клинические симптомы развившейся овариальной недостаточности появляются при снижении общего числа фолликулов до критически низкого уровня. Отсутствие полноценной циклической деятельности яичников сопровождается атрофическими процессами в эндометрии, вагинальном эпителии, молочных железах и постепенной регрессией вторичных половых признаков. Прекращение менструаций у взрослых лиц — вторичная аменорея — нередко сопровождается приливами в виде внезапно появления чувства жара, покраснения кожи лица, шеи и последующего обильного потоотделения.
Некоторые хромосомные болезни, обусловленные числовыми и структурными хромосомными аномалиями, имеют характерные особенности. Так, клинические проявления синдрома Шерешевского-Тернера, помимо полового инфантилизма и аменореи, включают низкий вес при рождении, отставание в росте с раннего детства, наличие стигм дисэмбриогенеза (широко расставленные соски, короткая шея, низкий рост волос, крыловидные кожные складки, неправильная форма ушных раковин, птоз верхнего века, «готическое» небо, деформация зубов, вальгусная деформация коленных и локтевых суставов), а также врожденных пороков, наличие на месте гонад их рудиментов или половых тяжей.
При синдроме тестикулярной феминизации у лиц с типичным женским фенотипом, нормальным ростом, молочными железами выявляются слабо выраженное оволосение, первичная аменорея и слепо заканчивающееся влагалище.
При аутоиммунном поражении фолликулярного аппарата у женщин с анамнезом аутоиммунных либо частых инфекционных заболеваний и ранее нормальной менструальной и репродуктивной функцией в возрасте 35—40 лет развивается аменорея и появляются симптомы, характерные для менопаузы: психо-эмоциональная лабильность, вазомоторные реакции, сердцебиения, метаболические нарушения (остеопороз, увеличение атерогенных фракций липидов в крови).
При аутоиммунном поражении рецепторов к гонадотропинам клинические симптомы появляются через несколько лет после менархе на фоне предшествующей опсоолигоменореи у женщин с правильным телосложением, сохраненным фолликулярным аппаратом яичников.
Для врожденного нарушения секреции ГРГ вследствие сочетанной аплазии или гипоплазии передней комиссуры и обонятельных луковиц (генито-ольфакторный синдром, синдром Каллмана) помимо гипогонадотропного гипогонадизма имеется аносмия или гипосмия, а в ряде случаев — неврологические нарушения, глухота, цветовая слепота.
В случае наследственно обусловленных дегенеративных изменений ядер гипоталамуса выявляются ожирение, умственная отсталость, пигментный ретинит, полидактилия и половой инфантилизм.
У больных с приобретенным дефицитом ГРГ вследствие опухолей, воспалительных и гранулематозных процессов, травматического повреждения гипоталамуса овариальная недостаточность является частым, но второстепенным проявлением по отношению к симптомам основного заболевания. К признакам, которые указывают на вовлечение в патологический процесс гипоталамуса, относятся нарушения сна и бодрствования, пищевого поведения, терморегуляции, развитие несахарного диабета, выпадение полей зрения.
При гипофизарном нанизме, связанном с развитием патологического процесса в гипофизе в детском возрасте, выявляется резкое отставание в росте и физическом развитии с раннего детства, пропорциональное телосложение, задержка сроков окостенения скелета.
Гипогонадотропный гипогонадизм у взрослых часто сочетается с тиреотропной и адренокортикотропной недостаточностью, для которых характерны соответствующие клинические симптомы.
Диагностика и дифференциальная диагностика овариальной недостаточности
Диагностические мероприятия проводятся в определенной последовательности и имеют целью установить факт наличия гормональной недостаточности яичников, определить ее тип и форму, а также выявить конкретную причину развития.
Факт наличия гипогонадизма устанавливается на основании жалоб на нарушение менструального цикла, бесплодие. Он должен быть подтвержден данными гормонального исследования (ЛГ, ФСГ, эстрадиол, пролактин).
Тип овариальной недостаточности (недостаточность лютеиновой фазы, ановуляция) определяют на основании оценки характера менструального цикла, полноценности лютеиновой фазы, наличия овуляции.
Форму овариальной недостаточности устанавливают с помощью исследования уровня гонадотропинов в крови.
С помощью дополнительных методов исследования (гормональных, иммунологических, генетических, лучевых, лапароскопии) выявляют конкретное заболевание, ставшее причиной овариальной недостаточности.
О патологии гипоталамуса и гипофиза, лежащих в основе гипогонадотропной недостаточности яичников, свидетельствуют данные МРТ, позволяющие выявить новообразования, аплазию либо гипоплазию гипофиза. При пангипопитуитаризме определяется не только снижение уровней ФСГ и ЛГ, но и ТТГ, АКТГ и пролактина. Повышение пролактина характерно для гиперпролактинемического гипогонадизма.
Гипергонадотропный гипогонадизм, наличие стигм дисэмбриогенеза являются показанием для проведения цитогенетического исследования (кариотипирования) с целью диагностики хромосомной и генной патологии (синдромов Шерешевского—Тернера и Каллмана, синдрома тестикулярной феминизации, дисгенезии гонад и др.).
Диагностике аутоиммунного оофорита способствуют выявление высокого уровня антиовариальных антител и антител к микросомальной фракции гранулезы яичников, а также гистологическое исследование ткани яичников.
Высокий уровень тестостерона в сочетании с быстро прогрессирующей вирилизацией указывает на наличие андрогенпродуцирующей опухоли яичников. Визуализацию опухолей надпочечников осуществляют с помощью КТ, яичников — с использованием УЗИ, МРТ, лапароскопии.
Диагностика гипотиреоза осуществляется на основании определения в крови уровня ТТГ.
В ходе проведения дифференциальной диагностики при аменорее необходимо исключить врожденную аплазию матки и влагалища и патологию выводящих путей: облитерацию канала шейки матки, облитерацию влагалищного отверстия, внутриматочные синехии.
Лечение овариальной недостаточности
Комплекс проводимых лечебных мероприятий определяется характером основного патологического процесса, формой овариальной недостаточности и возрастом, в котором развилось заболевание.
Для лечения гипогонадотропной овариальной недостаточности, обусловленной опухолями гипоталамо-гипофизарной области, используют хирургический или лучевой методы. При доказанном гипопитуитаризме назначают пожизненную гормональную заместительную терапию глюкокортикоидами, тироксином, эстрогенами и гестагенами. Для стимуляции овуляции используют менопаузальный гонадотропин, содержащий ФСГ и Л Г (менотропины) в соотношении 1:1.
Первично-гипоталамическая овариальная недостаточность требует стимуляции развития вторичных половых признаков путем назначения эстрогенов. При необходимости индукции овуляции назначают менотропины или импульсное введение ГРГ. Лечение гиперпролактинемического гипогонадизма изложено в соответствующем разделе.
При дисгенезии гонад первоначально проводится стимуляция развития вторичных половых признаков (терапия эстрогенами). Если в кариотипе определяется Y-хромосома или ее участок, то стимуляция проводится после гонадэктомии. В дальнейшем проводится длительная циклическая заместительная терапия эстрогенами и гестагенами. При типичной форме дисгенезии гонад лечение включает также назначение препаратов соматотропина для коррекции низкорослости.
При синдроме тестикулярной феминизации проводят гонадэктомию после полового созревания, а затем назначают эстрогены.
При гипергонадотропной форме аутоиммунного оофорита применяют заместительную гормонотерапию эстрогенами и гестагенами.
www.sweli.ru