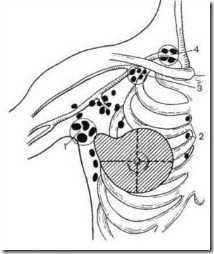
Диагностика заболеваний молочной железы
Современные методы диагностики заболеваний молочных желез в практике акушера-гинеколога
Актуальность проблемы заболеваний молочных желез обусловлена прежде всего неуклонным ростом этой патологии во всем мире [5, 7]. Так, в популяции нераковые заболевания молочных желез встречаются у 30–70% женщин, а при одновременно имеющих место гинекологических заболеваниях их частота возрастает до 76–97,8% [7]. В России ежегодно выявляется более 34 000 новых случаев рака молочных желез, при этом отмечается значительное снижение возраста заболевших. У 25% женщин до 30 лет и у 60% после 40 лет диагностируются дисгормональные заболевания молочных желез (мастопатии) [3]. Несмотря на то, что мастопатии не являются облигатным предраком, рак молочной железы встречается в 3–5 раз чаще на фоне диффузных дисгормональных доброкачественных заболеваний молочных желез и в 30–40 раз чаще при узловых формах мастопатии с явлениями пролиферации эпителия молочных желез [3]. В связи с этим значительно возрос интерес к доброкачественным заболеваниям, а снижение заболеваемости мастопатией — реальный путь к снижению частоты рака молочной железы. В целом рак молочной железы не является предметом изучения и лечения врачей акушеров-гинекологов, но к ним часто обращаются женщины с проблемами, напрямую не связанными с содержанием специальности, в том числе и с проблемами, касающимися молочных желез. Поэтому акушеры-гинекологи могут существенно улучшить работу по сохранению здоровья женщины при экстрагенитальной патологии и при некоторых формах онкозаболеваний, в частности, при раке молочной железы. Несомненно, приоритетными для гинекологов являются вопросы диагностики и лечения доброкачественных заболеваний молочных желез. Поскольку молочные железы являются неотъемлемой частью репродуктивной системы женщины, решение проблемы ее оздоровления невозможно без наблюдения и исследования молочных желез, что несомненно должно входить в круг обязанностей акушеров-гинекологов. Выявление диффузной и очаговой патологии молочных желез и правильная трактовка полученных результатов обследования позволяют своевременно направить женщин на комплексное обследование и сориентироваться в правильном выборе метода лечения.
Традиционно в России и ряде других стран заболеваниями молочных желез занимаются в основном хирурги, онкологи и маммологи. В связи с этим акушеры-гинекологи не могли уделять должного внимания обследованию и лечению молочных желез в режиме скрининга (как это, например, проводится при заболеваниях шейки матки) [5, 7]. А без их участия врачами вышеназванных специальностей зачастую недооценивается весь спектр функциональных и органических нарушений репродуктивной системы в целом [6, 7]. Кроме того, следует отметить, что низкая выявляемость заболеваний молочных желез на ранних стадиях зачастую обусловлена недостатком знаний в области клинической маммологии у врачей акушеров-гинекологов, так как именно данная категория врачей является наиболее часто посещаемой среди женщин. При профилактическом осмотре акушером-гинекологом состояние молочных желез в схему осмотра и сбора анамнеза пациентки часто не включается. Вышеперечисленное свидетельствует о том, что ранняя диагностика патологии молочной железы представляется затруднительной. Важной задачей является организация взаимодействий врачей гинекологов и онкологов-маммологов. Участие врачей первичного звена в направлении женского населения на маммологический скрининг является важным инструментом снижения смертности от рака молочной железы.
Цель нашей статьи — дать краткую обзорную информацию о современных методах диагностики заболеваний молочных желез и возможных диагностических критериях рака молочной железы.
Осмотр и пальпация — основные и доступные методы выполняются врачом в вертикальном положении женщины (с опущенными, а затем поднятыми вверх руками) и горизонтальном положении. При осмотре молочной железы учитываются аномалии (добавочные молочные железы), изменение формы и объема, изменение цвета кожных покровов (наличие и степень выраженности венозного рисунка, кожные симптомы). Пальпаторно обследуют всю железу последовательно по квадрантам и область субмаммарной складки. При пальпации молочных желез определяются участки болезненных уплотнений без четких границ в виде тяжей, а также грубые железистые дольки в виде «булыжной мостовой». Довольно часто встречается локальная болезненность. Указанные изменения наиболее выражены в верхненаружных квадрантах, которые в функциональном отношении являются наиболее активными.
Доступность молочных желез для обследования и кажущаяся простота диагностики часто приводят к неправильной интерпретации результатов клинического исследования, которое зачастую проводится малоподготовленными в этом вопросе специалистами. Все это ведет как к гипо-, так и к гипердиагностике.
Поэтому мануальное обследование должно дополняться комплексным рентгенологическим, ультразвуковым (УЗИ), радиотермометрией (РТМ-диагностика), электроимпедансной маммографией (ЭИМ), другими видами инструментальных исследований.
Основным на сегодняшний день методом объективной оценки состояния молочных желез является рентгенологическая маммография. Эта методика рентгенологического исследования позволяет своевременно распознать патологические изменения в молочных железах в 95–97% случаев [8]. Именно это качество в отличие от других методов диагностики позволяет рассматривать маммографию как ведущий метод скрининга. В настоящее время во всем мире общепринято (ВОЗ, 1984) начиная с 40 лет проводить маммографическое исследование 1 раз в 2 года (при отсутствии показаний для более частого обследования), после 50 лет — 1 раз в год. Исключением являются женщины до 35 лет, кормящие, беременные женщины и подростки, которым маммография противопоказана.
Маммография — это рентгенография молочной железы без применения контрастных веществ. Метод простой, безопасный для обследуемых, отличается высокой диагностической эффективностью.
Маммографию проводят в двух проекциях (прямой — краниокаудальной и боковой) на 5–10 день менструального цикла, когда паренхима молочной железы менее отечна и болезненна, а при отсутствии менструаций — в любой день. Также можно использовать дополнительную боковую проекцию с медиолатеральным ходом луча (косая проекция). На боковых снимках при правильной укладке должны визуализироваться частично грудная мышца, ретромаммарная клетчатка, переходная складка. В прямой проекции — сосок, выведенный на контур железы, все структурные элементы молочной железы, в 20–30% — грудная мышца.
При необходимости уточнения состояния определенного участка молочной железы необходимо проводить прицельную рентгенографию с помощью специальных тубусов различной площади. Это лучше отграничивает патологический участок, а использование дозированной компрессии повышает четкость изображения. С помощью прицельных рентгенограмм удается вывести опухоль в край железы. При этом она выявляется более отчетливо, лучше определяется лимфатическая дорожка и состояние кожи в прилегающих участках. Прицельные снимки позволяют избежать ошибок, обусловленных проекционными эффектами суммации теней. В ряде случаев целесообразно использовать прицельную рентгенографию с прямым увеличением рентгеновского изображения.
Рентгеновская картина молочной железы у каждой женщины индивидуальна. Важно ориентироваться врачам первичного звена в признаках злокачественности при описании маммограмм. При маммографии различают первичные и вторичные признаки злокачественности.
Первичными и основными рентгенологическими признакам рака молочной железы является наличие опухолевой тени и микрокальцинатов. Наиболее четко тень опухоли дифференцируется у женщин старшей возрастной группы на фоне инволютивно измененной ткани молочной железы. Тень опухоли, как правило, неправильной — звездчатой или амебовидной формы, с неровными, нечеткими контурами, характерной радиарной тяжистостью. Очень часто опухолевый узел сопровождается «дорожкой» к соску и втяжением последнего, утолщением кожи железы, иногда с ее втяжением. Одним из наиболее достоверных и ранних признаков рака является наличие микрокальцинатов, являющихся отображением отложения солей в стенках протоков. Иногда микрокальцинаты являются единственным рентгенологическим проявлением раннего рака молочной железы. Обычно микрокальцинаты имеют мелкоклеточный характер (размерами 1 мм и менее), напоминая песчинки. Чем их больше и чем они мельче, тем больше вероятность рака. Кальцинаты могут встречаться и при мастопатии и даже в норме, однако их характер значительно отличается от вышеописанного: их немного, они значительно крупнее (более 3–5 мм), более бесформенные и глыбчатые.
К вторичным (косвенным) рентгенологическим признакам рака молочной железы относят симптомы со стороны кожи, соска, окружающей ткани молочной железы, усиленная васкуляризация и т. д.
Несмотря на эффективность рентгенологического метода, у ряда больных разрешающая способность маммографии резко снижается: при выраженных диффузных формах мастопатии, у молодых пациенток с плотными молочными железами, при наличии имплантатов, выраженных воспалительных изменениях, отеке железы и фоновых заболеваниях типа фиброаденоматоза. В этом случае на помощь приходит УЗИ молочных желез.
Основные преимущества маммографии, используемые при диагностике заболеваний молочной железы: возможность получения позиционного изображения молочной железы, высокая информативность при обследовании, возможность визуализации непальпируемых образований, возможность сравнительного анализа снимков в динамике. Недостатки метода, ограничивающие применение: дозовая нагрузка, хотя она и ничтожно мала; в 1,8–6% случаев по данным литературы имеет место рентгенонегативный рак. По данным большинства авторов процент достоверности маммографического исследования в диагностике рака составляет от 75% до 95%. Достоинства новой технологии не ограничиваются только клиническими аспектами. Появление цифровых приемников изображения позволило методу маммографии развиваться в контексте фундаментальных изменений, происходящих во всех разделах медицинской визуализации и в самой системе организации медицинской службы.
По общепринятому мнению, УЗИ является основным методом диагностики заболеваний молочных желез у женщин до 35–40 лет, при беременности, лактации, а в более позднем возрасте предпочтение следует отдавать рентгенологической маммографии. Ультразвуковая диагностика постоянно наращивает свой потенциал благодаря совершенствованию уже имеющихся и разработке новых методик диагностики. Сканирование выполняется на ультразвуковых аппаратах линейным датчиком с частотой 7,5–10 МГц при коэффициенте увеличения изображения 1,5, с использованием иммерсии — наличия слоя геля на соприкасающихся поверхностях кожи и датчика — для уменьшения содержания между ними воздуха.
Преимуществами ультразвуковых исследований молочных желез являются: безопасность в плане дозовой нагрузки, что позволяет обследовать беременных и кормящих; высокая разрешающая способность, что важно при плотном фоне молочной железы у молодых женщин (возможность визуализации рентгенонегативных опухолей, образований, расположенных вблизи грудной стенки); дифференциальная диагностика солидного и полостного образования (практически 100% диагностика кист любого размера); оценка состояния силиконовых имплантантов молочных желез, особенно при их разрывах и утечке содержимого; обследование молочных желез в острый период травмы или воспаления; визуализация регионарных лимфатических узлов; проведение прицельных пункционных биопсий под объективным визуальным контролем пальпируемых и непальпируемых образований в молочной железе; многократное динамическое исследование в процессе лечения.
Несмотря на все достоинства УЗИ молочных желез, практические врачи в большинстве случаев при назначении лечения пациенткам любых возрастных групп ориентируются в основном на данные рентгеновской маммографии. Недоверие к УЗИ молочных желез связано с тем, что молочная железа является одним из наиболее трудных объектов для ультразвуковой диагностики, так как соотношение составляющих ее тканей постоянно меняется в зависимости от возраста, фазы менструального цикла, физиологических периодов жизни, массы тела, наличия патологических процессов. Поэтому специалист, проводящий УЗИ, должен уметь не только правильно идентифицировать различные тканевые компоненты, составляющие молочную железу, но и иметь достаточный опыт, чтобы составить себе представление, какой должна быть в норме структура молочной железы у каждой обследуемой пациентки с учетом отмеченных выше факторов. В настоящее время еще не существует единого подхода к идентификации различных тканей, образующих молочную железу, поэтому одна и та же эхографическая картина разными специалистами часто оценивается по-разному [4]. Кроме того, если врач не имеет четкого представления обо всем диапазоне структурных особенностей молочной железы, выявляемых при УЗИ в норме, то он может некоторые отклонения в пределах спектра нормального развития расценить как патологические. По-видимому, этим можно объяснить удивительно высокую частоту такого диагноза, как фиброзно-кистозная болезнь (ФКБ). Большинство публикаций посвящено ультразвуковой диагностике различных новообразований молочной железы как доброкачественного, так и злокачественного характера. И здесь не возникает принципиальных разночтений эхограмм, поскольку разработана четкая эхосемиотика узловых образований молочной железы [4]. Другое дело ультразвуковая диагностика такого заболевания, как ФКБ, суть которого состоит в дисплазии молочной железы доброкачественного характера с различной степенью выраженности пролиферативных и регрессивных изменений ее тканевых элементов. Учитывая очевидную гипердиагностику ФКБ по данным УЗИ, вновь встает вопрос о необходимости разработки корректной эхографической идентификации тканевых компонентов молочной железы в норме [4]. Отдельным пунктом стоит масталгия, диагностика которой существующими методами визуализации молочных желез представляется абсурдной. А своевременная дифференциальная диагностика масталгии разной этиологии предполагает правильный выбор дальнейшей тактики ведения женщин. Разночтения в интерпретации одной и той же эхографической структуры молочной железы разными авторами диктуют необходимость совершенствовать старые методы и проводить разработку новых методов исследования молочных желез.
К эхографическим критериям рака молочной железы относят: неправильную форму, нечеткие контуры, гипоэхогенную неоднородную структуру, гиперэхогенные включения разной величины, акустические тени, преобладание переднезаднего размера образования.
Новой технологией измерения температуры тканей молочной железы и ее цифрового изображения является метод микроволновой радиотермометрии (РТМ-исследование) с использованием компьютеризированного диагностического комплекса (РТМ-01-РЭС), предназначенного для измерении интенсивности собственного электромагнитного излучения внутренних тканей пациента в диапазоне сверхвысоких частот, которое пропорционально температуре тканей (рис. 1).
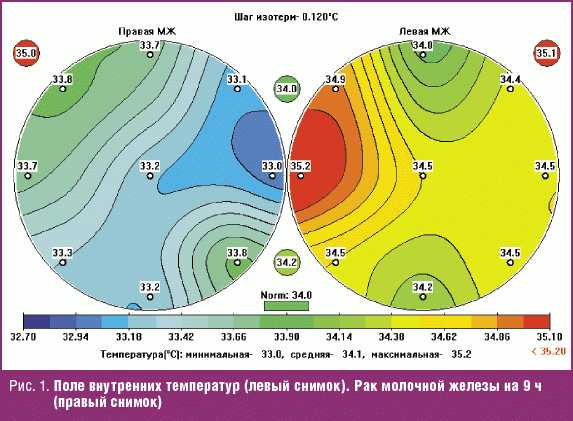
Изменение температуры (температурная аномалия) может быть, в частности, вызвано усиленным метаболизмом раковых клеток, на чем и основана ранняя диагностика рака. Согласно существующим представлениям, изменение температуры тканей обычно предшествует структурным изменениям, которые обнаруживаются при общепринятых методах исследования молочной железы — УЗИ, маммографии, пальпации. Поэтому термометрия представляет интерес для ранней диагностики заболеваний. Кроме того, метод термометрии по своему принципу действия абсолютно безопасен и безвреден для пациентов и обслуживающего персонала, так как при исследовании производится измерение интенсивности собственного электромагнитного излучения тканей человека. Поэтому использование радиотермометрии чрезвычайно эффективно для объективного контроля за ходом лечения и для проведения скрининговых исследований. Удельное тепловыделение в опухоли прямо пропорционально скорости ее роста, т. е. быстро растущие опухоли более «горячие» и поэтому лучше видны на термограммах. Таким образом, радиотермометрия обладает уникальной способностью обнаруживать в первую очередь быстро растущие опухоли. Введение в комплексную диагностику радиотермометрических обследований приведет к естественной диагностической селекции больных раком молочной железы с бурным ростом опухоли. Методика РТМ-обследования заключается в измерении внутренней температуры и температуры кожи молочных желез в 10 точках на каждой железе, включая аксиллярную область, область ареолы, середины квадрантов и границы квадрантов. Результаты измерений отображаются на экране компьютера в виде термограмм и полей температур. Кроме этого, в состав программы входит экспертная система диагностики рака молочной железы.
 В настоящее время в дополнение к существующим методам диагностики появилась возможность визуализации тканей молочной железы с помощью электроимпедансной томографии (рис. 2), метода получения изображения распределения импеданса в тканях. Для визуализации тканей молочной железы используется многочастотный 256-электродный электроимпедансный маммограф (МЭМ), разработанный Институтом радиотехники и электроники РАН, на частотах 10 кГц и 50 кГц.
В настоящее время в дополнение к существующим методам диагностики появилась возможность визуализации тканей молочной железы с помощью электроимпедансной томографии (рис. 2), метода получения изображения распределения импеданса в тканях. Для визуализации тканей молочной железы используется многочастотный 256-электродный электроимпедансный маммограф (МЭМ), разработанный Институтом радиотехники и электроники РАН, на частотах 10 кГц и 50 кГц.
С целью реализации метода электроимпедансной маммографии разработана измерительная система и алгоритм реконструирования изображений, которые позволяют, используя набор электродов, располагающихся в виде двумерной матрицы на плоской поверхности, визуализировать статические распределения электропроводности среды, прилегающей к поверхности с электродами. Результатом визуализации является набор изображений поперечных сечений среды плоскостями, параллельными плоскости электродов и располагающимися на разной глубине от поверхности среды [1, 2, 9–12].
Во время обследования матрица прижимается к молочной железе в направлении ребер, так что максимальное количество электродов оказывается в контакте с телом пациента, а толщина обследуемых тканей минимальна. Два отводящих электрода, один из которых используется как общий электрод источника тока, а второй — как опорный электрод измерителя разности потенциалов, состыкованы между собой и располагаются на запястье пациентки (рис. 3).
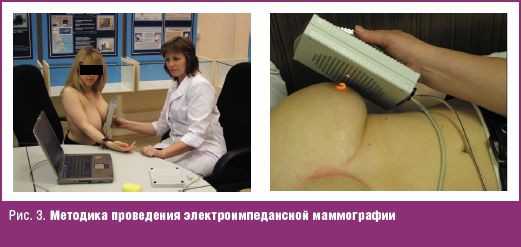
Последовательность работы измерительной системы следующая. Измеритель разности потенциалов подключается мультиплексором к первому электроду матрицы, выполняется процедура компенсации контактной разности потенциалов, а затем источник тока последовательно подключается к каждому из оставшихся электродов матрицы и производятся измерения. После этого цикл повторяется для другого регистрирующего электрода. Полный набор данных, используемых для реконструирования трехмерных распределений электропроводности, состоит из 65 280 результатов измерений. Обработка данных и инициирование процесса измерения осуществляется с помощью персонального компьютера, соединенного с прибором по универсальной последовательной шине (USB).
Результатом реконструирования являются электроимпедансные изображения семи поперечных сечений исследуемой среды, параллельных плоскости с электродами, взятых с шагом 0,7 см по глубине (рис. 4).
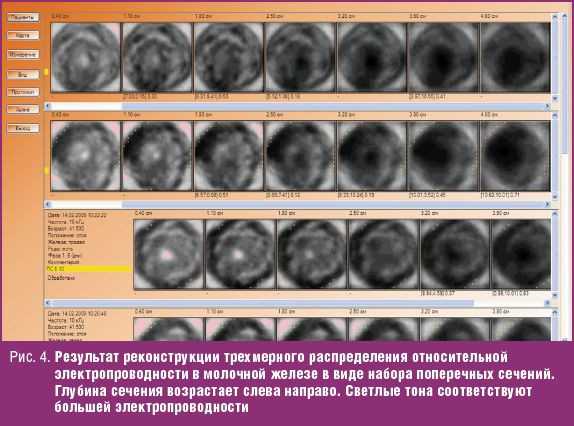
Длительность процедуры реконструкции составляет около 15–20 секунд для персонального компьютера с тактовой частотой порядка 1 ГГц.
В распоряжении врачей, занимающихся диагностикой заболеваний молочных желез, появился новый, доступный, безопасный и высокоинформативный метод электроимпедансной маммографии, существенно дополнивший существующий арсенал современных методов обследования, который можно использовать как метод скрининга у женщин всех возрастных периодов, так и в качестве надежного контроля состояния молочной железы при приеме комбинированных оральных контрацептивов и препаратов заместительной гормонотерапии без ограничения числа процедур обследования.
Метод ЭИМ существенно расширяет возможности акушеров-гинекологов и врачей других клинических специальностей в отношении инструментальной диагностики заболеваний молочных желез и дает им уникальные возможности объективной оценки их состояния как составной части неотъемлемого звена единой репродуктивной системы.
Предлагаемая программа многочастотного электроимпедансного обследования позволяет выделить четкие диагностические критерии различной диффузной и очаговой патологии молочных желез, дифференцировать масталгию различной этиологии, что важно для правильного выбора тактики ведения женщин с заболеваниями молочных желез.
Преимуществами электроимпедансной визуализации являются: возможность проведения динамического наблюдения у женщин любого возраста и проведение сравнительной оценки изображений в зависимости от стороны и позиции при исследовании, фазы менструального цикла, предыдущей диагностики; возможность обследования молочных желез во время беременности и лактации; цветное сканирование и режим «фильтрации» изображения, позволяющие дифференцировать доброкачественные и злокачественные образования по различной цветовой гамме; возможность визуальной оценки на разной глубине сканирования и визуализация органа в целом. Метод многочастотной ЭИМ позволяет в цифровом выражении определить показатели электропроводности молочных желез, что в какой-то мере исключает субъективную оценку в постановке диагноза.
Для рака молочной железы характерно:
- На электроимпедансных томограммах в месте вероятного расположения опухоли появляются гипоимпедансные районы с нечеткими размытыми контурами, распространяющиеся на несколько плоскостей сканирования с высокой электропроводностью (чаще всего более 0,95 усл. ед.).
- При использовании дополнительного контрастирования участки с высокой электропроводностью окрашиваются красным цветом.
- При визуализации в режиме цветной шкалы зоны расположения рака выделяются белым цветом с ярким красным контуром.
- Разница в изображениях в зависимости от стороны сканирования из-за нарушения архитектоники внутренних структур пораженной молочной железы при неизмененной здоровой молочной железе.
- Разница в показателях электропроводности в пораженной молочной железе в зависимости от позиции при исследовании.
- Наличие деформаций контуров изображения пораженной молочной железы и четкие недеформированные контуры здоровой молочной.
- Смещение внутренних структур.
- Резкое смещение графика частотного распределения электропроводности вправо по сравнению с непораженной молочной железой и с графиком распределения электропроводности пораженной молочной железы
Несмотря на огромный арсенал методов диагностики рака молочной железы в практике акушера-гинеколога, необходимо помнить, что только комплексное обследование пациенток и цитологическая или гистологическая верификация диагноза, осуществляемые в специализированных лечебных учреждениях, позволяет квалифицированно оказать необходимый перечень медицинских мероприятий. Если есть хоть минимальные подозрения на возможность малигнизации, пациентку необходимо отправить в онкологическое учреждение. В такой ситуации гипердиагностика и ложная тревога может в худшем случае стать тактической ошибкой, однако это может позволить избежать стратегической ошибки, что значительно важнее.
Литература
- Корженевский. А. В. Квазистатическая электромагнитная томография для биомедицины: Дис. … д-ра. физ.-мат. наук. М., 2009. 326 с.
- Корженевский А. В., Карпов А. Ю., Корниенко В. Н. и др. Электроимпедансная томографическая система для трехмерной визуализации тканей молочной железы // Биомедицинские технологии и радиоэлектроника. 2003. № 8. С. 5–10.
- Летягин В. П. Мастопатия // Гинекология. 2000. № 11. С. 468–472.
- Озерова О. Е. Нормальные эхографические особенности структуры молочных желез в различные возрастные периоды, при беременности и лактации // Sonoace international. 2001. Вып. 9. С. 50–57.
- Радзинский В. Е., Зубкин В. И., Золичев Г. Е. и др. Сборник научных трудов «Онкологический скрининг, канцерогенез и ранние стадии рака в практике гинеколога». Ижевск, 2000. С. 201–203.
- Радзинский В. Е., Ордиянц И. М. Комплексный подход к диагностике и лечению гинекологических и маммологических заболеваний и нарушений // Гинекология. 2003. Т. 5. № 4. С. 1–6.
- Радзинский В. Е., Ордиянц И. М., Зубкин В. И. и др. Нераковые заболевания молочных желез и гинекологические заболевания // Журнал Российского общества акушеров-гинекологов. 2006. № 2. С. 34–42.
- Серов В. Н., Тагиева Т. Т., Прилепская В. Н. Диагностика заболеваний молочных желез // Гинекология. 1999. № 1. С. 6–10.
- Cherepenin V., Korjenevsky A., Kornienko V. et al. The electrical impedance tomograph: new capabilities // Proceedings of the IX international conference on electrical bio-impedance. Heidelberg. 1995. P. 430–433.
- Cherepenin V., Karpov A., Korjenevsky A. et al. Three-dimensional EIT imaging of breast tissues: system design and clinical testing // IEEE Trans. Medical Imaging. 2002. V. 21 (6). P. 662–667.
- Cherepenin V., Karpov A., Korjenevsky A. et al. Preliminary static EIT images of the thorax in health and disease // Physiological Measurement. 2002. V. 23 (1). P. 33–41.
- Cherepenin V., Karpov A., Korjenevsky A. et al. A 3D electrical impedance tomography (EIT) system for breast cancer detection // Physiological Measurement. 2001. V. 22 (1). P. 9–18.
Ч. Н. Мустафин*, кандидат медицинских наук, доцент О. В. Троханова**, доктор медицинских наук, доцент
*ГБОУ ДПО РМАПО МЗ РФ, Москва **ГБОУ ВПО ЯГМА МЗ РФ, Ярославль
Контактная информация об авторах для переписки: chingis.x@gmail.com
www.lvrach.ru
Диагностика заболеваний молочных желёз
Женщины обязательно должны владеть приёмами самообследования молочных желёз. Рекомендуется регулярно проводить самообследование после «критических» дней, когда проходит напряжение груди. Дело в том, что накануне менструации, при нагрубании молочных желёз, можно обнаружить уплотнения, которые затем самостоятельно исчезнут после менструации. Нередко при пальпации груди у женщины накануне критических дней и врач находит уплотнения, которые потом самостоятельно исчезают.
Нагрубание молочных желёз происходит за счёт физиологической задержки жидкости в организме женщины во второй (прогестиновой) фазе менструального цикла, что самостоятельно проходит после месячных. Ограничение натрия (поваренная соль, натрия глютамат – усилитель вкуса) и применение мочегонных травяных сборов за 2 недели до менструации способствует уменьшению количества жидкости и уменьшает чувство напряжения в груди накануне «критических» дней.
Если же обнаруженное Вами уплотнение в молочной железе не исчезло после менструации – обратитесь к онкологу или маммологу.
План Ваших дальнейших обследований составит врач. Совсем не обязательно проходить все имеющиеся в наличии способы обследований. Некоторые из них дублируют друг друга, но есть более и менее информативные, более и менее быстрые. К сожалению, имеющийся у Вас полис ОМС фактически не обеспечивает быструю диагностику на современном оборудовании, а полис ДМС перестаёт работать при постановке диагноза «рак». Сообщите своему врачу о Ваших возможностях и желании пройти обследование на современном уровне, и он составит Ваш план обследований, как сделал бы это для своего родственника и сэкономит Ваше время.
Безусловно, более информативными способами диагностики заболеваний молочных желёз являются современные инструментальные методы. Так, например, даже опытный врач может не заметить небольшую опухоль (до 1 см), а в большой или плотной молочной железе он может не найти и более крупное образование. Существуют непальпируемые опухоли, которые выявляются только инструментальными методами диагностики.
В молодом возрасте не характерно появление злокачественных опухолей. Грудь у нерожавшей женщины достаточно плотная. Это обстоятельство делает маммографию не самым информативным методом диагностики. Поэтому при обнаружении опухоли в молочной железе в молодом возрасте целесообразно выполнить УЗИ - ультразвуковое исследование молочных желёз, опять же, после месячных. Данное исследование позволяет отличить кисту молочной железы от фиброаденомы, выявить кистозно-расширенные протоки, оценить состояние лимфатических узлов.
Для раннего выявления рака молочной железы стандартным исследованием является не осмотр врача и не УЗИ, а маммография. Впервые её необходимо выполнить с 35 лет. Это будет базисный снимок, когда маловероятно, что будет обнаружена злокачественная опухоль. Однако с этим снимком рентгенолог сможет сравнивать последующие Ваши маммограммы. Тогда, даже появление начальных признаков злокачественной опухоли не ускользнёт от его внимания.
Разновидностью маммографии является дуктография. Она применяется для диагностики папиллом протоков молочной железы (или цистаденопапилломы - ЦАП, проявляющейся выделениями из соска молочной железы, чаще кровянистыми или «ржавыми») и дуктэктазии (патологическое расширение её протоков).
Для диагностики папиллом протоков и дуктазии также может использоваться дуктоскопия.
Более информативным исследованием, чем маммография и УЗИ, является МРТ молочных желёз (магнито-резонансная томография). Она показана при непальпируемых опухолях, при плотной ткани молочных желёз, для диагностики заболеваний протезированной молочной железы (после установки имплантов), при расположении опухоли возле грудины, либо на периферии ткани железы, когда опухоль не попадает в маммографический снимок, либо при несмещаемых опухолях, при сомнительных результатах маммографии, или как самостоятельный метод (для скрининга у носительниц мутации BRCA), а также вместо маммографии для состоятельных пациенток.
Рентгенография лёгких /флюорография (ФЛГ)
Рентгенографию лёгких лучше выполнять в 3-х проекциях. Исследование направлено на получение информации о состоянии лёгких перед операцией и позволяет выявить метастазы, но проигрывает в этом компьютерной томографии (которая позволяет выявить метастазы меньшего размера).
Флюрография допустима только пациенткам с доброкачественными заболеваниями (фиброаденома, киста, цистаденопапиллома молочной железы), а также готовящимся к пластическим операциям на молочной железе, так как рассчитана она только на раннее выявление туберкулёза, а небольшие метастазы на ней просто не видны.
Подробнее, а также где можно сделать рентгенографию, какие исследования информативнее её - смотрите здесь.
Компьютерная томография (КТ)
Данное исследование не совсем оправдана для диагностики непосредственно заболеваний молочных желёз, в связи с наличием более информативных, простых или дешёвых методов диагностики (маммография, УЗИ и МРТ), однако опытный специалист при описании КТ снимков грудной клетки может выявить и довольно подробно описать состояние патологического очага в молочной железе, а также состояние её регионарных лимфатических узлов.
Компьютерная томография информативна для обнаружения и оценки динамики на фоне лечения метастазов в печени, лёгких, внутригрудных, подмышечных или шейных лимфатических узлах, а также в костях, находящихся в зоне сканирования. ПЭТ (позитронно-эмиссионная томография)ПЭТ-КТ (объединённый ПЭТ с компьютерным томографом)
По аналогичным причинам (как и КТ) не могут быть рекомендованы к рутинному использованию просто для диагностики заболеваний молочных желёз. Но ПЭТ (позитронно-эмиссионная томография) – актуальна при подозрении на рак и неинформативности вышеописанных неинвазивных способов диагностики, для выявления метастатического распространения опухоли, дифференциации между различными злокачественными процессами у одного пациента.
Зарубежные клиники Германии, Израиля, Финляндии, Швейцарии и пр. часто позиционируют наличие у них в арсенале ПЭТ-КТ исследования как признак современной диагностики. В Санкт-Петербурге установлено 4 таких аппарата. Два из них реально работают (сегодня выгоднее закупать оборудование, а не обеспечивать его применение). Обследование на нём обходится почти в 2 раза дешевле, чем в европейских центрах. В ряде случаев, когда пациент заинтересован пройти только все самые информативные обследования при подозрении на рак молочной железы и имеет такую возможность (например, МРТ молочных желёз и её регионарных лимфатических узлов, КТ лёгких, КТ или МРТ брюшной полости (печени) с контрастированием и остеосцинтиграфию) - действительно, нередко по информативности, быстроте получения результатов и цене оптимальнее пройти сразу ПЭТ-КТ - исследование, чем выполнять все вышеуказанные обследования вместе взятые.
Сцинтиграфия костей скелета (сканирование костей скелета)
Исследование показано для обнаружения костных метастазов рака молочной железы. Но возможно и ложное накопление радиофармпрепарата (РФП) в местах бывших переломов, неспецифическом воспалении (артрозы, артриты). В случае накопления РФП показана рентгенография или компьютерная томография этих костей для дифференциальной диагностики метастазов от вышеуказанных изменений.
Она показана пациентам в плане предоперационного обследования при размере опухоли больше 1.5 - 2.0 см и/или увеличенных регионарных лимфатических узлах.
Более подробную информацию, а так же где можно сделать остеосцинтиграфию в Санкт-Петербурге смотрите здесь.
Онкомаркеры
СА 15-3 и РЭА – не используются для диагностики рака молочной железы, но информативны для контроля за эффективностью лечения рака молочной железы при III стадии и выше, а также для наблюдения за пролеченными пациентами (смотри в сноске «Анализы и обследования» и здесь).
Дело в том, что только у 1 из 5 пациенток с уже установленным запущенным раком молочной железы (с отдалёнными метастазами) эти показатели повышаются.
При обнаружении любой опухоли в молочной железе показано её исследование под микроскопом. Отдельно необходимо оговорить временные рамки – когда это исследование необходимо осуществить. Биопсия бывает пункционная (тонкоигольная, выполняется шприцем с аспирацией) – позволяет получить содержимое кисты, клетки для цитологического исследования. Диагностическая значимость оценивается в 50 – 70 %. Трепан-биопсия – (выполняется толстой специальной иглой) позволяет получить фрагмент ткани для гистологического исследования. Её информативность может достигать 95%. Эксцизионная биопсия - выполняется при операции: после иссечения опухоли, её отправляют на гистологическое исследование. Термография и компьютерная диагностика (не путать с компьютерной томографией), равно как иридодиагностика, аурикулодиагностика, гадание и шаманство - не являются специфичными и достоверными средствами диагностики заболеваний молочной железы.
Далее пациентам даны рекомендации как рациональнее пройти необходимые обследования.
Перед первичным посещением врача-маммолога (или онколога) сначала выполните маммографию (женщины после 35 – 40 лет с опухолью молочной железы) и/или (до 35 лет) УЗИ молочных желёз и регионарных лимфатических узлов. Лучше эти обследования выполнять на 5-9 дни менструального цикла.
С этими обследованиями идите на консультацию к врачу, у которого планируете проходить лечение.
По результатам консультации Вам могут быть назначены дополнительные обследования – тогда будет необходимо явиться повторно с результатами этих обследований.
Для госпитализации на оперативное лечение пациенты собирают необходимые документы, проходят ряд обследований и сдают анализы, согласно вышеуказанному перечню.
www.abcsurgery.ru
Диагностика заболеваний молочных желез
Рак молочной железы: описание. Тенденции. Статистика. Вопросы диагностики.
В. А. Синицын, Т. В. Руднева Научный центр акушерства, гинекологии и перинатологии РАМН (дир. акад. РАМН проф. В. И. Кулаков) Москва
К патологии молочных желез относятся пороки и аномалии развития, воспалительные заболевания, дисгормональные дисплазии, доброкачественные и злокачественные опухоли, туберкулез, актиномикоз и др.
Рак молочной железы занимает первое место в структуре онкологической заболеваемости среди женщин. Ранняя диагностика — один из реальных путей улучшения результатов лечения. Эффективность лечения прямо зависит от распространенности опухолевого процесса.
Следует остановиться на так называемых факторах риска, знание которых может помочь в прогнозировании возникновения рака молочной железы и формирования групп риска. Фактор риска — понятие больше эпидемиологическое, чем этиологическое. Факторы риска не предопределяют развитие заболевания, а увеличивают вероятность его возникновения.
Доказано, что в семьях больных раком молочной железы среди их кровных родственников данное заболевание встречается чаще в 4,5-7 раз.
Определенное значение имеет время наступления менархе: неблагоприятным фактором является возраст младше 12 и старше 15 лет. Риск развития рака молочной железы связан с возрастом женщины при наступлении естественной менопаузы: наступление ее в возрасте 55 лет и старше ведет к увеличению риска в 2-3 раза.
При оценке генеративной функции обращают внимание на число родов или их отсутствие: риск возрастает у нерожавших, одинаков у рожавших 1-4 раза и значительно снижается при рождении 5 детей и более. Негативным фактором является отсутствие лактации. Отрицательно влияют очень высокие и очень низкие показатели роста и массы тела.
К факторам риска относятся также ионизирующее излучение, работа на химических предприятиях, проживание в экологически неблагоприятных регионах, чем, видимо, можно объяснить более высокую (в 1,5-2 раза) заболеваемость у жительниц крупных промышленных городов. Прямое влияние пищевых факторов спорно. Как фактор риска рассматривается возраст. Чем старше женщина, тем выше вероятность заболевания.
Большое значение придается наличию доброкачественных заболеваний молочных желез. Это заключение основано на концепции: «всякий риск имеет свой предрак». Действительно, многие клиникоэпидемиологические исследования показывают, что возникновению опухолей, как правило, предшествуют предопухолевые состояния. Изучение эпидемиологии доброкачественных заболеваний позволило выявить факторы риска, которые являются общими и для развития рака молочной железы. Все доброкачественные заболевания молочной железы являются в той или иной степени факторами риска. Однако наиболее значимы внутрипротоковая папиллома, киста, узловые формы мастопатии. Наименьший риск несет фиброаденома. Иногда рак молочной железы развивается и без предшествующих доброкачественных изменений, во всяком случае, без их клинических проявлений. Разделение факторов риска на различные группы весьма условно. Это, по-видимому, объясняется сложными, полиэтиологическими аспектами канцерогенеза.
Несмотря на актуальность проблемы рака молочной железы, следует отметить, что на его долю приходится лишь 3-5% от всей патологии молочных желез. Диагностика рака молочной железы и доброкачественных заболеваний основана на единых принципах. Она носит комплексный характер, проводится с участием онколога, рентгенолога, специалиста по ультразвуковой диагностике, морфолога, а также (при необходимости) других специалистов. Значительную роль в диагностическом процессе должны играть акушеры-гинекологи. Это самые «посещаемые» женщинами специалисты, поэтому их онкологическая настороженность может спасти не одну жизнь. Не следует забывать об обучении женщин приемам самообследования. Обращают внимание на анамнестические данные, учитывая при этом все перечисленные факторы риска, сопутствующие заболевания, особенно гинекологические и эндокринологические. Клиническое обследование дает возможность оценить состояние кожи, ареол и сосков (при этом следует обратить внимание на участки уплощения, втяжения, отека кожи, втяжение и эрозию сосков), позволяет определить наличие и характер выделений из сосков. Пальпация в различных позициях позволит определить наличие опухолевидных образований, их размеры, консистенцию, подвижность, контуры, связь с окружающими тканями, кожей и соском. Обязательно должны быть обследованы зоны регионарного лимфооттока: подмышечные, нади подключичные области.
Для изучения состояния молочных желез применяют различные методы. Маммография — рентгенологическое исследование молочных желез, отличающееся высокой эффективностью (98%). Исследование выполняется в первую фазу менструального цикла, а в менопаузе — в любое время. Помимо пленочной маммографии разработана электромаммография, при которой изображение получают на бумаге. Однако из-за недостаточного качества она не приобрела сторонников.
Кроме бесконтрастной маммографии, используются методики искусственного контрастирования: дуктография (контрастирование млечных протоков) и пневмокистография (контрастирование полости кисты). Показанием к дуктографии являются выделения из сосков, особенно кровянистые или «янтарные». Подобные выделения могут являться симптомом внутрипротоковой папилломы или рака. По данным дуктографии можно судить о топографии протока, типе ветвления, проходимости и наличии внутрипротоковых опухолей. При выявлении кисты производят пункционную биопсию, эвакуируют ее содержимое и вводят воздух в объеме удаленного содержимого. На рентгенограммах (пневмокистограммах) отображается внутренняя поверхность стенок кисты, что позволяет обнаруживать внутрикистозные разрастания.
Широкое применение имеет ультразвуковое исследование молочных желез. Оно наиболее информативно при исследовании «плотных» молочных желез у молодых женщин, при выявлении кист, в том числе очень мелких, внутрикистозных разрастаний, в дифференциальной диагностике кист и фиброаденом. Под ультразвуковым контролем можно проводить пункцию молочной железы. Недостатком метода является сравнительно большой процент ложноположительных заключений при доброкачественных образованиях и ложноотрицательных при злокачественных образованиях, расположенных в жировой ткани.
В последнее время в комплексной диагностике заболеваний молочной железы используется магниторезонансная томография. Иногда прибегают к радионуклидной диагностике, которая особенно информативна при «плотной» молочной железе с пальпируемым образованием, а также при рецидивах рака. В некоторых случаях используется термография — метод регистрации теплового излучения. Эффективность этого метода невысока. Использование опухолевых маркеров имеет невысокую диагностическую ценность для раннего выявления рака, чаще применяется для прогноза течения заболевания.
Существенным этапом в установлении диагноза служит морфологический метод. Материалом для цитологического исследования являются выделения из сосков, пунктаты из опухолевидных образований, соскобы с изъязвленных участков, содержимое кист и т.д.
Особое внимание уделяется скрининговым программам, в частности маммографическому скринингу. Главная задача таких программ — раннее выявление злокачественных опухолей, что может снизить смертность при раке молочной железы на 23-50%.
В соответствии с рентгенологическими признаками заболевания молочных желез делятся на доброкачественные дисплазии, злокачественные опухоли и другие патологические состояния. Среди доброкачественных дисплазий выделяют диффузные и локальные формы. К диффузным доброкачественным дисплазиям (мастопатиям) относят аденоз, фиброаденоз, диффузные фиброзно-кистозные мастопатии. К локальным формам дисплазий относятся кисты, фиброаденомы, дуктэктазии и узловые пролифераты. При диффузной кистознофиброзной мастопатии рентгенологическая картина разнообразна: выявляется нарушение структуры молочной железы, определяется множество округлых расплывчатых теней, видны утолщенные тяжи и крупнопетлистая деформация стромы, островки жировой клетчатки с участками фиброза.
При аденоз-мастопатии с преобладанием железистого компонента на маммограмах определяется множество округлых расплывчатых теней. Фиброаденоз представлен комбинацией гиперплазированных железистых долек и внутридольковой соединительной ткани. На рентгенограммах можно увидеть диффузно расположенные множественные микрокальцинаты.
На эхограммах при диффузных доброкачественных дисплазиях паренхима молочных желез может приобретать более высокую эхогенность за счет чередования гиперэхогенных соединительнотканных элементов с менее эхогенными железистыми структурами. Отмечаются утолщение стенок, увеличение просвета, неровность контуров протоков, карманообразные расширения в виде гипоэхогенных зон по ходу главной оси протока.
На фоне мастопатий часто встречаются кисты. Пальпаторно киста определяется как опухолевидное образование округлой формы, плотноэластической консистенции, не связанное с окружающими тканями. На рентгенограммах кисты дают округлые или овальные тени разной величины: от 0,5 до 4-5 см и более. Тень кисты однородна, очертания ровные. При эхографии определяются типичные признаки образований, содержащих жидкость: округлая форма, четкие ровные контуры, анэхогенная структура без отражения, сжимаемость.
Как правило, при выявлении кисты более 1 см проводится ее пункция с аспирацией содержимого. Содержимое кисты подвергается обязательному цитологическому исследованию.
Узловая мастопатия (узловая пролиферация) пальпаторно определяется как узлообразование плотной консистенции с нечеткими контурами. На рентгенограмме выявляются ограниченные участки гиперплазированной железистой ткани высокой плотности без четких границ. При эхографии обнаруживаются единичные или множественные участки сниженной эхогенности без четких контуров и границ. При узловой мастопатии необходимо проведение пункционной биопсии с цитологическим исследованием.
Фиброаденома — доброкачественная опухоль, возникающая из эпителия железистых долек. Пальпаторно определяется как плотное округлое подвижное образование с гладкими контурами. На рентгенограммах визуализируется правильной овальной или округлой формы образование с четкими контурами без перифокальной реакции. Длительно существующие фиброаденомы могут подвергаться обызвествлению. Своеобразным вариантом фиброаденом является филлоидная опухоль, напоминающая фиброаденому, но достигающая крупных размеров: до 7-10 см в диаметре. Эхографически фиброаденома визуализируется как округлое образование с четкими ровными контурами без дополнительных акустических эффектов. При наличии подобных образований проводят пункционную биопсию с цитологическим исследованием.
Внутрипротоковая папиллома — опухоль, располагающаяся в просвете млечного протока. При этом наблюдаются выделения из сосков, которые подвергаются обязательному цитологическому исследованию. При подозрении на наличие данной патологии производится дуктография, позволяющая уточнить диагноз. Внутрипротоковая папиллома визуализируется также при эхографии в виде изолированного расширения протока или солидного образования округлой формы.
Подавляющее большинство злокачественных опухолей молочных желез представляют собой рак (аденокарцинома). Неэпителиальные злокачественные опухоли встречаются редко. К вторичным злокачественным опухолям относятся метастатические поражения. При пальпации они имеют плотную консистенцию, малоподвижны, спаяны с окружающими тканями, имеют нечеткие контуры. Нередко пальпируются увеличенные регионарные лимфатические узлы, имеются так называемые кожные симптомы («лимонная корочка», умбиликация, морщинистость и т.д.). При диффузных формах рака молочной железы обращает на себя внимание увеличение молочной железы, гиперемия и отек кожи, болезненность, повышение температуры, что напоминает картину острого гнойного мастита. Злокачественные опухоли различного гистологического строения не имеют на маммограммах каких-либо специфических черт. Опухоли диаметром до 1 см обычно не пальпируются, особенно при больших размерах молочных желез. Возможности маммографии зависят от строения разных тканей. При преобладании железистой ткани заметить опухолевый узел бывает затруднительно. В подобной ситуации дополнительную информацию может дать ультразвуковое исследование. На фоне жировой инволюции, типичной для старших возрастов, на маммограммах удается определить даже образование величиной 2-3 мм. Тень злокачественной опухоли на снимке всегда меньше, чем ее размеры при пальпации, так как вокруг опухоли развиваются процессы сморщивания, участки инфильтрации и отека ткани. «Раковый» узел обычно имеет форму круга или овала, часто от него отходит дополнительный выступ, направленный к соску, называемый раковым мостиком. Часто опухоль состоит как бы из нескольких примыкающих друг к другу узлов. Очень важным рентгенологическим признаком рака на маммограммах является микрокальцинация. Этим термином обозначают мельчайшие скопления известковых солей в зоне новообразования. Микрокальцинаты обычно расположены в центральных участках опухоли на месте распадающихся раковых клеток, в просвете протоков. Чем больше определяется микрокальцинатов на ограниченном участке, тем выше вероятность злокачественного образования. Особое значение выявление микрокальцинатов приобретает в тех случаях, когда не удается с уверенностью очертить изображение новообразования. Тогда симптом микрокальцинации может оказаться решающим. Необходимо внимательно оценить очертания опухоли. Ее контуры неровны, наблюдаются зазубренность и мелкая волнистость краев узла, от него могут отходить различной величины и формы лучи-спикулы. Существенным признаком растущей опухоли может быть изменение структурного рисунка железы на ограниченном участке. Более того, если сопоставить маммограммы правой и левой молочных желез, то можно заметить и локальную асимметрию их структуры в зоне растущей опухоли.
О степени распространенности опухолевого процесса, в частности при метастатическом поражении подмышечных лимфатических узлов, можно судить по результатам так называемой аксиллографии (рентгенография подмышечных зон).
Внутрикистозный рак выявляется посредством описанной пневмокистографии: на внутренних стенках кисты обнаруживаются плоские, дугообразные или дольчатые разрастания. При эхографии в большинстве случаев узловые формы рака молочной железы представляют собой гипоэхогенные образования. Их эхоструктура разнообразна и зависит от наличия участков некроза, фиброза, кальцинатов, опухолевых сосудов. При диффузной форме определяется утолщение кожи, повышение эхогенности жировой клетчатки, сеть гипоэхогенных, параллельных и перпендикулярных коже трубчатых структур (расширенные инфильтрированные лимфатические сосуды). При этом на фоне повышенной эхогенности паренхимы молочной железы невозможно дифференцировать ее составные части.
Кроме доброкачественных дисплазий и злокачественных опухолей, следует остановиться на других патологических состояниях молочных желез. Проведение маммографии информативно при некоторых аномалиях развития. Так, например, при эктопической закладке железистой ткани уточняется состояние добавочной молочной железы или добавочной доли (часто она расположена в подмышечной области).
Воспалительные процессы, такие как острые маститы, являются нередким поражением, особенно в послеродовом периоде. На маммограммах отмечается интенсивное гомогенное затемнение с нечеткими границами и инфильтрацией субареолярной области. При неблагоприятном течении может сформироваться абсцесс. Очень внимательно следует относиться к пациенткам, у которых мастит возникает вне периода лактации, так как часто клинические проявления мастита могут маскироваться так называемым маститоподобным раком.
При воспалительных заболеваниях молочной железы большую диагностическую ценность имеет ультразвуковое исследование. Диффузная форма мастита характеризуется утолщением кожи, возрастанием эхогенности подкожной клетчатки и паренхимы с потерей четкости их дифференциации. Вовлеченные в воспалительный процесс млечные протоки характеризуются наличием гипоэхогенного гнойного содержимого. Как при рентгеномаммографии, так и при эхографии очень сложно дифференцировать воспалительные изменения от отечно-инфильтративной формы рака молочной железы.
Патологический секрет, выделяемый молочными железами независимо от менструации, беременности, лактации, обусловлен различными патологическими изменениями. Причина такой секреции может быть как экстра-, так и интрамаммарной. Наиболее частыми интрамаммарными причинами являются внутрипротоковая папиллома, интраканаликулярная фиброаденома, гиперпластическая пролиферация эпителия при некоторых формах мастопатии и, что особенно важно, злокачественная опухоль. Патологические выделения могут быть односторонними и, реже, двусторонними. Секрет может выделяться из соска самопроизвольно или при надавливании. Все выделения подвергаются обязательному цитологическому исследованию.
Комплексное маммологическое исследование — это реальный путь повышения качества ранней диагностики, а, следовательно, и улучшения результатов лечения рака молочной железы и доброкачественных заболеваний.
medprosvita.com.ua
Диагностика заболеваний молочных желез - Портал
Несмотря на все достижения теоретической и практической медицины,.
в России ежегодно выявляется более 34 000 новых случаев рака, при этом отмечается резкое снижение возрастного ценза заболевших. За последние 5 лет частота онкологической заболеваемости у подростков в возрасте 17-19 лет увеличилась в среднем на 13%[1].
Первый пик заболеваемости приходится на репродуктивный период от 30 до 40 лет..
По данным статистики число заболевших за этот период составляет 80-100 на 100 000 женщин. В последующие годы жизни отмечается увеличение частоты рака молочных желез, в частности, если в 50 лет регистрируется 180 случаев, то после 65 лет — 250 случаев на 100 000 женщин.
ЧИТАЙ ТАКЖЕ - Клиника предлагает спектр услуг
По данным ВОЗ, к концу столетия раком молочных желез ежегодно будет болеть около 750 тыс. женщин, что может явиться главной причиной смертности женщин в возрасте от 40 до 55 лет [1].
Такая же тенденция прослеживается в большинстве европейских государств. По данным Юнеско, ведущей причиной смерти среди молодых женщин в 28 индустриальных странах за последние 10 лет является рак молочной железы.
C чего начинать
В настоящее время общепризнанно, что рак молочной железы встречается в 3-5 раз чаще на фоне доброкачественных заболеваний молочных желез и в 30-40 раз чаще при узловых формах мастопатии с явлениями пролиферации эпителия молочных желез. В связи с этим очевидно, что в последние годы интерес к доброкачественным заболеваниям значительно возрос, а снижение заболеваемости мастопатией — реальный путь к снижению частоты рака молочной железы.
Классификация
Доброкачественные изменения молочных желез относятся к наиболее распространенным заболеваниям и включают различные по клиническим, морфологическим и этиологическим признакам процессы. Отличительной особенностью молочной железы является сложность четкой дифференцировки физиологических и патологических изменений, а также различных типов доброкачественной диффузной патологии. Это обусловлено тем, что нормальное строение молочной железы характеризуется большой вариабельностью в зависимости от возраста, состояния репродуктивной системы и периода менструального цикла.
По определению ВОЗ (1984), мастопатия — это фиброзно-кистозная болезнь (ФКБ), характеризующаяся нарушением соотношений эпителиального и соединительно-тканного компонентов, широким спектром пролиферативных и регрессивных изменений тканей молочной железы. Мастопатии представляют собой группу гетерогенных заболеваний, имеющих сложную клиническую и гистологическую картину, что весьма затрудняет не только диагностику, но и терминологическое обозначение диффузных процессов. Если по поводу классификаций узловых образований значительных разногласий у специалистов не возникает, то в отношении диффузных форм имеются определенные сложности, не позволяющие ввести довольно широкий спектр изменений в жесткие классификационные рамки. В клинической практике до сих пор широко бытует тенденция относить острые и хронические воспалительные процессы, патологическую секрецию, нарушение развития желез и другие процессы к ФКБ. Заболевания молочной железы вне беременности, объединяемые общим термином “мастопатия”, называют также “дисгормональными дисплазиями”. Данный термин, не отличающийся точностью, отражает в какой-то степени патогенез и отчасти морфологические изменения. На сегоднешний день существует большое число классификаций дисгормональных дисплазий, каждая из которых более или менее полно отражает прогрессивные и регрессивные изменения. В последние годы предложена клинико- рентгенологическая классификация, удобная для пользования в клинической практике и позволяющая выделить диффузные и узловые формы, которые диагностируются с помощью рентгенографии, при ультразвукового сканирования и морфологического исследования. 1. Диффузная форма фиброзно- кистозной мастопатии (ФКМ): — диффузная мастопатия с преобладанием кистозного компонента; — диффузная мастопатия с преобладанием фиброзного компонента; — смешанная форма диффузной мастопатии; — склерозирующий аденоз. 2. Узловая ФКМ Степень выраженности этих процессов определяется условно, по соотношению соединительнотканного, железистого компонентов и жировой ткани. Этиология ФКБ является доброкачественным заболеванием. Однако в ряде случаев данная патология может явиться промежуточной стадией в развитии злокачественного процесса. Поскольку доброкачественные заболевания и рак молочных желез имеют много общего в этиологических факторах и патогенетических механизмах, факторы риска развития мастопатий и рака молочных желез во многом идентичны. На сегодняшний день не выявлено ни одного специфического фактора риска развития данного заболевания, поскольку мастопатия — мультифакторное заболевание, связанное как с генетическими факторами, так и с факторами окружающей среды. В возникновении и развитии дисгормональных заболеваний молочных желез огромная роль отводится состоянию гипоталамо-гипофизарной системы. Нарушение нейрогуморальной составляющей репродуктивного цикла ведет к активации пролиферативных процессов в гормонально зависимых органах, в том числе и в тканях молочных желез, которые являются мишенью для стероидных гормонов яичников, пролактина, плацентарных гормонов и опосредованно гормонов других эндокринных желез организма. Многочисленными клиническими наблюдениями подтверждается, что доброкачественные заболевания молочных желез в 70% случаев сочетаются с различными нарушениями в нейроэндокринной и репродуктивной системах. На общность дисгормональной патологии молочных желез и ряда гинекологических заболеваний указывают многие авторы, которые единодушны в том, что среди многообразия экзо- и эндогенных факторов определяющим в патогенезе доброкачественных заболеваний молочных желез является нарушение ритма секреции гонадотропных гормонов, а возникший при этом гормональный дисбаланс выражается в абсолютной или относительной гиперэстрогении и недостатке прогестерона. Таким образом, решающая роль в развитии заболеваний молочных желез отводится прогестерондефицитным состояниям, при которых избыток эстрогенов вызывает пролиферацию всех тканей железы. Вместе с тем мастопатия нередко наблюдается у женщин с овуляторными циклами и ненарушенной репродуктивной функцией. В данном случае решающая роль в возникновении патологии молочных желез отводится не абсолютной величине гормонов в плазме крови, а состоянию рецепторов половых стероидов в ткани железы, поскольку состояние рецепторного аппарата определяет возникновение патологического процесса [2]. В неизменной ткани молочной железы количество рецепторов минимально. На фоне нарушения гормонального равновесия у одних женщин изменения в молочных железах могут не выходить за рамки физиологической нормы, тогда как у других при условии активации рецепторного аппарата способны перейти в патологический процесс с последующим развитием пролиферативных процессов. Жировая ткань молочной железы содержит гораздо меньше рецепторов и является в качестве депо эстрогенов, прогестерона и андрогенов. Под влиянием ароматазы андрогены превращаются в эстрадиол и эстрон. Этот процесс с возрастом усиливается , что является одним из факторов увеличения риска развития заболеваний молочных желез. В возникновении дисгормональной патологии молочных желез опосредованную роль играют заболевания печени. Как известно, в печени происходит ферментативная инактивация и коньюгация стероидных гормонов. Поддержание постоянного уровня гормонов в циркулирующей крови обусловлено их энтерогепатическим обменом. Выявлено неблагоприятное действие избытка половых гормонов на функцию печени. Заболевания гепатобилиарного комплекса чаще всего инициируют развитие хронической гиперэстрогении вследствие замедленной утилизации эстрогенов в печени. Эти данные подтверждаются большой частотой гиперпластических процессов в молочных железах при заболеваниях печени. Гормоны щитовидной железы (тироксин, трийодтиронин) играют важную роль в морфогенезе и функциональной дифференцировке эпителиальных клеток молочной железы. Действие тиреоидных гормонов на молочную железу может реализовываться различными путями, непосредственно или через действие на рецепторы к другим гормонам, в частности к пролактину. У 64% пациенток с различными формами мастопатии выявлена патология щитовидной железы. Гипофункция щитовидной железы повышает риск возникновения мастопатий в 3,8 раза. Клиническое обследование Первичный осмотр начинается с анализа анамнестических данных. Важное значение в понимании причин возникновения мастопатии имеют данные о перенесенных и особенно сопутствующих заболеваниях половых органов, печени и щитовидной железы. Особого внимания заслуживают сведения о характере и времени начала менструаций. Учитывают возраст наступления первой беременности, число родов, искусственных и самопроизвольных абортов. Не следует пренебрегать данными социально-бытового характера, поскольку известно, что одним из ведущих причинных факторов возникновения мастопатии является длительный психический стресс. Как уже было сказано, у части больных мастопатия проявляется на фоне генетической предрасположенности, в связи с чем важно установить характер заболеваний у ближайших родственников, особенно акцентируя внимание на заболеваниях женских половых органов и молочных желез. Уточняют жалобы, время их появления, связь с менструальным циклом, наличие выделений из сосков, их цвет, консистенцию, длительность и постоянство. Клиническое обследование включает в себя осмотр и мануальное исследование, при котором изучаются степень формирования желез, форма, размеры, состояние кожных покровов, соска, наличие кожных рубцов, втяжений, выбуханий, пигментаций и т. д. Проводится поверхностная и глубокая пальпация желез и региональных лимфатических узлов, которая позволяет определить консистенцию молочных желез, симметричность, наличие уплотнений, их характер, распространенность, наличие отека и соотношение с окружающими тканями. Особое внимание уделяют имеющимся узловым образованиям, определяют их размер, плотность, однородность, количество, подвижность. Маммография Основным методом объективной оценки состояния молочных желез является рентгенмаммография. Эта методика рентгенологического исследования позволяет своевременно распознать патологические изменения в молочных железах в 95-97% случаев. Именно это качество в отличие от других методов диагностики позволяет рассматривать маммографию как ведущий метод скрининга. В последнее время в литературе и особенно в средствах массовой информации появились сообщения о том, что регулярная маммография может способствовать развитию индуцированных раков молочной железы. Однако серьезные исследования, в том числе отечественные, опровергли это заключение [3]. В 1991 г. на Международном симпозиуме по маммографии в Москве были продемонстрированы данные, оценивающие риск маммографического скрининга. Было обнаружено, что при регулярном ежегодном проведении маммографии у 2 млн женщин лишь в одном случае был диагностирован индуцированный рак молочных желез. Л. Е. Денисов (1996) полагает, что 80,1% непальпируемых новообразований в молочных железах выявляются при проведении первичной маммографии. Ежегодное обследование молочных желез позволяет выявить непальпируемый рак I стадии у 92,9% женщин. Высокая ценность данного метода и минимальные дозы облучения позволяют добиться снижения смертности от рака. В настоящее время во всем мире принято (ВОЗ, 1984), начиная с 35 лет, проводить маммографическое исследование 1 раз в 2 года при отсутствии показаний для более частого обследования, после 50 лет — 1 раз в год. Исключением являются кормящие, беременные женщины и подростки, которым маммография назначается только по строгим показаниям. Как правило, маммографию проводят в 2 проекциях (прямой и боковой) на 8-10-й день менструального цикла. Другие методы диагностики Ультразвуковая диагностика дополняет и уточняет картину патологического процесса, полученного при других методах исследования. УЗИ было предложено в качестве вспомогательного исследования в 1951 г., но широкое применение получило лишь с 80-х годов. Данный метод позволяет с высокой точностью распознавать узловатые образования (особенно кисты), оценивать диффузные изменения. Однако диагностическая эффективность при диагностике опухолей менее 1 см составляет 58%, непальпируемых образований — 80%. Кроме того, эхография имеет ряд серьезных недостатков. В первую очередь это невозможность различать микрокальцинаты, являющиеся одним из первых признаков малигнизации, и диагностировать небольшие опухоли, низкая информативность при оценке диффузных изменений, трудности распознавания опухолей на фоне жировой ткани. Все это позволяет использовать УЗИ лишь как дополнительный метод в сочетании с рентгенологическим. Совместное их использование позволяет увеличить точность диагностики различных заболеваний молочных желез до 97%. Ультразвуковую и рентгенологическую маммографию целесообразно считать не альтернативными, а взаимодополняющими методиками, которые должны широко использоваться в диагностическом алгоритме заболеваний молочных желез. Довольно широкое распространение в 70-е годы получил метод термографии, принцип действия которого основан на разности температур кожных покровов над поврежденными и неповрежденными участками, что связано с особенностями кровообращения здоровых и патологически измененных тканей. Абсолютная безвредность, возможность неограниченных контрольных исследований, простота и относительная доступность данного метода привлекли внимание многих исследователей. Однако низкая разрешающая способность, невозможность детализации структуры молочных желез, трудности в выявлении небольших, особенно глубоко расположенных узлов позволяют относить данный метод лишь к вспомогательным методам. Компьютерная томография и ядерно-магнитный резонанс недостаточно информативны при патологии мягких тканей и очень дороги, в связи с чем их применение ограничено. Для диагностики изменений, локализованных в молочных ходах, применяют метод дуктографии. Контрастное вещество с добавлением метиленовой синьки вводят в расширенный молочный проток при помощи тонкой иглы, после чего проводят маммографию в 2 проекциях с последующим выявлением сектора, в котором находится патологическое образование. Для диагностики ФКМ используют пункционную биопсию с последующим цитологическим и морфологическим исследованием биоптата. Гистологическое исследование считается одним из самых важных методов оценки патологического процесса [4]. Точность диагностики составляет 90-100%. С целью определения патологических процессов в молочной железе проводится пневмокистография. Впервые данный метод был предложен французскими маммологами G. Gros и L. Sigrist в 1952 г. для диагностики внутрикистозной патологии. Полость кисты пунктировалась с последующей аспирацией. В спавшуюся кистозную полость вводился воздух в количестве, равном объему эвакуированной жидкости. Для дополнительного контроля полноты опорожнения полости проводилась маммография в двух проекциях. С целью улучшения визуализации G. Heber в 1972 г. предложил перед введением воздуха вводить контрастное вещество для получения двойного контрастирования. Пневмокистография обладает высокой разрешающей способностью для выявления внутрикистозных образований диаметром до 1-2 мм. Как показал дальнейший опыт применения данной методики, возможности пневмокистографии значительно шире, поскольку позволяют не только оценить внутреннее состояние полости кисты, но и обладают высоким терапевтическим эффектом. Так, по данным ряда авторов, терапевтический эффект пневмокистографии достигает 75% [5, 6]. Учитывая многократную лучевую нагрузку на этапе комплексного обследования, в последнее время все чаще используют тонкоигольную аспирационную биопсию под контролем ультразвука, что дает возможность произвести более точную прицельную пункцию, пунктировать кистозные образования диаметром от 0,5 см [7]. Учитывая то, что патология молочных желез зачастую является гормонально зависимым процессом, определение гормонального статуса является обязательным компонентом в комплексном обследовании женщин с заболеваниями молочных желез для правильного выбора лечебной тактики. В первую очередь определяют уровень пролактина в крови, поскольку данные многочисленных исследований свидетельствуют о связи между повышенной секрецией пролактина и ростом заболеваний молочных желез. Имеются сообщения, что у большинства нелеченых больных с диффузной мастопатией содержание пролактина в крови находится на верхней границы нормы [3]. Поиск скрининговых тестов, позволяющих с определенной степенью достоверности судить о вероятности развития патологических процессов в молочных железах, в последние два десятилетия обогатился открытием опухолевых маркеров. Данные литературы свидетельствуют о повышенном уровне опухолевых маркеров в группах женщин с выраженными диффузными формами мастопатий. Определение роли маркеров в прогнозировании возникновения патологии молочных желез более рационально проводить у пациенток, имеющих генетические или анамнестические факторы предрасположенности к злокачественному процессу или с пролиферативными формами мастопатий. По данным ряда авторов, такие онкомаркеры, как раково-эмбриональный антиген (РЭА), высокомолекулярные антигены СА 125 и СА 19-9, муциноподобный раково-ассоциированный антиген (МРА) позволяют осуществлять мониторинг эффективности проводимого лечения [9, 10]. Литература: 1. Сидоренко Л. Н. Молочная железа. Как уберечь себя от рака. 1998. 2. Lamarque J. L. An Atlas of the Breast: Clinical Radiodiagnosis. London, 1984. 3. Бурдина Л. М. Бурдина И. И. Мастодинон и его роль в лечение доброкачестквенных заболеваний молочных желез. Маммология 1998, 4. Богданова Л. И., Чайников И. Г. Сравнительная оценка УЗ и рентгеновской маммографии в диагностике заболеваний молочных желез. Маммологический Центр, г. Ижевск, 1998 5. Рожкова Н. И. Рентгендиагностика заболеваний молочных железы. М., 1993 6. Giatto. S. Morrone D. Bravetti P. Differential diagnosis of intracystic breast lesions in hemorrhagic cystc. Diagnosi differenziale delle lesioni. Radiol. Med. Torino. 1991, 81, 5, p. 592-596. 7. В. П. Харченко, Н. И. Рожкова, С. П. Прокопенко. Новые технологии в диагностике и консервативном лечении кист молочной железы. Московский НИИ диагностики и хирургии МзиМП РФ Маммология, 1999 8. Бодо М. Цитоморфологические и биометрические аспекты диагностики рака и предраковой пролиферации эпителия при дисгормональных гиперплазиях молочных желез. Атореф. Дис. Канд. Мед. наук.-Л. 1981 9. Vecchione A. New and old in prognosis determination. 1993, Nov-Dec, 7 (6B0. p.623-636).10. Yasasever V., Karaloglu D., Erturk N. Diagnostic value of the tumor marcers in breast cancer. Eur. J. Gynaecol Oncol. 1994, 15(1), p. 33-36.
www.vvi-klinika.ru