Гистерорезектоскопия удаление миомы
Удаление субмукозного узла при гистерорезектоскопии
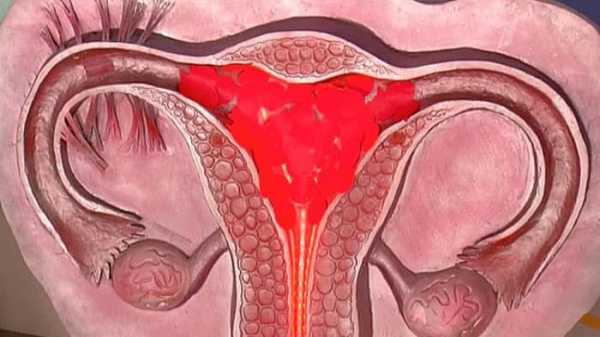
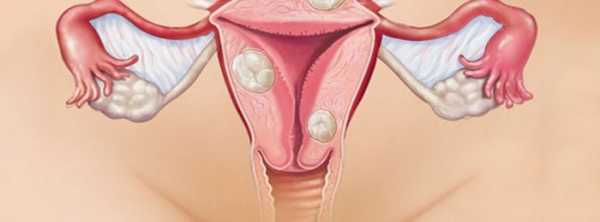
Субмукозная миома матки встречается значительно реже по сравнению с остальными формами доброкачественной опухоли. Локализуется она в глубоких слоях органа под слизистой.
Опасность патологии в том, что при данном расположении миомы болезнь часто сопровождается кровотечениями, приводящими к анемии, и выраженными болями внизу живота, как при физической нагрузке, так и в покое. Но самое плохое, что именно субмукозная миома матки чаще всего является причиной бесплодия. Именно поэтому при выявлении субмукозной миомы матки требуется ее удаление.
Миомы удаляются со стороны полости матки. Как правило, назначается гистерорезектоскопия субмукозного узла. В полость органа вводят гистерорезектоскоп – это тонкий оптический прибор, по сути он такой же, какой используют при офисной гистероскопии. Принципиальная разница между ними – в наличии рабочей части – петли, соединяющейся с прибором, позволяющей срезать миому и прижечь место среза. Преимуществом такой процедуры является отсутствие внешних рубцов на матке, что снижает вероятность осложнений в последующих родах и не влияет на тактику родоразрешения (возможны самостоятельные роды). Продолжительность вмешательства не более часа.
«РАЗМЕР – НЕ ГЛАВНОЕ» – это и про миому тоже.
На тактику лечения субмукозной миомы матки в первую очередь влияет тип и размер узла, общее количество узлов и репродуктивные планы пациента.
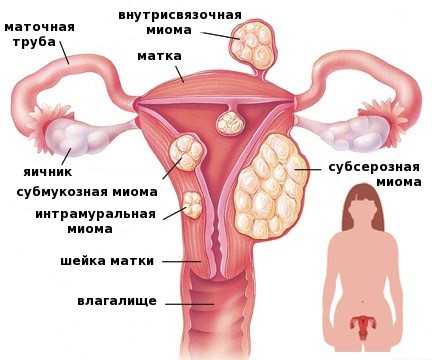
Узлы 0 и 1 типов, как правило, не вызывают сложности в удалении при резектоскопии. Тип узла показывает какая часть миомы расположена в полости матки, т.е. свободна от других тканей, а какая прорастает в стенку.
0 тип – весь узел в полости – самый простой вариант с хирургической стороны, даже при значительных размерах узла. Узел как шарик на тонкой ниточке сосудов соединяется с маткой – «ниточка» находится, прижигается и пересекается. Узел целиком или по фрагментам убирают из полости.
Тип 1 указывает что меньше чем на половину своего объема узел занимает стенку матки. При резектоскопии данный вариант миомэктомии проводится под контролем УЗИ – это необходимо чтобы не забраться глубоко в толщу матки и провести операцию максимально бережно. Перед операцией необходимо тщательное УЗ-исследование и предварительная гистероскопия. Если узел большой, ставится вопрос о двухэтапной тактике лечения, но об этом чуть позже.
Тип 2 – самый сложный из субмукозных – более 50% узла не в полости, а в стенке матки. Необходимо взвесить показания к операции, часто назначается амбулаторное наблюдение и гормональная терапия. Операция проводится в условиях развернутой операционной. Правильная тактика – проводить резекцию узла под контролем лапароскопии (со стороны живота). Это позволяет избежать осложнений и неплановых ситуаций.
Операции при размерах узла более 10 мм
В мировой и отечественной медицине все шире используется гормональная терапия, которая применяется как до хирургического вмешательства, с целью подготовки к операции (узел уменьшается в размерах), так и вместо нее, что, увы, редко встречается в практике. Показания для назначения гормональной терапии определяет только лечащий врач в строго индивидуальном порядке. Необоснованное назначение гормонов, без подбора дозировки и схемы приема опасно для здоровья пациента. При наличии крупных узлов для выполнения органосохраняющей операции требуется предварительно добиться уменьшения их размеров:
- Производится удаление большей доли узла с последующей гормональной терапией или без нее. Через определенный промежуток времени назначается повторная операция по удалению оставшейся части узла.
- Сначала проводится лечение гормональными препаратами и только после уменьшения размера опухоли назначается хирургическое вмешательство.
Послеоперационный период
Все пациенты, перенёсшие гистерорезектоскопию по поводу миомы матки, нуждаются в послеоперационном наблюдении в условиях стационара в течение 1 суток. В индивидуальном порядке пациент может быть выписан в день операции, по решению лечащего врача.
hystero.ru
Что такое гистерорезектоскопия: показания к операции и восстановительный период
Гистерорезектоспокия: что это? Этим вопросом задаются многие женщины, которым для лечения гинекологических заболеваний показано хирургическое вмешательство. Конечно, любая операция — это стресс. Однако не стоит паниковать: гистерорезектоскопия относится к категории так называемых малоинвазивных операций, поэтому восстановительный период не займет много времени. О том, что такое гистерорезектоскопия, вы узнаете из данной статьи.
Показания
Нередко женщины сталкиваются с такими проблемами, как регулярные невынашивания беременности, сложности с зачатием и т. д. Естественно, в подобных случаях врач назначает обследование организма. Если оказывается, что женское здоровье нарушено вследствие появления в матке различных новообразований, например, полипов или миомы, рекомендуется гистерорезектоскопия, или гистерорезекция. Операция позволяет добиться положительных результатов при следующих патологиях:
- частые выкидыши или бесплодие;
- лечение осложнений после аборта;
- гистерорезектоскопия субмукозного узла, то есть подслизистых миом;
- необходимость удаления остатков плодного яйца, внутриматочной спирали или плаценты;
- слишком обильные месячные;
- ликвидация врожденных пороков строения матки, например, перегородок, которые не позволяют зачать и выносить беременность;
- присутствие в матке полипов, миом и других доброкачественных новообразований;
- наличие в матке послеоперационных спаек, которые мешают забеременеть и выносить плод.
Гистерорезектоскопия может проводиться и с диагностическими целями, например, для контроля за послеоперационным восстановлением или реакцией на гормональную терапию. Иногда для этих целей может применяться гистероскопия. А также гистерорезектоскопия нередко проводится при подозрении на злокачественные новообразования матки.
Как осуществляется вмешательство?
Гистерорезектоскопия считается достаточно простой операцией: она хорошо переносится пациентками и чрезвычайно редко вызывает осложнения. Операция принадлежит к категории малоинвазивных вмешательств, в последние годы получивших широкое распространение как в гинекологии, так и в других областях медицины. Главное отличие таких операция от открытых вмешательств в том, что врачу не надо делать разрез на коже: достаточно ввести в полость органа тонкую трубку-эндоскоп, оснащенную диодом, и миниатюрные инструменты для удаления новообразований.
Для выполнения операции от врача требуется довольно высокий уровень квалификации и немалый опыт.
В общей сложности операция длится примерно полчаса. Протекает она в несколько этапов:
- женщина получает общий наркоз. При этом обычно используются довольно легкие препараты, так как длительное обезболивание не требуется. Поэтому состояние после пробуждения быстро приходит в норму. Выбор способа анастезии (масочной, эпидуральной, внутривенной) зависит от состояния пациентки;
- цервикальный канал, проходящий через шейку матки, расширяется, через него вводится либо газ, либо специальная жидкость. Это позволяет увеличить полость органа и лучше визуализировать патологические очаги;
- через цервикальный канал в матку вводится трубка, на одном конце которой расположена камера. Картинка с камеры транслируется на монитор, благодаря чему врач может увидеть все патологические изменения слизистой оболочки органа;
- в случае необходимости в орган вводится резектоскоп: устройство, позволяющее убрать новообразования. Удаление производится при визуальном контроле врача. Например, гистерорезектоскопия миомы матки осуществляется при помощи специального электроножа;
- на месте устраненных новообразований ткани прижигаются, что позволяет предотвратить воспаление;
- из органа выводится жидкость, после чего пациентка отправляется в палату.
Если в ходе гистерорезектоскопии был обнаружен полип, после удаления его отправляют для гистологического исследования. Это позволяет определить, не развивается ли в матке злокачественный процесс.
Есть ли у гистерорезектоскопии противопоказания?
Может показаться, что гистерорезектоскопия отличается простотой. Однако проводить ее можно не каждой женщине. Например, подобное вмешательство противопоказано в следующих случаях:
- обострение хронического заболевания;
- наличие у пациентки ОРВИ или ОРЗ;
- нарушение процесса свертывания крови: в этом случае во время операции может развиться серьезное кровотечение;
- имеются инфекционные заболевания органов мочеполовой системы, например, пациентка заражена хламидиями;
- гистерорезектоскопия противопоказана в случае патологического стеноза цервикального канала, то есть при сужении его просвета.
Абсолютным противопоказанием к операции является беременность. Для женщин в положении резектоскопию рекомендуют только в том случае, если отсутствует необходимость в сохранении беременности. Перед операцией следует проинформировать врача о наличии хронических заболеваний: многие из них считаются противопоказанием для проведения гистерорезектоскопии.
Как подготовиться к операции?
Обычно перед таким вмешательством женщина проходит полное клиническое обследование. Это позволяет определить, имеются ли у пациентки какие-либо противопоказания к гистерорезектоскопии. Важно пройти следующие анализы:
- флюорография;
- электрокардиограмма;
- анализы мочи и крови;
- анализ на различные инфекции (СПИД, сифилис, гепатит В);
- мазок влагалищной микрофлоры.
В зависимости от анамнеза пациентки могут быть назначены дополнительные исследования. В случае выявления каких-либо патологий может потребоваться их предварительное лечение. Непосредственно перед операцией медсестра должна сделать пациентке клизму. А также очень важно опорожнить мочевой пузырь. Перед гистерорезектоскопией нельзя принимать пищу и пить, поэтому обычно операция проводится в утреннее время. И также требуется тщательно подмыться и удалить волосы в области промежности.
Гистерорезектоскопия проводится примерно на шестой день цикла. Если у пациентки уже наступила менопауза, вмешательство может осуществляться в любой день.
Главные преимущества
Гистерорезектоскопия проводится достаточно часто. Связано это с неоспоримыми достоинствами данного метода лечения:
- операция принадлежит к категории малоинвазивных. Она отлично переносится дамами всех возрастов и не требует длительного реабилитационного периода;
- после процедуры женщина может быстро вернуться к своей обычной деятельности;
- гистерорезектоскопия никак не сказывается на репродуктивных функциях: после операции возможна беременность;
- после вмешательства на теле не останется шрамов и рубцов. Это важно не только с эстетической точки зрения: любые открытые операции чреватые серьезными осложнениями, например, воспалением послеоперационного шва. Естественно, в силу своей специфики гистерорезектоскопия подобного недостатка лишена. Это относится к главным различиям малоинвазивных вмешательств.
Восстановление после операции
Как правило, женщина может отправиться домой уже на второй день после такого вмешательства. Однако полный период реабилитации составляет около 14 суток. В это время могут присутствовать довольно неприятные ощущения в нижней части живота, появляются кровянистые выделения. Это не должно пугать: подобные симптомы говорят о восстановлении слизистой оболочки матки. Лечение в этом случае не требуется: после того, как закончится послеоперационный период, они исчезнут самостоятельно.
Чтобы избежать различных инфекций в течение некоторого времени женщине требуется принимать назначенные врачом антибиотики. Если боль после гистерорезектоскопии беспокоит достаточно сильно, можно пить анальгетики.
В течение примерно трех-четырех недель по прошествии вмешательства женщине требуется соблюдать простые правила:
- не поднимать тяжелые вещи;
- не заниматься силовыми видами спорта и не перегружаться;
- купаться только под прохладным душем, отказавшись от горячих ванн;
- уклоняться от спринцевания;
- не переохлаждаться.
В течение месяца не следует жить половой жизнью. Если вы планируете беременность, спросите врача, когда можно начинать предпринимать попытки зачать малыша. Если же целью гистерорезектоскопии было удаление полипа или миоматозного узла, дополнительно требуется принимать гормональные препараты, которые ускоряют процесс послеоперационного восстановления организма. Отказываться от их приема не стоит. Существует множество предрассудков, которые касаются данной группы лекарственных средств, однако, следует помнить, что врач назначает лекарства в определенной дозировке, которая не способна причинить пациентке вреда. Если после приема гормональных таблеток вы почувствовали недомогание, обратитесь к специалисту, чтобы он скорректировал схему лечения. Нельзя изменять ее самостоятельно или замещать препараты!
Осложнения
Гистерорезектоскопия сравнительно редко становится причиной развития осложнений. Однако в некоторых случаях у пациенток бывают:
- газовая эмболия сосудов матки. Это случается крайне редко и связано оно с тем, что используемые для расширения матки газы попадают в кровяное русло;
- перфорация стенки матки. Подобное осложнение может развиваться в случае неаккуратного выполнения хирургического вмешательства недостаточно квалифицированным специалистов. Если врач повредил маточную стенку, развивается массированное кровотечение, которое приводит к обморочному состоянию. В этом случае требуется немедленное восстановление объема циркулирующей крови и другие реанимационные мероприятия;
- гематометра, то есть спазм маточных стенок. Это вызывает обильное кровотечение, в некоторых случаях угрожающее жизни пациентки;
- при сильном поражении слизистой оболочки матки может развиться бесплодие.
Однако опасаться не стоит. Отзывы свидетельствуют о том, что после операции крайне редко развиваются серьезные осложнения. Чтобы обезопасить себя, следует найти хорошего специалиста, обладающего немалым опытом в проведении подобных операция, а также не скрывать от лечащего врача наличие хронических заболеваний.
Какие признаки указывают на развитие послеоперационных осложнений?
После гистерорезектоскопческой процедуры женщина должна особенно внимательно относиться к состоянию своего организма. Как правило, медицинский осмотр требуется через месяц после операции. Посетить специалиста раньше необходимо при появлении следующих симптомов:
- обильные месячные с кровью и сгустками;
- задержка месячных. Обычно менструация восстанавливается уже через месяц после операции. Если менструальный цикл не восстановился, необходимо провести дополнительное обследование организма;
- появление неприятного запаха от половых органов;
- сильные боли в нижней части живота и в пояснице, которые не купируются обезболивающими препаратами;
- повышение температуры тела.
Игнорировать эти симптомы, если они развиваются в послеоперационный период, ни в коем случае нельзя: они могут свидетельствовать о начале серьезных осложнений.
Чем раньше будет назначено необходимое лечение, тем лучше! Комплекс врачебных мероприятий может прописать только доктор. Самолечение в этом случае недопустимо.
Гистерорезектоскопия — операция, которую делают при многих гинекологических заболеваниях. Современные малоинвазивные методы лечения отличаются недолгим восстановительным периодом и высокой эффективностью. Чтобы лучше подготовиться к операции, избавиться от естественного в этой ситуации напряжения, задайте все тревожащие вас вопросы врачу и посмотрите видео, снятые в процессе вмешательства (последнее можно делать только в том случае, если вы не отличаетесь излишней впечатлительностью).
lechim-matku.ru
Гистероскопические операции, гистероскопия
В настоящее время гистероскопия позволяет не только обследовать внутреннюю поверхность матки, но и осуществлять многочисленные операции трансцервикальным доступом. Большое значение в развитии гистероскопии имеет постоянное совершенствование технологического обеспечения. Создание видеомониторов, гистерорезектоскопа позволило, по существу, создать новое направление в гинекологической хирургии.
Гистерорезектоскопия включает целый комплекс гистероскопических операций, которые выполняют с помощью специального электрохирургического инструмента — гистерорезектоскопа или резектоскопа. В течение многих лет для выполнения электрохирургических операций в полости матки использовали монополярный гистерорезектоскоп (рис. 11-4). В последние годы начали использовать биполярный резектоскоп. Этот инструмент считают более безопасным по сравнению с монополярным (рис. 11-5).
Рис. 11-4. Монополярный резектоскоп.
Рис. 11-5. Биполярный резектоскоп.
Гистерорезектоскоп — комплексный инструмент, состоящий из двух основных частей: оптической системы, позволяющей визуализировать объект исследования и следить за ходом операции, а также из рабочей части с набором разных электродов, с помощью которых проводят гистероскопические операции (рис. 11-6).
Рис. 11-6. Электроды для резектоскопа (а, б).
После определения путём визуального осмотра характера внутриматочной патологии диагностическая гистероскопия может перейти в оперативную. Всё зависит от вида выявленной патологии и характера предполагаемой операции. Уровень современного эндоскопического оборудования и возможности гистероскопии на сегодняшний день позволяют говорить об особом разделе оперативной гинекологии — внутриматочной хирургии. Некоторые виды гистероскопических операций заменяют лапаротомию, а иногда и гистерэктомию, что имеет большое значение для женщин репродуктивного возраста или пациенток пожилого возраста с тяжёлой соматической патологией, для которых большой объём оперативных вмешательств представляет риск для жизни.
К гистерорезектоскопическим операциям относят: удаление полипов эндометрия, рассечение плотных внутриматочных синехий, рассечение внутриматочной перегородки, миомэктомию, аблацию эндометрия. Все гистероскопические операции лучше проводить в раннюю фазу пролиферации, если нет необходимости в предварительной подготовке гормональными препаратами. Если проводили гормональную терапию с целью подготовки к операции, то операцию следует проводить через 4–6 нед после последней инъекции при применении агонистов ГнРГ и сразу же после окончания лечения антигонадотропными препаратами.
Для расширения полости матки при работе с монополярным резектоскопом нужно использовать неэлектролитные жидкости, не проводящие электрический ток: 5% раствор глюкозы, 1,5% раствор глицина, реополиглюкин, полиглюкин. При работе с биполярным резектоскопом для расширения полости матки используют простые растворы: 0,9% раствор натрия хлорида, раствор лактатрингера по Хартману©.
Резекция миомы матки. В 1978 г. Neuwirth с соавторами доложили о первом использовании гистерорезектоскопа для удаления субмукозного узла. С этого времени различные исследователи показали эффективность и безопасность данной эндоскопической операции. Трансгистероскопический доступ в настоящее время считают оптимальным для удаления субмукозных миоматозных узлов, что важно для женщин репродуктивного периода, особенно нерожавших. Субмукозная миома матки (рис. 11-7) помимо маточных кровотечений, часто бывает причиной нарушений репродуктивной функции (бесплодия, невынашивания беременности). Выполнение органосохраняющей операции, без образования рубца на матке, имеет большое значение для пациенток, планирующих беременность. Эту операцию с минимальным инвазивным воздействием и лучшими результатами считают альтернативой лапаротомии. При наличии субмукозной миомы с интерстициальным компонентом (1, 2 тип) целесообразно дооперационно проводить эмболизацию ветвей маточных артерий.
Рис. 11-7. Субмукозная миома матки.
Внутриматочные синехии (сращения), или так называемый синдром Ашермана, заключающийся в частичном или полном заращении полости матки, считают одной из причин нарушений менструальной и репродуктивной функций (рис. 11-8).
Рис. 11-8. Внутриматочные синехии (а, б).
В настоящее время единственный метод лечения внутриматочных синехий — их рассечение под прямым визуальным контролем гистероскопа, без травмирования оставшегося эндометрия.
Цель лечения: восстановление нормального менструального цикла и фертильности. Характер операции, её эффективность и отдалённые результаты зависят от вида внутриматочных синехий и степени окклюзии полости матки. Транцервикальное рассечение внутриматочных синехий под контролем гистероскопа считают высокоэффективной операцией. По данным различных авторов, восстановить менструальную функцию и создать нормальную полость матки удаётся в 79–90% случаев. Беременность наступает в 60–75% случаев, при этом патологию прикрепления плаценты наблюдают в 5–31% случаев.
Несмотря на высокую эффективность гистероскопического адгезиолизиса внутриматочных синехий, всё же существует определённая вероятность возникновения рецидива заболевания. Риск особенно высок при распространённых, плотных синехиях (до 60% рецидивов) и у пациенток с туберкулёзным поражением матки.
Для предотвращения рецидива внутриматочных сращений практически все хирурги предлагают вводить в полость матки различные приспособления (катетер Фолея, ВМК) с последующим проведением гормональной терапии (высокие дозы эстрогенгестагенных препаратов) с целью восстановления эндометрия в течение нескольких месяцев. Предпочтительно вводить ВМК на срок не менее 1 мес.
Внутриматочная перегородка — порок развития, при котором полость матки разделена на две половины (гемиполости) перегородкой различной длины (рис. 11-9). Пациентки с внутриматочной перегородкой составляют 48–55% общего числа пациенток с пороками развития половых органов. В общей популяции перегородку в матке выявляют приблизительно у 2– 3% женщин.
Рис. 11-9. Внутриматочная перегородка.
В настоящее время методом выбора лечения внутриматочной перегородки считают рассечение её под визуальным контролем трансцервикальным путём через гистероскоп. Аблация эндометрия. Все операции по деструкции эндометрия называют в литературе «аблация эндометрия». Впервые аблация эндометрия была предложена Badenheuer в 1937 г. Термин «аблация эндометрия» объединяет различные хирургические методики воздействия на эндометрий.
Непосредственное разрушение (деструкцию) всей толщи эндометрия осуществляют с помощью различных методов воздействия: моно и биполярной электрохирургии, лазерной энергии, микроволновой и криохирургии и т.д. При этом невозможно взять ткань на гистологическое исследование.
Резекция эндометрия — иссечение всей толщи эндометрия, может быть произведена только электрохирургически, когда режущей петлёй иссекают всю слизистую оболочку в виде стружки. При таком виде операции есть возможность проведения гистологического исследования иссечённой ткани.
ПОКАЗАНИЯ
Показания к гистероскопической миомэктомии:
- необходимость сохранения фертильности;
- нарушения репродуктивной функции, вызванные развитием субмукозного миоматозного узла;
- маточные кровотечения.
Показания к аблации эндометрия:
- меноррагии при неэффективности гормонотерапии у пациенток старше 35 лет, не планирующих беременность;
- проведение в качестве сопутствующей операции при полипэктомии и миомэктомии в пери и постменопаузе;
- невозможность проведения гормонотерапии при наличии гиперпластических процессов в эндометрии в пре и постменопаузе;
- рецидивирующие гиперпластические процессы эндометрия в пре и постменопаузе.
При подборе пациенток для аблации (резекции) эндометрия также необходимо учитывать следующие факторы: нежелание женщины в дальнейшем беременеть, отказ от гистерэктомии, желание сохранить матку, риск чревосечения. Величина матки не должна превышать (по данным разных авторов) размера 10–12 нед беременности. Наличие миомы не считают противопоказанием к аблации (резекции) эндометрия, но при условии, что ни один из узлов не превышает 4–5 см.
ПРОТИВОПОКАЗАНИЯ
Общие противопоказания к проведению любой гистероскопии:
- величина полости матки более 10 см;
- подозрение на рак эндометрия и лейосаркому;
- опухоль типа II (так называемый центрипетальный рост межмышечной миомы). Относительные противопоказания к гистерорезктоскопии при подслизистой ММ:
- средний диаметр подслизистого опухолевого узла свыше 60 мм (по данным трансвагинальной эхографии);
- опухоль типа I (классификация ESGE), исходящая из дна матки или её перешейка.
Противопоказания к аблации эндометрия:
- злокачественные новообразования половых органов;
- атипическая ГПЭ;
- наличие болевого синдрома;
- величина матки более 9–10 недель беременности;
- пролапс матки.
УСЛОВИЯ ДЛЯ ПРОВЕДЕНИЯ ОПЕРАЦИИ
Независимо от сложности и продолжительности операции, даже для самых коротких манипуляций необходимо иметь полностью оборудованную операционную, чтобы вовремя распознать и начать лечить как хирургические, так и анестезиологические осложнения.
ПОДГОТОВКА К ОПЕРАЦИИ
Предоперационная подготовка к оперативной гистероскопии не отличается от таковой при диагностической гистероскопии. При обследовании пациентки и подготовке к электрохирургической гистероскопической операции необходимо помнить о том, что любая операция может закончиться лапароскопией или лапаротомией.
Обязательный этап перед проведением аблации эндометрия: исключение злокачественных и предраковых процессов в гинекологических органах. Для этого проводят тщательное цитологическое исследование мазков, морфологическое исследование эндометрия, также желательна предварительная гистероскопия, УЗИ органов малого таза трансвагинальным датчиком.
Доказано, что лазерный луч NdYAG лазера и электрическая энергия через электрохирургическую петлю и шаровой электрод проникают и разрушают ткани на глубину 4–6 мм. В то же время даже при нормальном менструальном цикле толщина эндометрия меняется от 1 мм в ранней фазе пролиферации до 10–18 мм в фазе секреции. Следовательно, для получения оптимальных результатов при аблации (резекции) эндометрия толщина эндометрия должна быть менее 4 мм. Для этого операция должна быть выполнена в раннюю фазу пролиферации. Однако это не всегда бывает удобным как для пациентки, так и для врача.
Некоторые авторы предлагают непосредственно перед аблацией эндометрия проводить механический или вакуумный кюретаж полости матки, представляя его как эффективную альтернативу медикаментозной супрессии эндометрия. При этом процедура становится более дешёвой и доступной, позволяет избежать многочисленных нежелательных эффектов гормональной терапии. Кроме того, операция может быть выполнена независимо от дня менструального цикла, а также даёт возможность проведения гистологического исследования эндометрия непосредственно перед аблацией эндометрия.
Однако многие хирурги считают, что кюретаж не обеспечивает достаточного истончения эндометрия и, следовательно, предпочитают готовить эндометрий к аблации с помощью гормонов. При гормональной супрессии эндометрия аблация (резекция) эндометрия может быть выполнена при наитончайшем эндометрии, к тому же гормональная подготовка снижает кровоснабжение матки и уменьшает размеры полости матки. Такая подготовка уменьшает время операции, снижает риск значительной жидкостной перегрузки сосудистого русла и увеличивает процент успешных результатов. С целью гормональной подготовки используют различные препараты: агонисты ГнРГ (гозерелин, трипторелин по 1– 2 инъекции, в зависимости от величины матки), антигонадотропные гормоны (даназол по 400–600 мг ежедневно в течение 4–8 нед) или гестагены (норэтистерон, медроксипрогестерон по 10 мг ежедневно в течение 6–8 нед) и т.д.
МЕТОДЫ ОБЕЗБОЛИВАНИЯ
С целью обезболивания гистероскопических операций более предпочтительно использовать внутривенную анестезию, если не намечена длительная операция (более 30 мин). Для более длительных операций можно применять эндотрахеальный наркоз или эпидуральную анестезию, но если гистероскопию проводят в сочетании с лапароскопией, показан общий эндотрахеальный наркоз.
Особой проблемой анестезиологи считают операции аблации (резекции) эндометрия и миомэктомии ввиду возможных анестезиологических трудностей и изза сложностей в оценке потери крови и баланса жидкости. После таких операций неизбежна абсорбция жидкости, вводимой в полость матки, в сосудистое русло. Анестезиологу необходимо следить за балансом вводимой и выводимой жидкости и информировать хирурга о дефиците жидкости. При дефиците жидкости около 1000 мл необходимо ускорить окончание операции. Дефицит жидкости около 1500–2000 мл считают показанием для срочного прекращения операции. При общей анестезии заметить признаки чрезмерной абсорбции жидкости в сосудистое русло и реакцию пациентки трудно, если не развился отёк лёгких. После пробуждения можно наблюдать признаки церебральной раздражительности (беспокойство, спутанность сознания, головная боль, приводящая к судорогам). В связи с этим, для того чтобы вовремя заметить эти признаки и как можно раньше принять необходимые меры, многие анестезиологи предлагают проводить гистероскопические операции под эпидуральной или спинальной анестезией.
Однако есть пациентки, которые отказываются от данного вида анестезии или у которых есть противопоказания к такому обезболиванию. В этом случае им показан эндотрахеальный наркоз. В ходе операции и анестезии этим пациенткам необходимо определять концентрацию электролитов в крови и желательно определять ЦВД. При выявлении признаков синдрома абсорбции жидкости вводят диуретики и проводят инфузионную терапию под контролем показателей электролитов в крови.
Для успешного выполнения электрохирургических гистероскопических операций необходимо использовать видеомонитор, высокоинтенсивный источник света и эндомат, поскольку точность и правильность проведения операции связаны с чёткостью и чистотой обзора. Такие операции должен выполнять опытный эндоскопист. При проведении ряда гистероскопических операций, таких, как: удаление субмукозных узлов типа II, рассечение толстой внутриматочной перегородки, рассечение распространённых внутриматочных синехий, когда есть риск перфорации матки, — допустимо проведение лапароскопического контроля хода гистероскопической операции.
ТЕХНИКА ОПЕРАЦИИ
Миомэктомия. Для проведения электрохирургической резекции субмукозного узла необходимы: гистерорезектоскоп с режущими петлями диаметром от 6 до 9 мм и шаровой или цилиндрический электрод для коагуляции кровоточащих сосудов.
После расширения цервикального канала расширителями Гегара до № 9–9,5, резектоскоп с диагностическим корпусом вводят в полость матки, идентифицируют узел. Затем диагностический корпус меняют на операционный с электродом. Ткань узла постепенно срезают в виде стружки, при этом петлю постоянно нужно двигать по направлению к себе (рис. 11- 10). Скопившиеся кусочки узла периодически удаляют из матки щипцами или маленькой неострой кюреткой (рис. 11-11). Глубина резекции интерстициальной части узла не должна превышать 8–10 мм от уровня слизистой оболочки.
Интерстициальная часть узла сама выдавливается в полость матки по мере удаления узла. Если этого не происходит, операция должна быть прекращена. В этом случае рекомендуют повторную резекцию оставшейся части узла через 2– 3 мес.
Рис. 11-10. Резекция миоматозного узла (а, б).
Обычно операция не сопровождается значительной кровопотерей, но при повреждении глубоких слоёв миометрия может возникнуть кровотечение, поэтому надо быть осторожным. Мощность электрического тока регулируют в ходе операции под контролем зрения, мощность тока обычно составляет 80–110 Вт в режиме «резать». В конце операции петлевой электрод заменяют на шаровой, снижают внутриматочное давление и коагулируют кровоточащие сосуды в режиме коагуляции при мощности тока 40–80 Вт.
В зависимости от характера узла (субмукозный узел на узком основании или субмукозноинтерстициальный узел) операция может быть выполнена одномоментно или в два этапа. Одномоментное удаление считают более рискованным. При удалении интерстициальной части узла надо всегда помнить о глубине повреждения стенки матки, которое повышает риск развития кровотечения и возможной жидкостной перегрузки сосудистого русла. Если операция выполнена одномоментно, особенно при удалении узла с интерстициальным компонентом, рекомендуют спустя 2–3 мес провести контрольную гистероскопию для того, чтобы выяснить, нет ли какихлибо оставшихся фрагментов миомы. Также возможно выполнение гидросонографии.
Двухэтапную операцию рекомендуют для удаления узлов, у которых большая часть расположена в стенке матки (тип II). На первом этапе проводят гистероскопию и частичную миомэктомию (миолизис оставшейся части узла при использовании лазера). Затем можно назначить гормональные препараты с целью предоперационной подготовки на 8 нед. Можно провести повторную гистероскопию без предварительной подготовки (как правило, через 2–3 мес). За это время оставшаяся часть узла как бы выдавливается в полость матки, и узел легко иссечь полностью. При удалении субмукозных узлов типа II необходим контроль за проведением операции, что можно сделать с помощью трансабдоминального УЗИ или лапароскопии.
Рассечение внутриматочных синехий. Для рассечения синехий, расположенных центрально, можно использовать корпус гистероскопа для разделения синехий тупым путём.
Для рассечения внутриматочных синехий с успехом используют механические инструменты: эндоскопические ножницы и щипцы, гистерорезектоскоп с электродом «электронож», а также NdYAG лазер по контактной методике. Нежные, слабые синехии (эндометриальные) легко рассечь корпусом гистероскопа или механическими инструментами: ножницами и щипцами. Более плотные синехии рассекают ножницами постепенно, шаг за шагом, до восстановления нормальной формы полости матки.
При рассечении плотных, фиброзных синехий лучше использовать гистерорезектоскоп с электродом «электронож». Каждую спайку постепенно рассекают на незначительную глубину, тщательно контролируя освободившуюся полость, и так, шаг за шагом, постепенно проводят всю операцию. Начинать рассечение синехий нужно из нижних отделов и продвигаться в сторону дна матки и устьев маточных труб (рис. 11-12). Операции по рассечению внутриматочных синехий, особенно распространённых, относят к высшей категории сложности. Их должен выполнять опытный эндоскопист.
Рис. 11-12. Рассечение внутриматочных синехий.
Для предотвращения возможной перфорации матки операции проводят под УЗИконтролем при небольшой окклюзии полости матки, и под лапароскопическим — при значительной окклюзии полости матки.
Рассечение внутриматочной перегородки (метропластика). Для выполнения операции используют электрод «электронож» или прямую петлю. Перегородку рассекают постепенно по средней линии, при достижении дна матки возникает кровотечение, что считают сигналом для прекращения операции (рис. 11-13).
Рис. 11-13. Рассечение внутриматочной перегородки (а, б).
При наличии полной перегородки матки рекомендуют сохранять цервикальную часть перегородки для предотвращения вторичной истмикоцервикальной недостаточности. Рассечение перегородки при этом начинают на уровне внутреннего зева. Для успешного проведения этой операции в одну полость вводят катетер Фолея и раздувают, а во вторую — операционный гистероскоп. Затем начинают рассечение перегородки с уровня внутреннего зева и постепенно продвигаются в сторону дна матки. Операцию считают законченной, если удалось сформировать нормальную полость.
Большинство авторов рекомендуют после рассечения широкой внутриматочной перегородки с целью уменьшения риска развития синехий в месте рассечения перегородки и для быстрой эпителизации назначать эстрогены (эстрофем© по 2 мг ежедневно или в I фазу менструального цикла на 2–3 мес).
Аблация эндометрия. Гистероскопические операции аблации эндометрия могут быть лазерными и электрохирургическими.
Лазерная гистероскопическая аблация эндометрия. Пациентка и хирург на время операции должны надевать специальные очки. Лазерный проводник проводят через операционный канал гистероскопа. В качестве среды, расширяющей полость матки, используют простые жидкости: 0,9% раствор натрия хлорида, раствор лактатрингера по Хартману© и т.д. Рекомендуемая мощность NdYAG лазера составляет 30–80 Вт.
Существует две методики лазерного воздействия на эндометрий: контактная и бесконтактная. При контактной методике лазерное волокно прикладывают к поверхности эндометрия в области устьев маточных труб, лазер активизируют нажатием на педаль, и проводник тянут по поверхности эндометрия в направлении шейки матки. При этом правая рука постоянно надавливает на лазерный проводник и потягивает его, а левая рука держит гистероскоп. Важно помнить, что кончик проводника должен быть постоянно в центре обзора и в контакте со стенкой матки. Кончик проводника иллюминирует красным цветом и хорошо виден. При этом образуются параллельные борозды желтоватокоричневатого цвета. Обычно сначала такие борозды делают вокруг устья маточных труб, затем по передней, боковым и в последнюю очередь по задней стенке матки до тех пор, пока вся полость матки не превратится в бороздчатую желтовато- коричневатого цвета поверхность. Обработку внутренней поверхности матки проводят до уровня внутреннего зева, если планируют возникновение аменореи, а если нет, то воздействие лазерным лучом прекращают на расстоянии 8–10 мм от внутреннего зева. Во время вапоризации образуется много пузырьков газа и мелких обрывков эндометрия, ухудшающих обзор. В такой ситуации необходимо подождать, пока их смоет ток жидкости, и обзор станет лучше. При данной методике изза маленького размера кончика лазерного проводника операция длительна по времени, что считают её недостатком.
При бесконтактной методике кончик лазерного проводника проводят над поверхностью стенки матки настолько близко, насколько возможно без касания. При этом проводник необходимо направлять перпендикулярно к поверхности матки. Очередность обработки стенок матки та же, что и при контактной методике. При воздействии лазерной энергии эндометрий становится белым и разбухает, как при коагуляции. Изменения эндометрия менее выражены, чем при контактной методике.
Следует отметить, что полость матки небольшая, и поэтому бывает сложно подвести лазерный проводник перпендикулярно к поверхности матки, особенно в области нижнего сегмента матки. Поэтому часто приходится использовать комбинацию двух методик: контактной и бесконтактной.
Электрохирургическая аблация (резекция) эндометрия. В течение многих лет электрохирургические операции при гистероскопии проводили только с помощью монополярного тока. В последние годы появились инструменты и приборы для биполярной гистероскопической резекции и аблации эндометрия, что считают более безопасной технологией. В качестве среды, расширяющей полость матки, при использовании монополярного тока применяют неэлектропроводные жидкости (1,5% раствор глицина, 5% раствор декстрозы, 5% раствор глюкозы, реополиглюкин, полиглюкин и т.д.). При использовании биполярного тока для расширения полости матки применяют простые жидкости (0,9% раствор натрия хлорида, раствор лактатрингера по Хартману© и т.д.).
Пациентку укладывают на гинекологическое кресло. Предварительно проводят бимануальное исследование для определения положения матки и её величины. После обработки наружных половых органов шейку матки фиксируют пулевыми щипцами, расширяют цервикальный канал расширителями Гегара до № 9–10, в зависимости от модели резектоскопа, величины его наружного корпуса. Операционному столу придают частично положение Тренделенбурга для удержания кишечника дальше от матки, во избежание серьезных осложнений. До начала работы важно убедиться, что в ирригационной системе нет воздуха, что электрические провода исправны, целы, правильно подсоединены.
Когда всё готово, резектоскоп вводят в полость матки. Каждую из сторон матки обследуют детально, особенно если до операции не было диагностической гистероскопии. Выявление полипов эндометрия или субмукозных узлов небольших размеров не считают противопоказанием к операции. Наличие перегородки в матке или двурогой матки также не повод для отказа от операции. Однако в некоторых ситуациях необходимо быть крайне осторожным и несколько изменить технику операции. При выявлении участков эндометрия, подозрительных на малигнизацию, нужно сделать прицельную биопсию этих очагов и отказаться от операции до получения результатов гистологического исследования.
Первоначально должны быть иссечены полипы или миоматозные узлы петлевым электродом. Эти удалённые ткани необходимо отдельно отправить на гистологическое исследование. Только после этого начинают собственно аблацию (резекцию) эндометрия.
При электрохирургической методике используется одна из следующих методик: 1. Аблация эндометрия шаровым или цилиндрическим электродом путём гладильных движений в виде штрихов туда и обратно при мощности тока 75 Вт в режиме «коагуляция» (рис. 11-14).
Рис. 11-14. Аблация эндометрия (а, б).
2. Резекция эндометрия петлевым электродом, при которой эндометрий срезают в виде стружки по всей поверхности сверху вниз, проводят при мощности тока 80–120 Вт в режиме «резать» (рис. 11-15).
Рис. 11-15. Резекция эндометрия (а, б).
3. Комбинированный метод: резекцию эндометрия задней, передней стенок и дна матки петлёй на глубину 3–4 мм. На участках матки более тонких (области трубных углов матки и боковые стенки) не выполняют резекцию эндометрия, а если и выполняют, то используют для этого маленькую петлю. Резецированные кусочки ткани удаляют из полости матки. Затем, сменив электрод на шаровой или цилиндрический и снизив мощность тока в режиме «коагуляция» в зависимости от величины электрода (чем меньше электрод, тем меньше мощность тока), проводят коагуляцию эндометрия в области маточных углов и боковых стенок, а также коагуляцию кровоточащих сосудов.
В конце операции медленно снижают внутриматочное давление и при выявлении кровоточащих сосудов их коагулируют. При любой из этих методик начинать лучше всего с дна матки и области трубных углов, так как это наиболее неудобные области для проведения операции, и их лучше резецировать до того, как не закрылся обзор удалёнными кусочками ткани. Делают зачерпывающие движения вдоль дна матки и мелкие «брительные» движения вокруг устьев маточных труб до миометрия. Следует постоянно помнить о различной толщине миометрия на разных участках матки во избежание глубокой резки с риском перфорации или кровотечения. Манипуляции в матке необходимо проводить так, чтобы электрод находился постоянно в поле зрения. Начинающим хирургам для профилактики осложнений в области дна матки и устьев маточных труб лучше работать, используя шаровой электрод.
После обработки дна матки и области устьев маточных труб операцию проводят на задней стенке матки, так как резецированные кусочки ткани спускаются к цервикальному каналу и задней стенке и ухудшают её обзор. Следовательно, обрабатывать заднюю стенку надо до того, как ухудшился обзор. Движениями петлевого электрода в направлении на себя постепенно резецируют всю заднюю стенку, затем переднюю стенку. Резекцию эндометрия считают достаточной при появлении циркулярных мышечных волокон. При истончённом эндометрии глубина резекции составляет 2–3 мм. Более глубокая резка опасна изза травмирования крупных сосудов с риском развития кровотечения и жидкостной перегрузки сосудистого русла. При работе по боковым стенкам нужно быть осторожным, резка не должна быть глубокой изза опасности повреждения крупных сосудистых пучков. Эти области безопаснее обрабатывать шаровым электродом. По ходу операции и в конце удалённые кусочки ткани извлекают из матки щипцами или небольшой кюреткой очень осторожно во избежание перфорации матки.
Можно использовать и другую технику, при которой выполняют полную, по всей длине, резекцию эндометрия от дна к шейке матки, не двигая режущую петлю внутрь корпуса резектоскопа, а медленно извлекая сам резектоскоп из полости матки. При такой технике образуются длинные фрагменты ткани, которые мешают обзору, и их необходимо после каждой резки извлекать из матки. Преимущество этой методики в том, что полость матки всегда свободна от резецированных тканей. Недостаток состоит в том, что нужно каждый раз извлекать резектоскоп. Это удлинняет операцию и поддерживает кровотечение.
При любой из методик резекцию эндометрия необходимо прекращать, на 1 см не доходя до внутреннего зева во избежание атрезии цервикального канала.
Особого внимания при резекции эндометрия заслуживают пациентки с рубцами в нижнем сегменте матки после операции кесарева сечения. Стенка в этом месте может быть истончена, поэтому резекция должна быть крайне неглубокой. Лучше проводить поверхностную коагуляцию шаровым электродом. В процессе операции при повышенной кровоточивости сосудов, чтобы не увеличивать чрезмерно давление в полости матки, целесообразно периодически вводить в шейку матки невысокие дозы препаратов, влияющих на сократимость миометрия. С этой целью разводят 2,0 мл окситоцина в 10,0 мл изотонического раствора хлорида натрия, и этот раствор по мере необходимости вводят в шейку матки по 1–2 мл.
ОСОБЕННОСТИ ВЕДЕНИЯ ПОСЛЕОПЕРАЦИОННОГО ПЕРИОДА
Особенности послеоперационного ведения больных после гистероскопии зависят от многих факторов: характера патологии в матке, исходного состояния пациентки и половых органов, объёма эндоскопической манипуляции и операции. После проведённой гистероскопии в сочетании с раздельным диагностическим выскабливанием слизистой оболочки матки или простых гистероскопических операций (удаление полипов эндометрия, разрушение нежных внутриматочных синехий, рассечение небольших перегородок, удаление субмукозных миоматозных узлов на узком основании) в специальных рекомендациях необходимости нет. Пациентка может быть выписана из стационара в день операции или на следующий день.
Сукровичные или неинтенсивные кровяные выделения из половых путей наблюдают практически всегда после хирургической гистероскопии в течение 2–4 нед. Иногда выходят кусочки резецированных тканей, которые остались в полости матки. В таких случаях нет необходимости предпринимать какиелибо специальные меры, просто пациентка должна быть предупреждена о возможном появлении подобных выделений.
После рассечения внутриматочных синехий практически все эндоскописты предлагают вводить ВМК в полость матки на 2 мес, поскольку риск возникновения повторных синехий составляет более 50%. Если ввести ВМК возможности нет, допустимо введение в матку катетера Фолея или специального силиконового баллона, которые оставляют в течение недели. В этом случае необходимо назначить антибиотики широкого спектра действия. Для улучшения процессов эпителизации раневой поверхности рекомендуют ЗГТ в течение 2–3 мес.
В послеоперационном периоде у пациенток после рассечения внутриматочной перегородки с неоднократными самопроизвольными выкидышами и после рассечения распространённых внутриматочных синехий проводят профилактический курс антибактериальной терапии. Остальным пациенткам антибиотики можно не назначать.
Источник: Гинекология - национальное руководство под ред. В.И. Кулакова, Г.М. Савельевой, И.Б. Манухина 2009 г.
www.medsecret.net
Осложнения гистероскопии и гистерорезектоскопии: профилактика и лечение
06 Апреля в 18:06 25999
Безусловно, с внедрением в клиническую практику гисте-ро(резекто)скопии внесены существенные коррективы в традиционные каноны диагностики и лечения заболеваний матки. В современной гинекологии гистероскопия является ведущим инструментальным методом диагностики состояний эндометрия, а с появлением гистерорезектоскопии открылась возможность для расширения показаний к органосохраняющим операциям, что позволило не только уменьшить частоту радикальных хирургических вмешательств, но и обеспечить более благоприятное течение послеоперационного периода. В настоящее время гистерорезектоскопия вполне закономерно считается методом выбора хирургического лечения больных с предраком эндометрия, подслизистой миомой матки малых размеров и внутриматочной перегородкой. Вместе с тем, гистеро(резекто)скопия - сравнительно сложная операция, требующая определенного клинического опыта и соблюдения особых мер предосторожности. Поэтому гистеро(резекто)скопия, как впрочем и любое другое хирургическое вмешательство, не может не сопровождаться осложнениями. Тем не менее, частота осложнений гистерорезектоскопии несравнима с таковой радикальных операций. Согласно данным мировой литературы, частота осложнений гистерорезектоскопии варьирует в пределах 0.7-6% (в наших исследования - 2.2%), в то время как частота осложнений абдоминальной гистерэктомии достигает 38-43%.Осложнения гистеро(резекто)скопии подразделяют на следующие группы:
- травматические повреждения;
- кровотечение;
- осложнения, обусловленные особенностями физико-химических свойств сред растяжения полости матки;
- инфицирование;
- бесплодие;
- стеноз шеечного канала и как его следствие - гематометра.
Среди факторов риска механической перфорации матки необходимо выделить:
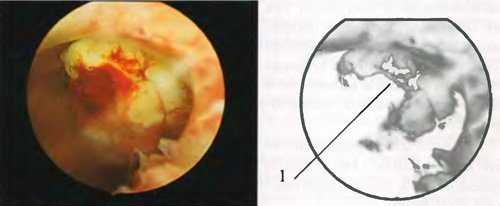
а) ретрофлексию матки; б) стеноз цервикального канала; в) эндомиометрит; г) рак матки; д) инфантильную матку; е) чрезмерные усилия при расширении шеечного канала; ж) несоблюдение правил выполнения внутриматочных вмешательств. Наиболее часто механическая перфорация матки (полная или неполная) наблюдается во время зондирования полости матки и/или расширения шеечного канала. Кроме этого, перфорация матки может произойти при «слепом» введении резектоскопа (острым краем керамического покрытия внутреннего тубуса). Под нашим наблюдением находилась больная Н., 26 лет, которая поступила в клинику для искусственного прерывания беременности. Беременность первая, гестационный срок - 8 недель. При расширении шеечного канала произведена неполная перфорация матки с образованием «ложного» хода в миометрии. Контрольная гистероскопия обнаружила, что «ложный» ход отличают неровные края (фрагменты расслоенного миометрия) и кровоточащая поверхность, а также узкий просвет. Причем диаметр просвета соответствовал таковому расширителя Гегара, посредством которого был окончательно сформирован «ложный» ход. «Ложный» ход «ложный» ход отличают неровные края (1) и кровоточащая поверхность Одним из самых серьезных осложнений гистерорезектоскопии следует считать перфорацию матки высокочастотным электродом или лазерным лучом. Во-первых, перфорация матки теплоэнергетическими факторами приводит не только к повреждению целостности ее стенок, но и может быть причиной достаточно серьезной травмы кишечника. В литературе описаны клинические наблюдения перфорации тонкой кишки и «резекции» фрагмента сигмовидной кишки во время гистерорезектоскопии, повлекшие за собой развитие стойкой нетрудоспособности (в одном наблюдении пациентка перенесла три лапаротомии, резекцию кишечника и колоностомию). Во-вторых, в сравнении с механической перфорацией риск ранения маточных сосудов высокочастотным током или когерентным светом значительно выше (данное осложнение нередко заканчивается летальным исходом; нам известен случай, когда ранение маточных сосудов электродом-петлей явилось причиной геморрагического шока и интраоперационной смерти пациентки). В литературе опубликованы работы, описывающие крайне редкие (почти казуистические) осложнения гистерорезектоскопии. Автор-аноним описал случай разрыва маточных труб вследствие чрезмерного растяжения полости матки углекислым газом. На наш взгляд, вероятная причина подобного осложнения кроется в элементарном несоблюдении правил безопасности - подача газа в полость матки осуществлялась без специального редуктора (гистерофлатора) или вместо гистерофлатора был использован лапарофлатор, обеспечивающий более высокую скорость поступления газа. R.Macdonald et al. сообщили о, казалось бы, невероятном инциденте перфорации нижней полой вены в ходе гистерорезектоскопии. В качестве комментария к сообщению авторов следует констатировать, что особую опасность представляет своевременно недиагностированная перфорация матки во время гистерорезектоскопии: иногда хирург, как правило, начинающий, неадекватно оценивает степень риска хирургического вмешательства и поэтому «не замечает» перфорации матки, продолжая выполнение уже осложнившейся операции, усугубляя, тем самым, тяжесть ее последствий.
«Ложный» ход «ложный» ход отличают неровные края (1) и кровоточащая поверхность Одним из самых серьезных осложнений гистерорезектоскопии следует считать перфорацию матки высокочастотным электродом или лазерным лучом. Во-первых, перфорация матки теплоэнергетическими факторами приводит не только к повреждению целостности ее стенок, но и может быть причиной достаточно серьезной травмы кишечника. В литературе описаны клинические наблюдения перфорации тонкой кишки и «резекции» фрагмента сигмовидной кишки во время гистерорезектоскопии, повлекшие за собой развитие стойкой нетрудоспособности (в одном наблюдении пациентка перенесла три лапаротомии, резекцию кишечника и колоностомию). Во-вторых, в сравнении с механической перфорацией риск ранения маточных сосудов высокочастотным током или когерентным светом значительно выше (данное осложнение нередко заканчивается летальным исходом; нам известен случай, когда ранение маточных сосудов электродом-петлей явилось причиной геморрагического шока и интраоперационной смерти пациентки). В литературе опубликованы работы, описывающие крайне редкие (почти казуистические) осложнения гистерорезектоскопии. Автор-аноним описал случай разрыва маточных труб вследствие чрезмерного растяжения полости матки углекислым газом. На наш взгляд, вероятная причина подобного осложнения кроется в элементарном несоблюдении правил безопасности - подача газа в полость матки осуществлялась без специального редуктора (гистерофлатора) или вместо гистерофлатора был использован лапарофлатор, обеспечивающий более высокую скорость поступления газа. R.Macdonald et al. сообщили о, казалось бы, невероятном инциденте перфорации нижней полой вены в ходе гистерорезектоскопии. В качестве комментария к сообщению авторов следует констатировать, что особую опасность представляет своевременно недиагностированная перфорация матки во время гистерорезектоскопии: иногда хирург, как правило, начинающий, неадекватно оценивает степень риска хирургического вмешательства и поэтому «не замечает» перфорации матки, продолжая выполнение уже осложнившейся операции, усугубляя, тем самым, тяжесть ее последствий. Меры профилактики перфорации матки достаточно просты и требуют лишь внимания хирурга и его ассистентов:
1) перед гистеро(резек-то)скопией хирург обязан произвести двуручное исследование, чтобы оценить позицию и величину матки; 2) зондирование матки и расширение ее шеечного канала необходимо осуществлять бережно, без чрезмерных усилий; при дилатации шеечного канала не следует пренебрегать расширителями Гегара с промежуточными значениями (7.5; 8.5 и т.д.); 3) введение гистеро(ре-зекто)скопа производят строго под контролем зрения; 4) при работе с электродом типа «петля» или «игла» электрогенератор активируют до соприкосновения режущей поверхности электрода со слизистой во избежание проникающего ранения матки и маточных сосудов высокочастотным сигналом; 5) электрод активируют только при его перемещении по направлению к тубусу резектоскопа; исключается подача тока при перемещении электрода от тубуса (за исключением электрохирургической метропластики); 6) подачу тока с электрогенератора осуществляют исключительно под визуальным контролем; является недопустимым подведение электрического сигнала при нахождении электрода вне зоны видимости; 7) при высоком риске перфорации матки (иссечение внутриматочной перегородки у пациенток с двурогой маткой; резекция подслизистой миомы матки на широком основании) гистерорезектоскопию выполняют под контролем лапароскопии; 8) с целью предупреждения перфорации шейки матки и/или ее перешейка введению резектоскопа предшествует введение наружного тубуса с обтуратором, имеющим гладкую безопасную поверхность; 9) патогномоничными «признаками» перфорации матки являются: «проваливание» гистеро(резекто)скопа за пределы матки, резкое «спадание» стенок полости матки, избыточный расход жидкости.Кроме чисто технических аспектов профилактики перфорации матки и ранения маточных сосудов во время гистерорезектоскопии необходимо акцентировать внимание и на других факторах:
1) хирург обязан оценивать свои возможности, их переоценка нередко приводит к развитию интраоперационных осложнений; 2) хирург не должен надеяться на постороннюю помощь; врач, выполняющий гистерорезектоскопию, обязан владеть полным объемом экстренной хирургии и в случае перфорации матки и/или ранения маточных сосудов произвести соответствующие корригирующие мероприятия. Перфорация матки высокочастотным электрическим током или лазерным лучом, следствием которой могут быть ранения кишечника, мочевого пузыря, магистральных сосудов малого таза, является одним из наиболее тяжелых осложнений гистерорезектоскопии. В связи с этим, при высоком риске подобных осложнений гистерорезектоскопию целесообразно осуществлять под контролем лапароскопии.Показаниями для лапароскопического мониторинга служат следующие клинические ситуации:
- электрохирургический (лазерный) лизис внутриматочных сращений; лизис плотных краевых спаек требует лапароскопического контроля, так как сопряжен с риском перфорации матки; при центральных и/или изолированных спайках отсутствует необходимость в лапароскопическом мониторинге;
- рассечение внутриматочной перегородки (абсолютное показание для лапароскопического контроля);
- электрохирургическая миомэктомия; резекцию подслизистых опухолей на широком основании, расположенном вблизи серозного покрова матки, следует производить под контролем лапароскопии; удаление подслизистых узлов миомы на «ножке» или широком неглубоком основании не нуждается в лапароскопическом мониторинге.
 Кровотечение из резецированного узла миомы: 1 - кровоточащая поверхность опухоли С целью профилактики интраоперационного кровотечения ряд авторов рекомендует производить гормональную подготовку эндометрия препаратами, стимулирующими атрофические процессы в слизистой тела матки.
Кровотечение из резецированного узла миомы: 1 - кровоточащая поверхность опухоли С целью профилактики интраоперационного кровотечения ряд авторов рекомендует производить гормональную подготовку эндометрия препаратами, стимулирующими атрофические процессы в слизистой тела матки. Основу интраоперационного гемостаза составляют изложенные ниже принципы:
1) электрохирургическую деструкцию эндометрия и подслизистых опухолей мышечной оболочки матки осуществляют в режиме «резание + коагуляция»; 2) во избежание ранения крупных сосудов слизистой, расположенных преимущественно в проекции трубных углов матки и ее боковых стенок, электрокаутеризацию указанных анатомических областей производят с помощью электродов с широкой рабочей поверхностью (шар, бочонок, ролик); 3) первоначально для остановки диффузного кровотечения из слизистой тела матки применяют электрокоагуляцию кровоточащих участков электродами с широким основанием (шар, бочонок, ролик); при неэффективности последней прибегают к тампонаде полости матки; 4) для гемостатической тампонады полости матки используют следующие методы: а) баллонодилатацию - специальный пластиковый баллон (или воздушный латексный шар) вводят в полость матки и заполняют жидкостью (физиологический раствор, растворы антисептиков) в количестве около 80-100 мл в зависимости от объема полости матки; под давлением жидкости стенки баллона расправляются и тампонируют кровоточащую слизистую; для баллонодилатации можно использовать также катетер Foley; б) марлевую тампонаду - марлевый тампон, пропитанный 3% раствором перекиси водорода или растворами гемостатических веществ (вазопрессин, терлипрессин, аминокапроновая и транексамовая/трансамча, циклокапрон/ кислоты, этамзилат/дицинон/), вводят в полость матки по типу тугой тампонады; при извлечении марлевого тампона его предварительно орошают жидкими средами; 5) в случае кровотечения из шеечного канала или перешейка матки (как правило, в результате неполной перфорации матки тубусом резектоскопа) лигируют нисходящие ветви маточных сосудов - накладывают узловые швы на боковые стенки шейки матки, ориентируясь на область ее перешейка. Анализ особенностей физико-химических свойств различных сред растяжения полости матки, представленный в главе 3, показал, что не существует идеальной среды растяжения: каждую из них отличают свои преимущества и недостатки, обусловленные как объемом хирургического вмешательства, так и типом теплоэнергетического воздействия на ткани. Поэтому при выборе контрастирующей среды для гистерорезектоскопии руководствуются, главным образом, двумя факторами: а) безопасностью пациента (т.е. снижение риска возможных осложнений) и б) обеспечением оптимальной визуализации в окуляре телескопа.В соответствии с требованиями безопасности пациента «идеальная» среда растяжения полости матки должна обладать следующими свойствами:
1) не вызывать гемолиз и эмболию; 2) обладать минимальным воздействием на плазму; 3) не повышать осмотическое давление. Наиболее частыми осложнениями инсуфляции СО2 в полость матки являются нарушения сердечной деятельности, ацидоз, механические повреждения тканей, газовая эмболия. Формирование указанных осложнений во многом определяют такие факторы, как скорость потока газа и его давление. Так, нарушения сердечной деятельности и ацидоз развиваются при скорости потока углекислого газа 400 мл/мин, а газовая эмболия с летальным исходом - при скорости потока газа 1000 мл/мин, нагнетаемого в течение 2 мин. Поэтому, несмотря на «идеальные» оптические свой ства углекислого газа, целесообразность его применения в качестве среды растяжения полости матки остается дискуссионной.Ряд авторов придерживается мнения, что строгий контроль над скоростью потока и давлением углекислого газа, инсуфлируемого в полость матки с помощью электронных гистерофлаторов сводит к минимуму риск развития ацидоза и газовой эмболии. Однако, на наш взгляд, даже минимальный риск подобного осложнения (по данным Pierre F. et al. - 0.58 на 1000 исследований) диктует необходимость отказа от применения газовых сред для растяжения полости матки. Более того, СО2 не может быть использован в качестве среды растяжения во время гистерорезектоскопии (абсолютное противопоказание), поскольку при теплоэнергетическом воздействии на ткани резко возрастает риск эмболизации.
Главный недостаток растворов-диэлектриков с низкой вязкостью, широко применяемых для гистерорезектоскопии (5% раствор глюкозы, маннитол, сорбитол, глицин) - их способность вызывать гипергидратацию и, соответственно, гипонатриемию (водная интоксикация). Клиническими симптомами тяжелых форм гипонатриемии являются брадикардия, артериальная гипертензия, тошнота, рвота, судороги, отек легких и декомпенсированные нарушения сердечной деятельности. Известны случаи летальных исходов вследствие жидкостной перегрузки. Основная причина гипергидратации во время гистерорезектоскопии - чрезмерная интравазация растворов с низкой вязкостью в результате образования больших венозных пазух и/или повреждения тканей (неполная перфорация матки, глубокая резекция эндометрия, электрохирургическая миомэктомия). Учитывая, что растворы, используемые для гистерорезектоскопии, гипотонические, их избыточная концентрация в сосудистом русле приводит к снижению осмолярности плазмы, нарушая K/Na-отношение. Изменение K/Na-баланса сопровождается повреждением гематоэнцефалического барьера, преодолевая который, излишнее количество воды проникает в межклеточное и межтканевое пространство мозга, увеличивая, тем самым, его гидростатическое давление. Таким образом, развивается отек мозга, который приводит к снижению мозгового кровотока, увеличению внутричерепного давления и, следовательно, гипоксии ткани мозга. В исследовании M.S.Baggish et al. проведен анализ двух случаев тяжелой гипонатриемии, возникшей в результате гипергидратации 3% раствором сорбитола и 1.5% раствором глицина, последствиями которой явились кома, остановка дыхания и смерть. Содержание натрия в плазме этих больных составило соответственно 121 и 102 ммоль/л. Посмертное вскрытие обнаружило, что в обоих наблюдениях имела место мозговая грыжа. Безусловно, определенными качествами «идеальной» среды растяжения полости матки обладает изотонический (0.9%) раствор хлорида натрия, поскольку изотонический раствор не оказывает раздражающего действия на ткани, быстро выводится из сосудистой системы и лишь временно увеличивает объем циркулирующей жидкости. Изотонический раствор не решает проблему жидкостной перегрузки, однако его чрезмерная интравазация не приводит к формированию отека мозга. Тем не менее, как солевой раствор хлорид натрия абсолютно неприемлем для электрохирургической резектоскопии: свободные электролиты раствора образуют достаточно большую площадь сечения, обуславливая резкое снижение электрического потенциала. Опыт собственных исследований убеждает: следование правилам безопасности при выполнении гистерорезектоскопии (что, впрочем, является обязательным условием любого хирургического вмешательства) сводит к нулю риск развития тяжелых форм гипонатриемии.К указанным правилам относят:
1) детальное дооперационное обследование пациенток, включающее анализ содержания электролитов в сыворотке крови; 2) неукоснительное соблюдение противопоказаний к гистерорезектоскопии; 3) строгий учет расхода потребляемой жидкости; 4) адекватный контроль над скоростью потока и давлением внутриматочной инфузии. Вместе с тем, вопросы лечения гипонатриемии, учитывая вероятность летального исхода, заслуживают особого внимания.Меры профилактики и терапии острой гипонатриемии включают следующие основные этапы:
1) немедленное прекращение операции при подозрении на гипонатриемию и/или перерасходе жидкости (лимит последней составляет 2 л); более того, в определенных клинических ситуациях (как правило, при подслизистой миоме матки сравнительно большой величины) следует предупреждать пациенток о возможности отсроченной повторной операции; под нашим наблюдением находились больные с подслизистой миомой матки, у которых диаметр опухоли достигал 4-5 см; в подобных случаях мы целенаправленно производили повторную гистерорезектоскопию спустя 1 месяц от момента первого хирургического вмешательства, что позволило не только предотвратить развитие осложнений, но и улучшить отдаленные результаты хирургического лечения: при контрольной гистероскопии, выполненной в отсроченном периоде, ранее резецированные опухоли отличались гладкой блестящей поверхностью и небольшими размерами; для их окончательного удаления потребовалось не более 5-7 минут;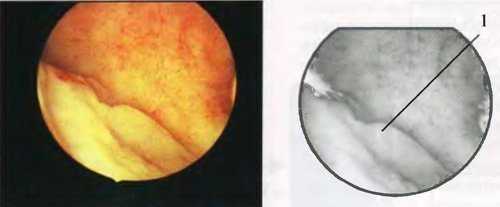 Отсроченная миомгистероректэктомия 2) парентеральное введение диуретиков; несмотря на то, что традиционная терапия гипонатриемии заключается в ограничении жидкости и наблюдении, острая постхирургическая водная интоксикация требует ускоренного выведения свободной воды из организма; 3) почасовой контроль содержания электролитов в сыворотке крови до нормализации клинико-лабораторных показателей; 4) мониторинг деятельности сердечно-сосудистой, дыхательной и мочевыделительной систем; 5) внутривенная инфузия изотонического раствора хлорида натрия (в первые часы острой гипонатриемии допускается введение малых доз гипертонического раствора). В отличие от жидкостей с низкой вязкостью, интравазация которых приводит к снижению осмолярности плазмы, растворы с высокой вязкостью (гискон) при проникновении в кровь повышают онкотическое давление плазмы. И в том и в другом случае происходит увеличение объема циркулирующей жидкости (различие заключается лишь в его механизме). Следовательно, проблема растворов с высокой вязкостью идентична таковой низкомолекулярным соединениям -жидкостная перегрузка, обуславливающая развитие отека легких. Хорошо известно, что гискон - гидрофильное вещество и при проникновении в кровь способен увеличивать объем циркулирующей жидкости, по крайней мере, в шесть раз.
Отсроченная миомгистероректэктомия 2) парентеральное введение диуретиков; несмотря на то, что традиционная терапия гипонатриемии заключается в ограничении жидкости и наблюдении, острая постхирургическая водная интоксикация требует ускоренного выведения свободной воды из организма; 3) почасовой контроль содержания электролитов в сыворотке крови до нормализации клинико-лабораторных показателей; 4) мониторинг деятельности сердечно-сосудистой, дыхательной и мочевыделительной систем; 5) внутривенная инфузия изотонического раствора хлорида натрия (в первые часы острой гипонатриемии допускается введение малых доз гипертонического раствора). В отличие от жидкостей с низкой вязкостью, интравазация которых приводит к снижению осмолярности плазмы, растворы с высокой вязкостью (гискон) при проникновении в кровь повышают онкотическое давление плазмы. И в том и в другом случае происходит увеличение объема циркулирующей жидкости (различие заключается лишь в его механизме). Следовательно, проблема растворов с высокой вязкостью идентична таковой низкомолекулярным соединениям -жидкостная перегрузка, обуславливающая развитие отека легких. Хорошо известно, что гискон - гидрофильное вещество и при проникновении в кровь способен увеличивать объем циркулирующей жидкости, по крайней мере, в шесть раз. 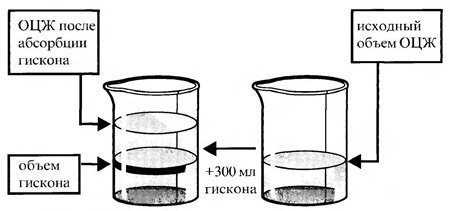 Изменение объема циркулирующей жидкости в ответ на абсорбцию гискона Однако остается неуточненным вопрос: какое количество высокомолекулярного раствора приводит к формированию отека легких? M.S.Baggish et al. попытались предсказать порог токсичности гискона, но обнаружили лишь недостоверную корреляцию между объемом инстиллируемого декстрана и его концентрацией в крови через 30 мин после введения препарата. Существует точка зрения, согласно которой, дексгран-70 обладает прямым токсическим эффектом на легочные капилляры, вызывая экстравазацию и внутритканевой отек легких. Полагают, что гискон влияет на свертываемость крови: в литературе имеются сообщения о развитии диссеминированной внутрисосудистой коагулопатии в ответ на внутриполостную инфузию декстрана-70. M.S.Baggish et al. установили, что гискон способствует уменьшению синтеза фибриногена, не влияя на уровень продуктов распада фибрина. По мнению S.Cronberg et al., гискон обуславливает слипание и агрегацию тромбоцитов. Гискон является аллергеном, осложнениями которого могут быть не только изменения кожи (сыпь, локальная гиперемия, сопровождающаяся зудом), но и сердечный коллапс. Частота анафилактических реакций с летальным исходом при использовании декстрана-70 в качестве среды растяжения полости матки варьирует в пределах 0.008-0.069%. Аспекты терапии жидкостной перегрузки гисконом окончательно не изучены. Высокая молекулярная масса декстрана-70 затрудняет его фильтрацию почками, а единичные работы, посвященные применению для этих целей плазмофереза, не решают проблему. Итак, сравнительно высокая частота осложнений декстрана-70, его непредсказуемая гидрофильность (способность в малых концентрациях в несколько раз увеличивать объем циркулирующей жидкости), отсутствие четких концепций в лечении осложнений гискона в сочетании с «техническими» недостатками высокомолекулярного соединения (из-за высокой вязкости гискона крайне сложно обеспечить его постоянный отток из полости матки; кроме этого, гискон образует плотный налет на поверхности инструментов, что существенным образом затрудняет выполнение операции) - в совокупности диктуют необходимость отказа от применения гискона в качестве среды растяжения полости матки во время гистерорезектоскопии. Частота инфекционных осложнений гистерорезектоскопии достаточно низкая и не превышает 0.17-2.9%. Однако в структуре указанных осложнений имеют место сепсис и бактериальный шок. S.Amin-Hanjani et J.M. Good наблюдали формирование пиометры и бактериемии после электрохирургической аблации эндометрия. Поэтому мы являемся сторонниками профилактической противовоспалительной терапии, направленной на предупреждение септических осложнений в послеоперационном периоде. Как показали наши исследования, профилактическая антисептическая терапия не только обеспечивает благоприятное течение послеоперационного периода, но и способствует ускорению регенерации слизистой тела матки после резектоскопии. Тотальная аблация эндометрия у пациенток молодого репродуктивного возраста сопряжена с высоким риском развития бесплодия или невынашивания беременности. Вместе с тем, бесплодие после гистерорезектоскопии лишь условно можно расценивать как послеоперационное осложнение, так как потеря способности эндометрия к восприятию оплодотворенной яйцеклетки является скорее закономерным итогом, чем осложнением. Тем не менее, к электрохирургической аблации слизистой тела матки нельзя относится как к методу стерилизации, поскольку электродеструкция эндометрия не обеспечивает 100% контрацептивный эффект. В литературе описаны наблюдения беременности после гистерорезектоскопии, закончившиеся неосложненными родами. Однако отсутствие отдаленных перинатальных исходов оставляет открытым вопрос о целесообразности родоразрешения после тотальной аблации эндометрия. Стеноз шеечного канала и, как его следствие - гематометра после гистерорезектоскопии формируются в результате электродеструкции однослойного цилиндрического эпителия, выстилающего канал шейки матки. Раневые поверхности шеечного канала, возникшие в результате хирургического вмешательства, слипаются между собой, образуя рубцовое сращение и, тем самым, препятствуют выходу крови из полости матки. Во избежание подобного осложнения не рекомендуется осуществлять электро- или лазеркоагуляцию слизистой шеечного канала при выполнении аблации эндометрия. Не является поводом для дискуссий, что никому из хирургов (независимо от их квалификации) не удалось избежать интра- или постоперационных осложнений различной степени тяжести. По-видимому, отсутствие хирургических осложнений в деятельности практикующего врача свидетельствует либо о незначительном опыте специалиста, либо об отсутствии такового в целом. В настоящее время проблеме хирургических осложнений отводится пристальное внимание, учитывая, что только глубокий анализ собственных осложнений, а также осложнений коллег-специалистов позволяет разработать эффективные превентивные действия. Хирург, скрывающий свои осложнения, лишает своих коллег, особенно начинающих, возможности предотвратить подобные осложнения. А.Н. Стрижаков, А.И. Давыдов
Изменение объема циркулирующей жидкости в ответ на абсорбцию гискона Однако остается неуточненным вопрос: какое количество высокомолекулярного раствора приводит к формированию отека легких? M.S.Baggish et al. попытались предсказать порог токсичности гискона, но обнаружили лишь недостоверную корреляцию между объемом инстиллируемого декстрана и его концентрацией в крови через 30 мин после введения препарата. Существует точка зрения, согласно которой, дексгран-70 обладает прямым токсическим эффектом на легочные капилляры, вызывая экстравазацию и внутритканевой отек легких. Полагают, что гискон влияет на свертываемость крови: в литературе имеются сообщения о развитии диссеминированной внутрисосудистой коагулопатии в ответ на внутриполостную инфузию декстрана-70. M.S.Baggish et al. установили, что гискон способствует уменьшению синтеза фибриногена, не влияя на уровень продуктов распада фибрина. По мнению S.Cronberg et al., гискон обуславливает слипание и агрегацию тромбоцитов. Гискон является аллергеном, осложнениями которого могут быть не только изменения кожи (сыпь, локальная гиперемия, сопровождающаяся зудом), но и сердечный коллапс. Частота анафилактических реакций с летальным исходом при использовании декстрана-70 в качестве среды растяжения полости матки варьирует в пределах 0.008-0.069%. Аспекты терапии жидкостной перегрузки гисконом окончательно не изучены. Высокая молекулярная масса декстрана-70 затрудняет его фильтрацию почками, а единичные работы, посвященные применению для этих целей плазмофереза, не решают проблему. Итак, сравнительно высокая частота осложнений декстрана-70, его непредсказуемая гидрофильность (способность в малых концентрациях в несколько раз увеличивать объем циркулирующей жидкости), отсутствие четких концепций в лечении осложнений гискона в сочетании с «техническими» недостатками высокомолекулярного соединения (из-за высокой вязкости гискона крайне сложно обеспечить его постоянный отток из полости матки; кроме этого, гискон образует плотный налет на поверхности инструментов, что существенным образом затрудняет выполнение операции) - в совокупности диктуют необходимость отказа от применения гискона в качестве среды растяжения полости матки во время гистерорезектоскопии. Частота инфекционных осложнений гистерорезектоскопии достаточно низкая и не превышает 0.17-2.9%. Однако в структуре указанных осложнений имеют место сепсис и бактериальный шок. S.Amin-Hanjani et J.M. Good наблюдали формирование пиометры и бактериемии после электрохирургической аблации эндометрия. Поэтому мы являемся сторонниками профилактической противовоспалительной терапии, направленной на предупреждение септических осложнений в послеоперационном периоде. Как показали наши исследования, профилактическая антисептическая терапия не только обеспечивает благоприятное течение послеоперационного периода, но и способствует ускорению регенерации слизистой тела матки после резектоскопии. Тотальная аблация эндометрия у пациенток молодого репродуктивного возраста сопряжена с высоким риском развития бесплодия или невынашивания беременности. Вместе с тем, бесплодие после гистерорезектоскопии лишь условно можно расценивать как послеоперационное осложнение, так как потеря способности эндометрия к восприятию оплодотворенной яйцеклетки является скорее закономерным итогом, чем осложнением. Тем не менее, к электрохирургической аблации слизистой тела матки нельзя относится как к методу стерилизации, поскольку электродеструкция эндометрия не обеспечивает 100% контрацептивный эффект. В литературе описаны наблюдения беременности после гистерорезектоскопии, закончившиеся неосложненными родами. Однако отсутствие отдаленных перинатальных исходов оставляет открытым вопрос о целесообразности родоразрешения после тотальной аблации эндометрия. Стеноз шеечного канала и, как его следствие - гематометра после гистерорезектоскопии формируются в результате электродеструкции однослойного цилиндрического эпителия, выстилающего канал шейки матки. Раневые поверхности шеечного канала, возникшие в результате хирургического вмешательства, слипаются между собой, образуя рубцовое сращение и, тем самым, препятствуют выходу крови из полости матки. Во избежание подобного осложнения не рекомендуется осуществлять электро- или лазеркоагуляцию слизистой шеечного канала при выполнении аблации эндометрия. Не является поводом для дискуссий, что никому из хирургов (независимо от их квалификации) не удалось избежать интра- или постоперационных осложнений различной степени тяжести. По-видимому, отсутствие хирургических осложнений в деятельности практикующего врача свидетельствует либо о незначительном опыте специалиста, либо об отсутствии такового в целом. В настоящее время проблеме хирургических осложнений отводится пристальное внимание, учитывая, что только глубокий анализ собственных осложнений, а также осложнений коллег-специалистов позволяет разработать эффективные превентивные действия. Хирург, скрывающий свои осложнения, лишает своих коллег, особенно начинающих, возможности предотвратить подобные осложнения. А.Н. Стрижаков, А.И. Давыдов medbe.ru