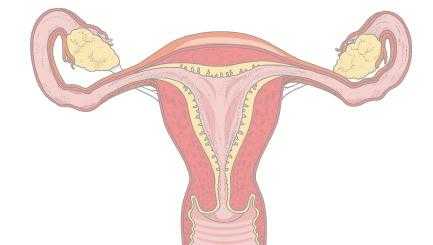
Синдром склерокистозных яичников
Синдром склерокистозных яичников
Первый наиболее часто отмечаемый «комплекс» нарушений при синдроме ПКЯ — это ановуляция, нарушения менструального цикла (олигоаменорея), первичное бесплодие, гиперпластические процессы эндометрия.
Часто назначаемым лечением при этой клинической ситуации (препараты первой линии), — это применение эстроген-гестагенных стероидных контрацептивов комбинированного типа по контрацептивной схеме. Здесь нет необходимости перечислять все препараты, которые можно рекомендовать для лечения. Современный аптечный рынок предлагает их в значительном количестве.
Основой лечебного эффекта, к которому стремятся при синдроме ПКЯ, является понижение гонадотропной активности и стероидогенеза в яичниках (снижение синтеза не только андрогенов, но и эстрогенов). Создаваемый искусственный менструальный цикл в условиях сниженной секреции ЛГ и ФСГ и подавленного фолликулогенеза обеспечивает снижение эстрогенного влияния на ткани-мишени, что приводит к атрофии эндометрия и даже уменьшению размеров кистозно-измененных яичников.
Достижение правильного ритма искусственного менструального цикла, устранение гиперпластических процессов эндометрия и снижение выраженности гирсутизма (о чем речь ниже), особенно при применении препаратов, обладающих антиандрогенным эффектом (Фемоден, Диане-35), — вот основной итог терапии стероидными контрацептивами синдрома ПКЯ.
Лечение может проводиться в циклическом режиме, по контрацептивной схеме, на протяжении 8–12 менструальных циклов, или в прерывистом режиме, с отменой лечения после каждых 2–3 циклов с расчетом на получении ребаунд-эффекта (усиление секреции гонадотропинов после снятия «гормонального тормоза»), способного вызвать овуляцию и запланированную беременность.
Важно учесть, что при применении стероидных контрацептивов у больных ПКЯ может быть получена и побочная реакция, а именно развитие стойкой аменореи после достаточно продолжительного лечения. В этих случаях следует возобновить гормонотерапию, но с использованием последовательной комбинации эстрогена (эстрадиола валерат) и прогестина (Климонорм, Климен, Цикло-Прогинова), назначаемых в циклическом режиме, для устранения возникшей аменореи и формирования правильного цикла (4–6 циклов).
Несомненно, получение соединений, могущих избирательно стимулировать овуляцию, является одним из выдающихся открытий ХХ века. В этом отношении существенный вклад в лекарственную терапию ановуляции и восстановление фертильности при синдроме ПКЯ внесло применение Кломифена.
Кломифен (клостильбегит, кломид, перготайм, серосфен — аналоги хлортианизена, антиэстрогены, по химической структуре сходные с синтетическим эстрогеном нестероидной природы — диэтилстильбэстролом, но не обладающие эстрогенным эффектом на органы-мишени, а даже, наоборот, являются по своему действию антиэстрогенами) — «препарат выбора» для лечения ановуляции и может применяться в качестве препарата второй линии для лечения бесплодия.
Влияние кломифена на сдвиги в репродуктивной системе пациентки вполне «патогенетическое». Препарат блокирует в гипоталамусе и аденогипофизе рецепторы эстрадиола, что вызывает устранение эстрогенного влияния на эти структуры. В результате такого действия происходит усиление секреции ГН-РГ и выброс аденгипофизом ФСГ и ЛГ, достигающих своего пика секреции, к моменту отмены кломифена. Увеличение уровня ФСГ в крови стимулирует созревание фолликулов в яичниках и усиление синтеза эстрадиола в гранулезных клетках.
Возрастание уровня эстрадиола в крови к середине менструального цикла инициирует по механизму положительной обратной связи овуляторный выброс ЛГ. Происходит разрыв фолликула и наступает овуляция, с последующими изменениями в женской репродуктивной системе, свойственными нормальному овуляторному циклу: восстановление овуляции нормализация ритма менструального цикла, восстановление фертильности и устранение гиперпластических процессов в органах-мишенях.
Читайте также: Насморк у грудного ребенкаКломифена цитрат (Клостильбегит) назначается в дозе 100–150 мг в день, с 2–3-го дня цикла, в течение 5 дней. Обычно рекомендуется проведение не более 6 циклов лечения, начиная с дозы 100 мг, с постепенным увеличением ее, в случае отсутствия эффекта, до 150 мг в сутки.
Критерии эффективности лечения: восстановление правильного ритма менструального цикла (средняя частота 80–85%) и двухфазной базальной температуры (длительность повышения базальной температуры во вторую фазу не менее 14 дней), уровень прогестерона в крови, свойственный полноценной лютеиновой фазе (6,7–56,8 нмоль/л), снижение содержания эстрона и повышение уровня эстрадиола.
Повышенный уровень эстрадиола, действуя на гипоталамо-гипофизарный комплекс по механизму положительной обратной связи, обусловливает овуляторный выброс ЛГ и ФСГ, в среднем через 7 дней с момента приема последней таблетки кломифена.
Овуляция и образование желтого тела, секретирующего прогестерон, сопровождается снижением уровня тестостерона и андростендиона.
По обобщенным данным, приводимым Т. А. Назаренко (2008) в своей монографии, клиническая эффективность кломифена цитрата, оцениваемая по частоте наступления овуляции и беременности весьма разнится. Так, если овуляция отмечалась на фоне лечения у 70–80% пациенток, то беременность наступала лишь у 20–30%. Автор определила и клинические критерии, по которым можно прогнозировать положительную реакцию на прием кломифена цитрата или резистентность к нему.
Чувствительность пациентки к стимуляции кломифена цитратом можно предположить, если:
– возраст до 30 лет;
– длительность нарушения менструального цикла не более 5 лет, а бесплодия не более 2 лет;
– нарушение менструального цикла по типу олигоаменореи или нормогонадотропной аменореи;
– достаточная эстрогенная насыщенность (проба с прогестероном положительная);
– уровень гормонов: ЛГ до 15 МЕ/л, ФСГ до 5–7 МЕ/л, тестостерон на верхней границе нормы, пролактин — норма.
Резистентность пациентки к лечению кломифена цитратом можно прогнозировать, если:
– возраст пациентки старше 30 лет;
– индекс массы тела более 25;
– определяется увеличенный объем яичников (более 10 см3);
– уровень ЛГ более 15 МЕ/л;
– уровень эстрадиола менее 150 пмоль/л.
При изолированном применении кломифена цитрата по указанной выше схеме мы не видели проявлений гиперстимуляции яичников, проявляющейся образованием двусторонних кист. Однако такую вероятность развития событий следует иметь в виду.
Поэтому важен эхографический мониторинг состояния яичников при проведении лечения (оценка динамики роста фолликула, его размеры).
При отсутствии эффекта от гормональной терапии синдрома (не более 4–6 циклов) показана лапароскопическая клиновидная резекция яичников.
Клиновидная резекция яичников, доказавшая свою эффективность в лечении больных ПКЯ, должна являться воздействием «второй линии» и выполняться по определенным показаниям.
К ним относятся:
1) неэффективность лекарственной (гормональной) терапии синдрома, проводимой на первом этапе;
2) первоначально выраженный гирсутный синдром.
Клиновидная резекция яичников, выполняемая с 1906 года у больных синдромом ПКЯ, является эффективным методом хирургической коррекции ановуляции и уменьшения массы стероидпродуцирующей ткани яичников. Правда, результаты лечения после выполнения клиновидной резекции, согласно данным литературы, варьируют. После операции регулярные менструации восстанавливаются в среднем примерно у 80% больных, беременность наступает у 63%.
Читайте также: Возрастные изменения в сердечно-сосудистой системеНаиболее выражен клинический эффект клиновидной резекции яичников в устранении гирсутных проявлений, если они были обусловлены гиперандрогенией яичникового генеза.
К сожалению, положительный эффект операции в отношении сохранения овуляторных циклов непродолжителен и ограничивается двумя-тремя годами. Наибольшая частота восстановления репродуктивной функции наблюдается в течение первых 6–8 месяцев после выполнения операции. В последующем тактика ведения пациенток определяется рядом факторов: в случае восстановления правильного менструального цикла в течение 6 месяцев лечения не назначают, при отсутствии беременности, с 4-го месяца после операции начинают прием гестагенов (утрожестан, дуфастон) с 16-го дня цикла по 26-й день, в течение 6–8 циклов. По данным, приводимым в специальной литературе, повторная стимуляция Кломифена цитратом, если первая не удалась по своему конечному результату, неэффективна. Поэтому если возникают показания к повторной стимуляции (сохраняющаяся вторичная аменорея, не наступившая беременность), ее проводят по схемам с использованием аналогов Гн-Рг и менотропинов.
Второй «комплекс» нарушений, выявляемый со значительной частотой при синдроме ПКЯ, связан с гиперандрогенией и гирсутизмом (70%) и ожирением (40%).
В основе развития гирсутизма у женщины (независимо от источника андрогенов) обычно лежат два механизма:
1) повышение уровня андрогенов в крови и (или)
2) повышение активности 5a-редуктазы, превращающей местно в волосяном фолликуле тестостерон в дигидротестостерон (ДГТ), через который и реализуется собственно андрогенный эффект.
Здесь следует заметить, что развитие гирсутизма зависит не только от повышения содержания андрогенных гормонов в крови, но и от чувствительности волосяных фолликулов к этим соединениям. Так, при синдроме ПКЯ у 30–40% пациенток гирсутизма не наблюдают, несмотря на повышенный уровень андрогенов в крови, что может объясняться слабой чувствительностью придатков кожи к андрогенному влиянию из-за низкого содержания в ткани ферментов-редуктаз. И наоборот, у пациенток с идиопатическим гирсутизмом, у которых нет данных, свидетельствующих о синдроме ПКЯ, уровень андрогенов может быть нормальным или незначительно повышенным, но определяется высокая активность тканевых редуктаз (например, 3α- и 3β-кеторедуктазы), образующих 3α- и 3β-андростендиолы из ДГТ, которые отражают интенсивность гормонального эффекта андрогенов на волосяные фолликулы. Таким образом, содержание 3α-андростендиола в плазме может отражать интенсивность утилизации андрогенов волосяным фолликулом кожи, независимо от величины содержания андрогенов в кровотоке.
Возвращаясь к проблеме гирсутизма при синдроме ПКЯ, следует учитывать эти два механизма реализации андрогенного эффекта и соответственно им планировать адекватное лечение. Во всяком случае у пациентки с синдромом ПКЯ и гирсутными проявлениями всегда следует иметь в виду повышенную тканевую активность указанных редуктаз и усиленную утилизацию андрогенов кожей, в сравнении с больной, у которой ПКЯ не проявляются гирсутизмом.
Читайте также: Сонный паралич - признаки и симптомыТактика лечения гирсутизма у пациенток с ПКЯ предполагает решение двух задач:
1) снижение продукции андрогенов яичниками и (или) надпочечниками;
2) блокада андрогеновых рецепторов кожи, чтобы предотвратить рост волос.
Лечение проводится длительно, от 6 месяцев до 1 года, для достижения положительных результатов.
Препаратами «первой линии» в лечении гирсутизма при синдроме ПКЯ являются уже указанные выше стероидные контрацептивы комбинированного (эстроген-гестагенного) типа. Снижая уровни ЛГ и ФСГ, они уменьшают продукцию андрогенов яичниками и увеличивают продукцию глобулина, связывающего половые гормоны, снижая таким образом, уровень свободного тестостерона. Специальное внимание при этом следует обратить на препараты с выраженным местным антиандрогенным эффектом (Фемоден, Диане-35). Усиливает антиандрогенный эффект стероидных контрацептивов присоединение к ним антиандрогена Андрокура (ципротерона ацетат), назначаемого по 10 мг в день, с 1-го по 15-й день приема основного препарата.
При получении данных обследования, указывающих на надпочечниковый «компонент» гирсутных проявлений (несколько повышенные уровни свободного и общего тестостерона в сочетании с повышением ДГЭА-С и повышенной экскрецией 17- КС, положительные данные дексаметазонового теста) к лечению стероидными контрацептивами присоединяется дексаметазон из расчета 0,25 мг (1/2 таб.) в сутки, постоянно, без перерыва, в течение 6 месяцев. Дозу дексаметазона лучше подбирать индивидуально по мере лечения, ориентируясь на величины экскреции 17-КС (снижение до минимальных значений), снижение содержания ДЭА-С и кортизола в плазме крови, исследуемых на 5–7-й день в каждом цикле лечения. В случае нормализации показателей андрогенного статуса и отсутствия на фоне проводимого лечения полноценной овуляции возможно проведение стимуляции овуляции кломифеном в течение 4–6 циклов, в возрастающей дозировке 50–150 мг в сутки. Показано увеличение частоты наступления овуляции под влиянием кломифена при условии подавляющей функцию коры надпочечников терапии дексаметазоном.
Примерно 55–65% больных с синдромом ПКЯ страдают метаболическим синдромом: ожирением, которое развивается в раннем пубертатном периоде до появления менархе. В последующие годы ожирение приобретает черты диэнцефального нарушения, для которого свойственны гиперинсулинемия, сниженная толерантность к углеводам, гиперлипидемия, увеличение содержания в крови инсулиноподобных факторов роста, малая эффективность лечения низкокалорийной диетой.
Совокупность этих влияний в условиях хронической гиперэстрогении инициирует интенсивную клеточную пролиферацию в тканях-мишенях, что может повышать риск развития гиперпластических изменений в репродуктивной системе. Образующийся порочный круг разрывается одновременным назначением препаратов, нормализующих репродуктивный цикл и проведением комплекса мер, направленных на нормализацию метаболических показателей: преодоление резистентности к инсулину, низкокалорийная диета, препараты тироксина и антиоксиданты (альфа-токоферол).
По материалам: health-medicine.info
Загрузка ...Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
health-medicine.info
Синдром склерокистозных яичников
Среди своеобразных видов патологии организма женщины, которая часто выявляется в пубертатном периоде, большое внимание клиницистов в течение многих лет продолжает привлекать проблема склерокистозного изменения яичников, известного под названием – синдром Штейна – Левенталя.
После сообщения Я. К. Хачкурузова (1915), а позднее В. К. Лесного (1928) и Е. Е. Гиговского (1930) о своеобразной клинической картине нарушения менструальных циклов при двустороннем увеличении яичников на почве склерокистозных изменений их детальное описание этого синдрома Stein и Lowenthal (1935) способствовало появлению значительного количества литературных материалов, посвященных этому вопросу. В частности, из множества работ последних лет следует выделить монографию П. Г. Шу-шания, коллективный труд под редакцией А. С. Слепых, докторские диссертации Н. И. Бескровной, Д. А. Пальчик, обзор Е. М. Вихляевой (1973) и др.
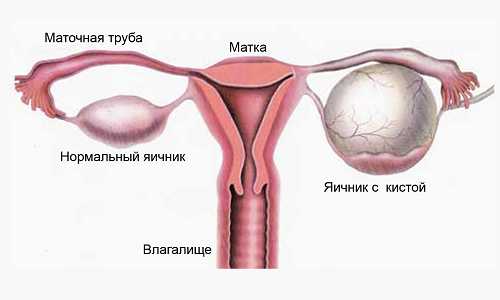
Основными признаками склерокистозных изменений яичников являются довольно равномерное двустороннее увеличение их и наличие плотной сероватой или перламутрово-белой оболочки (так называемые большие серые яичники), сквозь которую просвечивают множественные мелкие фолликулярные кисточки со светлым содержимым. В корковом слое яичников число примордиальных и зрелых фолликулов заметно уменьшено. Соединительнотканная строма внутренней оболочки фолликулов гиперплазирована, поверхностные слои ее и стенки сосудов фиброзированы. На газовой гинекограмме четко видны контуры обоих увеличенных яичников. Количество кислых и нейтральных мукополисахаридов повышено.
Как подчеркивает Б. И. Железов, при гистологическом исследовании макроскопически заметно измененных яичников иногда делаются ошибочные заключения о наличии склерокистоза гонад в случаях гипертекоза или текоматоза; при последнем имеет место изменение отделов яичников, а именно Диффузная гиперплазия и лютеинизация стромы. На разрезе ткань подобных яичников имеет неравномерный или диффузный желтый цвет, обусловленный лютеинизированными клетками, которые располагаются в виде отдельных или множественных групп; кистозно-атрезирующиеся фолликулы встречаются в небольшом количестве или даже отсутствуют. Белочная оболочка не Утолщена или утолщена неравномерно. Гипертекоз, наблюдаемый не только в менопаузе, но и у женщин детородного возраста, Ряде случаев обнаруживался в сочетании с гиперплазией сетчатой зоны коры надпочечников. Изменения стромы яичников при гипертекозе сопровождаются нередко андрогенным эффектом, что клинически проявляется в виде симптомов вирилизма или гирсутизма. Подчас отмечается сочетание с раком тела матки (Я. В. Бохман) или молочной железы.
В многочисленных работах был подвергнут детальному анализу вопрос о яичниковом генезе склерокистозных изменений гонад, о состоянии гипоталамо-гипофизарных структур при этом заболевании и о роли надпочечиикового фактора при учете столь нередкого вирильного синдрома у больных этой категории.
Общепризнанным основным фактором заболевания признается нарушение процесса биосинтеза стероидных гормонов в яичниках. Если в физиологических условиях соотношение между эстрогенами и андрогенами яичников составляет 7:1, то у больных с синдромом склерокистозных яичников обнаруживаются серьезные ферментные нарушения, которые могут идти в двух направлениях.
У части больных имеет место извращенный путь обменных превращений стероидов; биосинтез их происходит преимущественно в клетках гипернлазировашюй внутренней оболочки с выделением значительных количеств до-гидроэпиандростерона, обладающего сильным андрогенным действием. При втором варианте вследствие нарушения биосинтеза гормонов не происходит превращения апдростендиола в эстрогены; он накапливается в избыточном количестве в фолликулярных «кисточках» вместе с 17-сс-оксипрогестероном и тестостероном–предшественниками эстрогенов, обладающими андрогенными свойствами.
Нарушения, обусловливающие дефект синтеза эстрогенов яичниками, имеют генетически обусловленный, врожденный характер. Высказано предположение, что этиологическим фактором в развитии синдрома склерокистозных яичников является повреждающее действие вирусных инфекций на хромосомный набор, в особенности в группах А, С и др. (Sterba, Sturma).
Возможны 4 этиологических типа синдрома склерокистозных яичников. К ним относятся: 1) первичные поражения на уровне гипоталамуса; 2) вторичные поражения на уровне гипоталамуса (при врожденном гипер-кортицизме); 3) задержка биосинтеза гормонов на уровне ароматизации; 4) задержка биосинтеза гормонов на уровне З-эпи-Р-ол-дегидрогеназы. Поэтому допустимо обозначение заболевания как синдром микрополикистозных яичников, который включает несколько клинических единиц.
Вследствие неодинаково выраженной степени блокады биосинтеза эстрогенов яичников клинически наблюдаются различные виды заболевания.
В части случаев оно обнаруживается вскоре после менархе, проявляясь в виде довольно стойких ановуляторных нарушений и бесплодия; только в дальнейшем развиваются вторичные гипоталамо-гипофизарные расстройства на почве нарушения физиологических соотношений между уровнем экзогенных и эндогенных воздействий на организм. В части случаев характерный симптомо-комплекс возникает под влиянием аффекта, например после психической травмы, иногда после начала половой жизни, после родов и абортов. Нередко у больных обнаруживаются и полигландулярные эндокринные расстройства с повышенной лабильностью нервной системы. Поэтому, возможно, известную роль в патогенезе заболевания играют первичные нарушения гипоталамо-гипофизарных отношений центрального происхождения, что обусловливает нарушение циклической секреции гонадотропин-рилизинг-факторов и гонадотропинов, а также нарушение биосинтеза стероидов яичников с появлением ановуляторных циклов.
В ряде случаев имеют место изменения функции коры надпочечников. Вырабатываемый в избытке в яичниках андростендион блокирует соответствующий фермент коры надпочечников; возникающая на основе этого дисфункция усиливает патологическое андрогенное влияние в организме женщины. Сказанное позволяет считать заболевание неоднородным по патогенезу, что и объясняет многообразие картины болезни и различные клинические варианты ее течения, поскольку возможно переплетение различных механизмов, ведущих к нарушениям функции яичников, гипоталамо-гипофизарных и адрепокортикальных структур.
К числу наиболее частых клинических симптомов заболевания относятся нарушения менструального цикла характера гипоменструального синдрома, ановуляторных циклов (заканчивающихся длительными кровотечениями), аменореи и гирсутизма.
Хотя патология месячных и необычное оволосение появляются у большинства больных в пубертатном возрасте, однако выраженные симптомы заболевания нередко выявляются позже – после 20 лет и главным образом у замужних женщин, поскольку бесплодие, одно из основных проявлений синдрома, обычно привлекает к себе внимание после нескольких лет брачной жизни.
Частота клинических признаков, сопровождающих склерокистоз яичников, примерно такова: нарушения менструальной функции составляют 95 %, гирсутизм – 87 %, бесплодие – 71 %, гипоплазия матки – 45%, ожирение – 36%, гипоплазия молочных желез – 32% (Н. И. Бескровная, 1971).
Несмотря на значительные изменения в яичниках, почти у 20% больных рано или поздно наступает беременность, которая чаще заканчивается самопроизвольным абортом или осложненными родами.
Один из наиболее постоянных признаков заболевания – гирсутизм – обычно появляется спустя некоторое время после начала нарушения менструальных циклов.
Патологическое оволосение происходит на лице, околососковых кружках, белой линии живота, вокруг пупка и на нижних конечностях. Однако в ряде случаев верхняя граница лобкового оволосения бывает горизонтальной, по женскому типу. Больные имеют вполне женский облик с характерным распределением жира в подкожной клетчатке и развитием мускулатуры по женскому типу.
Как подчеркивает Д. А. Пальчик на основании своих наблюдений, большинство клинических симптомов и морфологических изменений яичников, описанных при синдроме Штейна – Левенталя, не являются специфическими; в частности, гипоменорея, гирсутизм, бесплодие и двустороннее увеличение яичников наблюдаются и при постпубертатных формах адреногенитального синдрома, а в сочетании с вегетативно-сосудистыми нарушениями – при болезни Иценко – Кушинга, что отмечается также Н. И Бескровной. Д. А. Пальчик выделила 3 клинических варианта склеро-кистозных яичников, а именно: 1) типичную неосложненную форму с нарушением менструальных циклов; 2) осложненную форму, при которой нарушению менструальной функции сопутствуют вторично возникшие вегетативно-сосудистые расстройства, часто в сочетании с нарушениями жирового и углеводного обмена и эмоционально-психическими изменениями; 3) атипическую клиническую форму, при которой преобладали первично возникшие вегетативные расстройства, иногда за несколько лет до нарушения функции яичников.
Н. И. Бескровная также выделила на своем обширном материале 3 клинические формы синдрома: 1) наиболее частую типичную форму (73% от общего числа больных) с характерными нарушениями менструальных циклов; 2) редкую форму (3,8%), характеризующуюся метрорагиями; 3) смешанную форму (19,6%), при которой задержки регул чередовались с очередными обильными кровопотерями.
Считая наиболее правильным представление о ведущей роли функциональных нарушений в области гипоталамических центров, возникающих в период возрастного становления половой функции, Н. И. Бескровная приводит в пользу своего взгляда на синдром Штейна – Левенталя следующие факты:
- Клинические проявления синдрома в молодые годы, преимущественно в пубертатном возрасте;
- Монотонную экскрецию гоиадотропных гормонов с отсутствием ритмических колебаний в выделении ФСГ и ЛГ;
- Обратимый характер менструальных нарушений в ряде случаев при своевременном гормональном и главным образом при хирургическом лечении.
При объективном исследовании больных, помимо весьма частого (но далеко не обязательного) гирсутизма, обнаруживающегося вскоре после появления месячных или после начала нарушения менструальных циклов, большей частью пальпаторно удается установить двустороннее увеличение яичников (примерно в половине случаев). При отсутствии явного увеличения их или для уточнения диагноза прибегают к газовой гинекографии. Однако традиционное представление о том, что на пневмопельвеограммах величина яичников составляет примерно 3/4 тени матки, часто неверно, так как при наличии уменьшенных размеров последней создается неправильное представление об увеличении относительных размеров яичников.
Следует иметь в виду, что в редких случаях, как указывает Б. И. Железнов, склерокистозные яичники сочетаются с новообразованиями: дермоидная киста, арренобластома, с очаговой стромалыюй гиперплазией или хилюсно-клеточной гиперплазией яичников; тека-клеточная и гранулезо-клеточная опухоль и т. п.
Кольпоцитологическое исследование обнаружило, по данным Н. И, Бескровной, разнообразие данных; однако характерным было отсутствие двухфазности циклов.
В трети случаев пролиферативные или атрофические изменения влагалищного эпителия сочетались с отчетливыми проявлениями андрогенного воздействия. Эндометрий в 77% случаев обнаруживал гипопластические изменения и только в 5% случаев – атрофические. Почти у всех больных отсутствовали признаки секреторной трансформации эндометрия. В 92,7% случаев была установлена ановуляция.
По Б. И. Железнову, эндометрий в 20% случаев находится в состоянии гиперплазии. Н. И. Бескровной удалось установить на своем материале наличие достоверных корреляций между андрогенной активностью и степенью гирсутизма у больных.
Для выяснения источников гиперпродукции андрогенов (яичники или надпочечники) большую помощь может оказать фракционное исследование 17-КС, а также применение проб на стимуляцию и подавление функций надпочечников и яичников.
Автору в 6 случаях удалось установить наличие сочетания синдрома Штейна – Левенталя с гиперфункцией коры надпочечников. Если в физиологических условиях в женском организме вырабатывается не более 1 мг тестостерона (половина продукции которого приходится на яичники, а половина – на надпочечники), то в случае нарушения процесса биосинтеза эстрогенов продукция тестостерона в женском организме может увеличиться до 3–4 мг в сутки (в частности, за счет превращения андростен-диола в тестостерон и прегненолона в дегидроэпиандростерон, способный превращаться в тестостерон), что соответствует величинам, типичным для мужского организма.
Schneider и соавт., изучая экскрецию андрогенов при синдроме Штейна – Левенталя, установили, что уровень выделения эпи-тестостерона выше 10 мкг в сутки у большинства обследованных женщин, причем в результате стимуляции хориогонином у всех отмечалось значительное нарастание экскреции этого андрогена (на 400 и более процентов).
Поскольку после резекции яичников (а в нескольких случаях после их полного удаления) наступало резкое снижение выделения тестостерона и эпитестостерона, следует считать, что определение содержания эпитестостерона в моче до и после стимуляции хорионическим гонадотропином является хорошим тестом для определения функции яичников при ановуляторных циклах.
Согласно исследованиям Д. А. Пальчик, изучение экскреции 17-КС показало нормальные цифры у 29 больных, умеренно повышенные (11 – 19 мг в сутки) – у 35 и значительное повышение (свыше 20 мг в сутки) – у 10. В основном наблюдалось увеличение наиболее активных фракций 17-КС: дегидроэпиандростерона и андростерона.
Синдром Штейна–Левенталя следует дифференцировать с андрогенпродуцирующими опухолями яичников, заболеваниями коры надпочечников, диэнцефальным синдромом, конституциональным гирсутизмом и некоторыми другими состояниями. Для этого, помимо тщательного опроса больных, внимательного осмотра с выявлением особенностей телосложения, распределения подкожного жира и волосяного покрова на теле, характера и выраженности вторичных половых признаков, необходимо применение специальных методов функциональной диагностики, пневмопельвеографии, определение экскреции прегнандиола с мочой, 17-КС и 17-ОКС, применение проб на подавление функции надпочечников, а также в ряде случаев пробная терапия кортикостероидами, половыми или гонадотропными гормонами.
Установленные Д. А. Пальчик изменения характера экскреции 17-КС и их фракций в условиях стимуляции яичников хориогонином (по 1500 ед. внутримышечно в течение 4 дней) позволяют выделить 3 формы склерокистозных яичников: типичную, осложненную и атипичную.
При повышенном содержании апдростенолона в моче введение хорио-гонина не вызывает изменений прегнантриола и 17-КС, по снижает количество андростеполона и повышает уровень экскреции эстрадиола с мочой, что свидетельствует о нарушении ферментной системы в яичниках. При низком исходном содержании андростеполона в моче введение хорионического гонадотропина ведет к увеличению экскреции прегнантриола, 17-КС и андростеполона при неизмененном содержании эстрадиола (это свидетельствует о наличии энзимного блока в системе 19-гидроксилазных ферментов).
При гирсутизме яичникового происхождения вспомогательное значение имеет прогестероновый тест, ведущий к снижению выделения 17-КС, а также в меньшей мере к выделению с мочой 17-оксикортикостероидов.
Вышеуказанные пробы помогают уточнить патогенез заболевания и облегчают выделение так называемых смешанных форм, когда имеется сочетание поражения яичников и коры надпочечников. В неясных случаях желательно, как уже упоминалось, применение супраренографии для определения размеров надпочечников.
До последнего времени отсутствовала единая классификация, охватывающая все формы нарушения полового развития девочек, проявляющиеся разнообразными симптомами в периоде полового созревания и половозрелости. С этой точки зрения заслуживает внимания разработанная В. И. Бодяжиной, Л. Г. Тумилович, М. Н. Кузнецовой, Е. А. Богдановой общая классификация нарушений полового развития, в которой учитываются их патогенез и клинические проявления.
ginekolog.my1.ru
Синдром склерокистозных яичников (Штейна-Левенталя)
04 Мая в 12:19 1786
Актуальность проблемы склерокистозных яичников определяется увеличением числа больных за счет повышения точности диагностики, сложностью патогенеза заболевания, трудностями распознавания клинически не выраженных форм синдрома, сравнительно частыми рецидивами. Кроме того, у значительного числа больных с синдромом склерокистозных яичников выявляются гиперпластические процессы эндометрия. Возможность развития у больных с синдромом склерокистозных яичников атипической гиперплазии и рака эндометрия определяет онкологический аспект этой проблемы. По современным представлениям, в патогенезе синдрома склерокистозных яичников существенное значение имеют следующие факторы: 1) первичный (возможно генетически обусловленный) дефект энзимных систем в яичниках, приводящий к ингибиции синтеза эстрогенов и накоплению предшественников с андрогенной активностью; 2) снижение эстрогенного влияния на гипоталамический тонический центр регуляции выделения гипофизом гонадотропинов (по механизму положительной обратной связи), что приводит к постоянному, а не циклическому выделению гонадотропинов. Это препятствует их накоплению в гипофизе и устраняет возможность овуляторного выброса ФСГ и ЛГ, создавая тем самым хроническое состояние ановуляции; 3) длительная постоянная стимуляция половых желез гонадотропинами, приводящая к функциональным сдвигам (накопление предшественников андрогенов, синтез качественно измененных эстрогенов) и морфологическим изменениям (гиперплазия текаткани, развитие фолликулярных кист) в яичниках; 4) диэнцефальные нарушения и обусловленный этим избыток жировой ткани у части больных, способствующие повышенной ароматизации андростендиона в эстрон и увеличению таким путем «эстрогенного пула» в организме; закономерным результатом этих сдвигов является повышенная эстрогенная стимуляция эндометрия. Сложный патогенез заболевания определяет многообразие его клинических проявлений, что, как справедливо отмечает Е.М. Вихляева (1981), требует выделения основных клинических форм синдрома склерокистозных яичников в пределах одной нозологической единицы с тем, чтобы выбрать оптимальный метод лечения.Для уточнения онкологических аспектов синдрома Штейна—Левенталя было исследовано состояние эндометрия в двух группах больных. Первую группу составили 105 больных (средний возраст 24 года), оперированных в гинекологическом отделении Псковской областной больницы. Хотя преимущественной формой нарушения цикла у этих больных была опсоменорея или аменорея, нормальное состояние эндометрия или атрофия отмечены всего в 23%; в 74 % - железистая (ЖГЭ), а в 3% — атипическая гиперплазия эндометрия (АГЭ).
Вторая группа представлена 80 больными, у которых синдром Штейна—Левенталя был выявлен в НИИ онкологии им. проф. Н.Н. Петрова. Эти больные имели значительно большую длительность заболевания (средний возраст 29 лет), причем первоначальная аменорея сменилась у них ациклическими маточными кровотечениями. ЖГЭ была выявлена в этой группе в 64%, АГЭ - в 10%,аРЭ- в 15% случаев. Сочетание синдрома Штейна—Левенталя с высокодифференцированным РТМ: а — вид больной. Гирсутизм; б — высокодифференцированная аденокарцинома эндометрия. х 150 Высокая частота атипической гиперплазии и РЭ в значительной мере обусловлена фактором специального отбора больных в онкологической стационар. Тем не менее принципиальная возможность развития РЭ у больных с длительно существующим нелеченым синдромом Штейна-Левенталя не вызывает сомнений. Поэтому представляется правильным всех больных с синдромом склерокистозных яичников вне зависимости от вариантов его течения относить к группе риска заболевания предраком и РЭ. При сочетании нескольких факторов риска (ожирение, гиперлипидемия, сахарный диабет) опасность развития РЭ возрастает. Существенное значение при этом имеет фактор времени, в течение которого указанные нарушения сохраняются некомпенсированными. Поэтому развитие атипической гиперплазии и РЭ у некоторых больных в репродуктивном периоде можно рассматривать как позднее осложнение длительно существующего, нелеченого синдрома склерокистозных яичников. В связи с зтим нарушения менструального цикла, бесплодие и гирсутизм не являются единственными показаниями для лечения синдрома склерокистозных яичников. С онкологической точки зрения, не меньшее значение имеет нормализация состояния яичников и эндометрия. Необходимо исследовать состояние эндометрия до лечения при синдроме склерокистозных яичников, а также в ближайшие и в отдаленные сроки после его завершения (клиновидная резекция яичников, стимуляция овуляции). Я.В. Бохман-
Гормонозависимые опухоли
И.В. Бохман (1972) отметил, что частота первично множественных опухолей среди 340 больных РЭ составила 12%. В описанных 42 таких наблюдениях преобладали опухоли яичников, молочной железы и толстой кишки. Приводятся детальные описания синхронного и метахронного развития трех, четырех и се...
Онкогинекология -
Механизмы противоопухолевого иммунитета
Иммунная система организма представляет собой совокупность всех лимфоидных органов и клеток, среди которых выделяют четыре основных типа иммунокомпетентных клеток: Т- и В-лимфоциты, NK-клетки (естественные киллеры) и макрофаги. В процессе дифференцировки полипотентные стволовые клетки в кост...
Онкогинекология -
Аспирация кист
Как изолированный способ лечения в настоящее время практически не применяется. Однако возможно при наличии больших (более 10 см) образований яичника. Аспирация поводится пункционной иглой, введенной через дополнительный троакар.
Онкогинекология
medbe.ru
Сидром склерокистозных яичников
Одно из не очень распространенных, но опасных гинекологических заболеваний – это склерокистоз яичников. Это патология яичников возникает в результате образования на их поверхности небольших кист. Как правило, размер кист не достигает больше 1 см. Не смотря на это, яичники увеличиваются в размерах и начинают приносить боли и дискомфорт всему организму. Другое название данного заболевания – это синдром Штейн-Левенталя.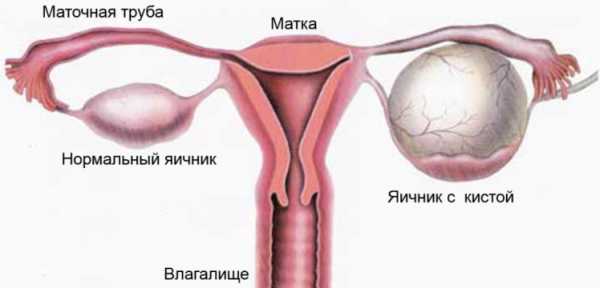
Встречается склерокистоз яичников довольно-таки редко. Всего лишь в 5% от всех гинекологических заболеваний. Но, данная патология опасна тем, что женщина может остаться полностью бесплодной, если вовремя не начать лечение.
Виды
Как и любое заболевание, синдром склерокистозных яичников имеет несколько видов. Врачи разделяют два вида патологии:
- наследственная патология;
- приобретенная патология.
Наследственный склерокистоз яичников, как можно догадаться, передается женщине от матери или бабушки. Даже если у матери не было данного заболевания, а в роду оно присутствовало, это не значит, что ребенок не может унаследовать его.
Приобретенный склерокистоз появляется у девушек во время полового созревания, а также у женщин репродуктивного возраста, которые никогда не беременели и не рожали.
Причины
Сегодня врачи не пришли к общему выводу о том, почему у женщин возникает склерокистоз яичников. Считается, что главную роль в возникновении этого заболевания играют половые гормоны, а точнее нарушение их синтеза и выделения.
Немаловажно учитывать тот факт, что нарушение работы эндокринных органов женщины также может способствовать возникновению этого заболевания.
Другие врачи упорно настаивают на том, что склерокистоз возникает по причине чрезмерного выделения гормона, который стимулирует фолликул (ФСГ). В результате этого нарушения яичник не может нормально работать. В нем начинают формироваться незрелые кисты, которые покрываются плотной оболочкой.
Нарушение синтеза лютеинизирующего гормона также может стать причиной возникновения данного заболевания.
Если верить другим теориям, причинами склерокистоза являются такие факторы:
- высокая активность коры надпочечников;
- дефицит эстрогенов;
- нарушения в формировании стероидных гормонов.
Именно эти факторы способствуют нарушению созревания фолликул. В организме женщины повышается количество мужских половых гормонов. В результате этого возникает бесплодие.
Симптомы
Каждая девушка должна следить за своим «женским» здоровьем. Очень важно регулярно обследоваться у гинеколога. Это помогает выявить любое заболевание на ранней стадии и быстро, а главное легко избавиться от него.
Но, одного посещения гинеколога недостаточно. Важно знать основные симптомы различных заболеваний для того, чтобы «по первому звоночку» записаться на приём к врачу и развеять все опасения.
Итак, к основным симптомам склерокистоза яичников относятся:
- нарушение менструального цикла;
- резкое похудение или резкий набор лишнего веса;
- бесплодие;
- яичники резко увеличиваются в размерах (с двух сторон);
- появление повышенной волосатости тела;
- гипоплазия женских половых органов, груди.
Некоторые симптомы каждая женщина сможет определить самостоятельно. К примеру, если вы придерживались своего нормального ритма жизни, но при этом резко набрали несколько лишних килограммов, стоит задуматься над тем, нет ли у вас каких-либо проблем.
Еще одни симптомы – это постоянные головные воли, общая усталость без причины и вялость. Снижение сексуальности и сексуального желания, частая бессонница могут подсказать о наличии данного заболевания.
Отсутствие «критических дней» также считается симптомом склерокистоза яичников. Менструация может стать слишком обильной или, наоборот, скудной. Если вы заметили какие-либо отклонения от своего привычного менструального цикла – срочно обращайтесь к своему гинекологу.
Чаще всего пациентки обращаются к врачу, когда замечают у себя несколько симптомов, которые перечислены выше. Длительные и безрезультатные попытки зачать ребенка – это еще одна причина обращения к гинекологу, которая напрямую связана с данным заболеванием.
Первое обследование, которое должен привести врач – это стандартный осмотр на гинекологическом кресле. Как правило, специалист прощупывает размеры матки и оба яичника для того, чтобы определить, если ли какие-либо посторонние тела на поверхности.
Врач также должен определить наличие или отсутствие овуляции. Это можно сделать с помощью функциональных тестов, которые измеряют базальную температуру. Специалист делает соскоб эндометрия и кольпоцитограмму.
Самое главное обследование – это ультразвуковая диагностика или просто УЗИ. Только на нем можно увидеть уплотнения на яичниках, а также кисты.
Для постановки диагноза предусмотрено также газовая пельвеограмма. С ее помощью можно увидеть:
- уменьшение матки;
- увеличение яичников и изменение их формы.
Лечение
После постановки диагноза врач обязан назначить лечение склерокистоза яичников. В зависимости от степени запущенности склерокистоза, гинеколог назначает:
- консервативный метод лечения;
- оперативный метод лечения.
Консервативный метод лечение предполагает лечение с помощью специальных гормональных препаратов. Чаще всего назначают:
- Для стимуляции овуляции назначают прием кломифена (назначается с 5-х суток начала «критических дней» и принимается в течение 5-ти дней).
- Для того чтобы повысить лютеинизирующий гормон назначают терапию с помощью циклофенилом.
- Для избавления от чрезмерной растительностb на теле назначают овосистон. Он регулирует обмен стероидов.
- Если у пациентки наблюдаются проблемы с надпочечниками, то врачи назначают преднизолон.
- Для вызова менструаций чаще всего назначают бисекурин.
Очень часто врачи не могут обойтись без оперативного вмешательства. Это надежный способ избавления от данной проблемы. Лапароскопия позволяет проводить операции без разрезов, что очень радует всех пациенток.
Некоторые девушки прибегают к народным методам лечения. Конечно же, не стоит к этому относиться слишком серьезно. Различные травы и отвары не принесут никого вреда организму, а возможно поспособствуют скорейшему выздоровлению. Можно использовать следующие травы:
- калину;
- трава лабазника;
- цветок под названием «пион», а точнее его настой;
- чистотел;
- лопух (а точнее его сок).
Свежий сок калины следует смешать с цветочным медом. На протяжении 4-х месяцев принимайте этот напиток. Дозы нужно увеличивать постепенно.
Траву лабазника необходимо смешать с листьями малины и залить кипятком. Выпивать такой отвар нужно в течение 24 часов, иначе он испортится. Принимать такое народное лекарство нужно 3 месяца.
Настой из пиона разбавить с обычной водой. Принимать 3 раза в день. Обратите внимание на то, что пить такой настой нужно строго по часам, то есть в одно и тоже время.
Чистотел нужно принимать очень аккуратно. Передозировка этим целебным растением может обернуться очень плачевно. Обязательно перед лечением нужно проверить, переносит ли ваш организм чистотел. Приготовить отвар очень просто. Достаточно взять стебло молодого чистотела, помыть его и нарезать небольшими кусочками. Дальше его необходимо закинуть в кипящую воду и прокипятить в течение одной минуты. Перед употреблением обязательно дайте отвару настояться. На это уйдет не больше 20-ти минут. Принимать его необходимо ежедневно за полчаса до приема пищи по 50 мл.
Сок лопуха также помогает бороться с данным заболеванием. Добыть его очень просто. Достаточно пропустить через мясорубку молодые листья лопуха, и из полученной массы выжать сок. Принимать нужно ровно месяц приблизительно по одной столовой ложке до еды. Если вы посчитаете, что курс лечения нужно продолжить, то сделайте перерыв в 14 дней, и снова продолжите прием этого сока.
В любом случае, нельзя ограничиваться лишь народными методами лечения. Обязательно необходимо принимать препараты, которые назначил врач. Не забудьте перед этим проконсультироваться с ним о том, можно ли вам принимать различные травы вместе лекарствами. Возможно, некоторые препараты и травы не совместимы друг с другом и могут привести только вред. В обязательном порядке нужно ставить в известность обо всех своих действиях. Только так лечение будет эффективным.
Беременность
Все знают, что склерокистоз яичников и беременность – это практически несовместимые вещи. Всё потому, что у женщины отсутствует овуляция, соответственно девушки не может забеременеть. Поэтому, многие девушки задают себе вопрос можно ли забеременеть при склерокистозе яичников.
Врачи в один голос заявляют, что во время протекания болезни забеременеть невозможно, так как яйцеклетка не может «попасть» в маточную трубу и оплодотвориться. Но, у каждой женщины есть шанс забеременеть после полного выздоровления. Поэтому, не нужно терять надежду и бросать лечение. У вас всегда есть шанс родить здорового ребенка, даже после склерокистоза яичников.
Похожие записи
gormonoff.com