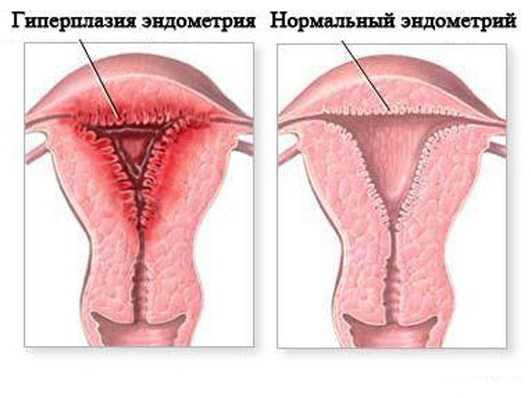
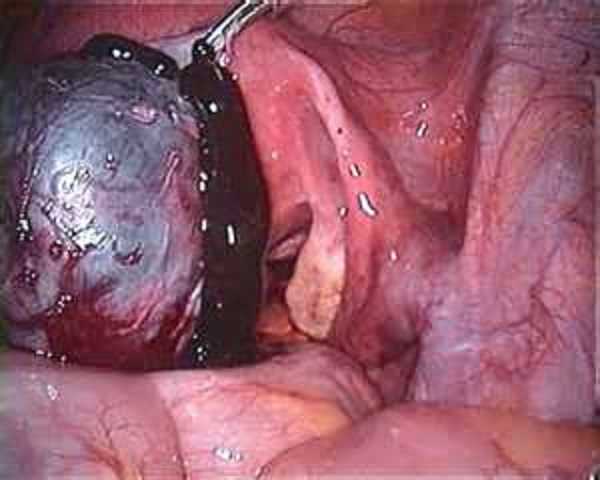
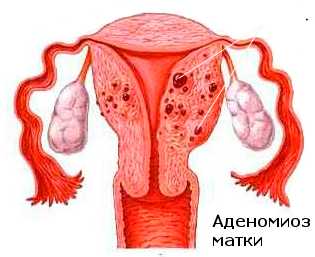
Эндометриоз патологическая анатомия
Патогенез
ЭНДОМЕТРИОЗ - одна из важнейших проблем гинекологии, т.к. это заболевание вызывает бесплодие и тазовые боли у миллионов женщин во всем мире. Причины возникновения и развития эндометриоза остаются предметом споров с того момента, когда он был выявлен впервые.
Согласно данным последних лет. эндометриоз относится к числу наиболее распространенных гинекологических заболеваний у женщин репродуктивного возраста и обнаруживается, по данным разных авторов в 1 - 50 % случаев во всей популяции, в том числе у 20 % женщин, страдающих бесплодием. Первые научные сообщения, посвященные эндометриозу, относятся к 1896 - 1907 гг. Однако за столетний период проблема не только не утратила своей актуальности, но до настоящего времени является наиболее дискутабельной.
Это обусловлено рядом причин, среди которых необходимо выделить:
увеличение частоты эндометриоза в гинекологической заболеваемости за последнее десятилетие;
сложность его диагностики на начальных этапах развития, отсутствие чет кой концепции в системе обследования и лечения больных эндометриозом.
Эндометриоз - патологический процесс, формирующийся на фоне нару-шенного гормонального, иммунного и биохимического гомеостаза организма и характеризующийся ростом и развитием ткани, идентичной по структуре и функции эндометрию, за пределами границ нормальной локализации слизистой оболочки тела матки.
В структуре гинекологической заболеваемости эндометриозу отводится третье место после воспалительных процессов и миомы матки. Установление действительной частоты эндометриоза в обшей популяции представляет определенные трудности, обусловленные, в первую очередь, неоднозначным подходом исследователей к диагнозу «эндометриоз». Так, можно выделить 4 основных направления в диагностике эндометриоза:
констатация как косвенных, так и прямых клинических признаков;
регистрация ультразвуковых и/или рентгенологических критериев забо левания;
визуальная диагностика очагов эндометриоза в ходе лапароскопии или лапа- ротомии;
морфологическое изучение биопсийного материала, полученного в ходе ла пароскопии или лапаротомии.
Гистологическое строение эндометриоза во многом напоминает строение эндометрия (сочетание железистого эндометриоподобного эпителия и цитогенной стромы), однако, в отличие от неизмененной слизистой тела матки, эндометриоидная ткань менее подвержена циклическим превращениям - в частности, под влиянием прогестерона в очагах не происходит полноценной секреторной трансформации и, в целом, эндометриоидные гетеротопии достаточно слабо реагируют на воздействие экзогенных гормонов. Необходимо подчеркнуть, что соотношение железистого эпителия и цитогенной стромы в очагах эндометриоза различной локализации неодинаково. Так, достоверно установлено, что в гетеротопиях, развивающихся в миометрии (внутренний эндометриоз тела матки) преобладает стромалъный компонент. Вместе с тем, какой-либо определенной закономерности, касающейся соотношения стромального и железистого компонентов в очагах наружного генитального эндометриоза, не обнаружено.
Макроскопически эндометриоз может иметь форму узлов, инфильтратов или кистозных образований, полость которых заполнена геморрагическим содержимым. Узлы эндометриоза формируются в результате проникновения в ткани, окружающих фокусы эндометриоза, менструальноподобных кровянистых выделений, протеолитических и липолитических ферментов, выделяемых патологическими имплантатами, а также продуктов деструкции тканей, образующихся в зоне эндометриоза.
Подобное развитие эндометриоидных узлов определяет особенность их строения, а именно, отсутствие в них окружающей соединительнотканной капсулы. Это имеет немаловажное клиническое значение, т. к. указанная особенность строения эндометриоза учитывается не только при проведении дифференциальной диагностики его с другими патологическими состояниями гениталий, но и хирургическом лечении больных эндометриозом .
Классификация
В настоящее время принято выделять генитальный (локализация патологического процесса во внутренних и наружных половых органах) и экстра-генитальный эндометриоз (развитие эндометриоидных имплантатов в др. органах и системах организма женщины). В свою очередь генитальный эндо-метриоз подразделяется на внутренний (тело матки, ее перешеек, интерсти-циальные отделы маточных труб) и наружный (наружные половые органы, влагалище и влагалищная часть шейки матки, ретроцервикальная область, яични-
ки, маточные трубы, брюшина, выстилающая углубления малого таза). Наружный генитальный эндометриоз целесообразно классифицировать по отношению к брюшине: внутрибрюшной (пернтонеальный) эндометриоз (яичники, маточные трубы, брюшина, выстилающая углубления малого таза) и экст-раперитонеальный эндометриоз (наружные половые органы, влагалище, влагалищная часть шейки матки, ретроцервикатьная область).
В современном представлении теории патогенеза эндометриоза могут быть подразделены на пять основных групп, среди которых выделяют транспортную (имплантационную, транспортную, иммиграционную, лимфогенной, гематогенной и ятрогенной диссеминации), целомической метаплазии, эмбриологических клеточных гамартий, гормональную, а также ряд иммунологических концепций.
Наибольшее распространение получила имплантадионная теория (или теория ретроградной менструации), впервые предложенная Sampson J.A. (1921) и обоснованная в серии его работ.
Теории лимфогенной, гематогенной и ятрогенной диссеминации, а также ретроградной менструации по существу представляют различные концепции транспортной гипотезы происхождения эндометриоза, т. к. отличает их лишь, способ переноса клеток эндометрия за пределы его физиологической локализации.
Теория целомической метаплазии представляет наиболее спорный аспект в патогенезе эндометриоза. В соответствии с этой гипотезой, впервые выдвинутой Н.С. Ивановым в 1887 г. и разработанной R. Meyer (1903), развитие эндометриоза происходит вследствие перерождения (метаплазии) мезотелия брюшины, в результате которого образуются фокусы эндометриоподобных желез и стромы. С точки зрения теории целомической метаплазии сторонники ее объясняют обнаружение признаков эндометриоза у женщин с агенезией мюл-леровского протока, отсутствием матки или ее гипоплазией, дисгенезией гонад, а также случаи выявления эндометриоза у мужчин. Источником этих опухолей является поверхностный (зародышевый) эпителий гонад, развивающийся из це-ломического эпителия. Последний, как известно, дает начало парамцуезонеф-ральным протокам, из которых формируется трубный, эндоцервикальный и эн-дометриальный эпителий. Целомический эпителий гонад обладает способно-
стью к превращению (метаплазии) в эпителий различного вида, в т. ч. и эндо-метриального типа. Подтверждением этого служат данные о присутствии антигена СА-125 как в фетальном целомическом эпителии и в его производных (плевре, перикарде, брюшине, поверхностном эпителии яичника и мюллеров-ском протоке), так и в эпителии мюллеровского происхождения у взрослых пациенток (трубном, эндометриальном, эндоцервикальном), что. несомненно, указывает на их общее эмбриональное происхождение. Гипотеза целомической метаплазии до настоящего времени не получила экспериментального подтверждения.
В отношении гормональной и иммунологической концепций патогенеза эндометриоза, можно предположить, что гормональные и/или иммунологические нарушения не являются непосредственной причиной формирования эндометриоидных фокусов, а лишь способствуют этим процессам, т. е. играют роль факторов (пусковых механизмов), предрасполагающих к возникновению патологического процесса.
До настоящего времени механизм происхождения и развития эндометриоза окончательно не изучен. Ни одна из известных теорий в полной мере не отвечает современным представлениям об этом заболевании. Даже гипотеза комбинации имплантационной и метапластической теорий, согласно которой эндометриоз представляет ни что иное, как метапластическую реакцию эпителия в ответ на раздражающее действие трансплантированной эндометриальнои ткани, не в полной мере объясняет пути формирования и развития эктопических участков эндометриоподобных желез и стромы.
Происхождение (а, в последующем, и развитие) эндометриоидных фокусов, отличающихся между собой как клиническим течением, так и гистологическим строением, имеет различную патогенетическую основу.
Выше освещены аспекты патогенеза наружного эндометриоза. Механизм развития внутреннего эндометриоза тела матки остается в достаточной мере спорным и малоизученными. Наиболее вероятной является имплантационная теория происхождения аденомиоза. Железы и строма базального слоя эндометрия врастают в мышечный слой матки. Наиболее предпочтительной выглядит гипотеза их диссеминации как ятрогенным (врастание элементов эндометрия в подлежащую мышечную основу во время абортов, осложненных родов, диагностических выскабливаний эндометрия), так и лимфо- и гематогенным путем.
Структурно-функциональные особенности гениталыюго эндометриоза
С морфологических позиций наиболее важным является не столько сходство эндометриоидной ткани с эндометрием по строению и функции, сколько обязательное присутствие в ней 2 компонентов - эпителиального и стромаль-ного.
Наружный эндометриоз, особенно перитонеальный, макроскопически отличается широким полиморфизмом и может быть диагностирован даже при отсутствии видимых изменений серозного покрова. Более того, почти у 70 % женщин в перитонеальной жидкости обнаруживаются жизнеспособные эн-дометриоидные клетки.
В настоящее время является общепризнанным, что развитие внутреннего эндометриоза обусловлено пенетрацией железистого и стромального компонентов базального слоя эндометрия в миометрий. Поэтому гистологическая диагностика внутреннего эндометриоза основана на идентификации в мышечном слое матки очагов, имеющих сходство с ее слизистой оболочкой. Погружному росту составных компонентов базального слоя эндометрия способствуют дес-молитические процессы, а также нейро - дистрофические применения в области гистобиологического барьера, деструкция соединительно-тканной основы мио-метрия. При морфологическом исследовании участков миометрия, вовлеченных в патологический процесс, очаги эндометриоза имеют характерное строение и представлены железистыми структурами различной формы и величины (от малых с узким просветом, до более крупных, в том числе, кистозно-расширенных), выстланных цилиндрическим эпителием. Железы в эндометриоидных гетеротопиях располагаются изолированно в виде скоплений. Строма, окружающая железы, имеет цитогенный характер и состоит из многочисленных фибробластоподобных клеток с вариабельным содержанием колла-геновых волокон, лимфоцитов, гистиоцитов, мелких кровеносных сосудов. В количественном отношении в одних эндометриоидных гетеротопиях цитоген-ная строма преобладает над железистым компонентом, в других - имеет вид узкой полоски вокруг желез. Следует отметить, что эндометриоидные гетерото-пии с железистым эпителием без признаков функциональной активности и очаги т. н. функционально активного эндометриоза наблюдаются в одном и том же участке поражения независимо от степени распространения эндометриоза, а также состояния яичников и эндометрия. Нередко функционально неактивные
и активные эндометриоидные гетеротопии располагаются непосредственно вблизи или на небольшом расстоянии друг от друга. Функционально активные эндометриоидные гетеротопии характеризуются богатой клетками стромой, окружающей железы и пролиферативными изменениями эпителия различной интенсивности (в отдельных железах наблюдается высокая митотическая активность). Подобные особенности в эндометриоидных гетеротопиях преимущественно наблюдаются у больных с ановуляторными нарушениями менструальной функции. В очагах функционально неактивного эндометриоза строма менее выражена, с относительно высоким количеством коллагеновых волокон; в железистом эпителии преобладают индифферентные клеточные элементы. В отдельных эндометриоидных очагах имеется сочетание эпителия без признаков функциональной активности и пролиферативного типа. Последние идентифицируются в участках эпителия, в которых прилежащая строма отличается сосудистым компонентом преимущественно капиллярного типа.
Гистологическая картина эндометриоза яичников не отличается от эндометриоза в др. органах. Однако в ряде случаев обнаружение эндометриоза яичников сопряжено с определенными трудностями, обусловленными, главным образом, двумя факторами:
малыми размерами гетеротопии, расположенных на наружной поверхности яичников или в поверхностных отделах коркового слоя;
отсутствием в стенках эндометриоидных кист эпителиальной выстилки (лишь у 50 % пациенток с кистозными образованиями яичников, имеющими шоколадное содержимое, удается верифицировать признаки эндометриоза).
На ранних стадиях эндометриоидные поражения располагаются в поверхностных отделах яичников и/или на их наружной поверхности, имеют небольшие размеры, а глубина пенетрации в подлежащую ткань не превышает 1-5 мм. По мере прогрессирования патологического процесса появляются мелкие кистоз-но-расширенные железы с тенденцией к постепенному увеличению и росту в направлении овариальной ткани, что приводит к образованию кист. Как правило, диаметр эндометриоидных кист не превышает 2-3 см, в редких наблюдениях достигает 10 см и более. По мере формирования кистозной полости с геморрагическим содержимым (шоколадным) отмечается увеличение толщины ее стенки, что сопровождается усилением фиброзных изменений последней. Благодаря способности крови проникать через стенку эндометриоидной кисты, на поверхности последней формируются плотные спайки, развитие которых при-
водит к сращению патологически измененного яичника с задней поверхностью матки и широкой связки.
В очагах эндометриоза яичников (т.н. малые формы) железистый эпителий преимущественно цилиндрический, пролиферативного типа, тогда как эпителиальная выстилка эндометриоидных кист представлена, главным образом, однорядным цилиндрическим или кубическим эпителием, обычно ин-дифферерентного типа без признаков функциональной активности, а также с дистрофическими изменениями. Эпителиальная выстилка эндометриоидных кист яичников характеризуется гетерогенностью функционального состояния.
Как и выстилающий эпителий, подэпителиальная строма в стенке эндометриоидных кист также отличается гетерогенностью функционального состояния: различные участки стенки кист характеризуются вариабельностью по-дэпителиальной цитогенной ткани, неодинаковым содержанием фибробла-стоподобных клеток, лимфоцитов, гистиоцитов, соединительной тканных волокон, сидерофагов, а также выраженностью отека и кровоизлияний.
Необходимо подчеркнуть, что функциональное состояние эпителиального и стромального компонентов эндометриоидной кисты во многом определяется особенностями васкуляризации стенки опухолевидного образования.
В участках ретроцервикального эндометриоза, независимо от размеров поражения, среди волокнистой соединительной ткани располагаются очаги цитогенной ткани с единственной железистой структурой или скоплениями желез различной формы и величины, включая кистозно-расширенные. Содержание цитогенной ткани в гетеротопиях ретроцервикальной локализации характеризуется широкой вариабельностью - от тонкого слоя с небольшим количеством клеточных элементов вокруг железистых структур до относительно крупных скоплений с многочисленными фибробластоподобными клетками с примесью лимфоцитов и гистиоцитов. В большинстве железистых структур эпителий имеет сходство с таковым эндометрия ранней стадии пролиферации или лишен признаков функциональной активности. В отдельных участках ретроцервикального эндометриоза наблюдаются железы с изменениями, идентичными секреторному эндометрию, что подтверждается и электронномикроскопиче-ским исследованием патологических имплантантов. Однако отсутствие основных показателей секреторной трансформации железистого эпителия - гигантских митохондрий и отложений гликогена в цитоплазме и системы канальцев в ядре клеток - позволяют предположить неполноценный характер секреторных
преобразований. На основании данных электронной микроскопии нельзя исключить, что функциональное состояние железистого эпителия - в очагах рет-роиервикального эндометриоза в определенной мере обусловлено характером подэпителиальной стромы и ее васкуляризацией: эпителиальные клетки с хорошо развитыми цитоплазматическими органеллами и многочисленными системными микро-ворсинками на апикальной поверхности располагаются, главным образом, в железистых структурах гетеротопий, богатых цитогенной тканью, причем сосуды нередко локализуются вблизи базальной мембраны желез. Подобная субмикроскопическая картина наблюдается и при эндометриоидных поражениях брюшины.
Обнаружение в железах гетеротопий с отдельными признаками секреторных преобразований позволило некоторым авторам высказать предположение, что функциональная активность в эндометриоидных имплантатах, определяется генетически, а эффективность гормонального воздействия на них зависит от дифференцировки клеток и степени развития цитоплазматических органелл.
Диагностика эндометриоза брюшины сопряжена с определенными трудностями, обусловленными отсутствием визуальных изменений в пораженных участках серозного покрова. Подтверждением этому служат данные сканирующего электронномикроскопического исследования брюшины больных, страдающих так называемым бесплодием неясного генеза, а также подвергшихся хирургическому лечению по поводу наружного генитального эндометриоза
Согласно данным литературы, генетическое программирование клеточных элементов играет немаловажную роль в их дифференцировке, структурных изменениях и обеспечении специфической функции. В связи с этим, влияние гормонов на клеточные элементы рассматривается как вторичное, обусловленное дифференцировкой клеток. Многие очаги эндометриоза лишены признаков функциональной активности, поскольку не имеют достаточного количества эс-трогенных и прогестероновых рецепторов. Обнаружено, что содержание эстро-генных, прогестероновых и андрогенных рецепторов в эндометриоидных гете-ротопиях ниже таковой в эндометрии.
Таким образом, несмотря на значительный прогресс, достигнутый при изучении эндометриоза, многие аспекты этой проблемы остаются открытыми и, прежде всего, это касается макроскопических особенностей гетеротопий с учетом их морфологической картины, патофизиологических механизмов регрессии
и экспансивного роста. Не вызывает сомнений, что для решения утих вопросов необходимо проведение комплексных мероприятий с использованием высокоинформативных современных методов исследования.
ЭКСТРАПЕРИТОНЕАЛЬНЫЙ ЭНДОМЕТРИОЗ ЭНДОМЕТРИОЗ ШЕЙКИ МЛ ТКИ
Результаты современных исследований свидетельствуют о резком возрастании частоты данной гетеротопий в обшей популяции. Одним из объяснений подобного роста считают широкое применение на рубеже 60-70 гг. диатермо-коагуляции. Диатермокоагуляция (ДЭК), произведенная с целью терапии эндо-цервикозов в 1-ую фазу менструального цикла является предрасполагающим фактором для развития эндометриоза шейки матки, т. к. грануляционная ткань, образовавшаяся на раневой поверхности влагалищной части шейки матки после отторжения струпа, представляет идеальную зону для имплантации клеток эндометрия, отторгшихся во время очередной менструации.
studfiles.net
Эндометриоз
Эндометриоз представляет собой эндометриоподобное разрастание ткани, которая по своим морфологическим признакам сходна по строению со слизистой полости матки, но развивается вне пределов обычного расположения эндометрия.
Эндометриоз обладает особенностью к пенетрирующему росту в окружающие ткани, что объясняется протеолитическими свойствами стромы его. Он может прорастать слизистые оболочки, мышечную ткань, серозу, клетчатку, кожу и даже кость. Эндометриоз обладает особенностью метастазировать. Распространение его клеток осуществляется током крови или лимфы, происходит также в результате перфорации эндометроидных кист.
Основными составными частями эндометриоза являются эндометриальный эпителий и цитогенная строма. Эндометриоз, в котором железистая ткань отсутствует, называется стромальным, или интерстициальным.
Подавляющее большинство исследователей рассматривают их как эндометроидные гетеротопии. Следует иметь в виду возможность злокачественного перерождения эндометриозов (в рак, саркому или канцеросаркому). В очаге одновременно с эндометриоподобным эпителием разрастается также соединительная ткань.
В развитии эндометриоза этиопатогенетическое значение имеет ряд факторов. Установлена роль гормональных факторов в развитии этого заболевания. Существенное значение при этом имеет повышение содержания эстрогенного гормона и недостаток прогестерона.
В этиопатогенезе эндометриоза придается большое значение травме. Увеличение частоты эндометриоза, наблюдаемое в последние годы, связывают с совершенствованием оперативной техники и расширением показаний к оперативным вмешательствам на органах малого таза.
Особенное значение в возникновении его придается операциям, во время которых вскрывают полость матки (кесарево сечение, вмешательство по поводу перфорации матки, удаление подслизистых узлов с оставлением матки). Выскабливание слизистой и зондирование матки, продувание труб могут также способствовать отторжению и распространению кусочков эндометрия. У женщин после диатермокоагуляции на шейке матки ретроцервикальный и цервикальный эндометриоз выявляется в 33,7% (Е. Е. Гиговский, 3. В. Малышева, 1974).
Очевидно, неоднократные выскабливания слизистой матки способствуют развитию эндометриоза не только в результате травмы слизистой, но и ретроградного поступления крови по трубам.
Грубая пальпация матки во время операции может способствовать выдавливанию частиц эндометрия в просвет трубы. Доказана также возможность прорастания эндометриоза по каналам от лигатур. Следовательно, самые разнообразные операции и манипуляции на матке могут способствовать развитию заболевания.
Затруднение естественного оттока менструальной крови и поступление ее по трубам в малый таз или брюшную полость является также фактором, способствующим развитию эндометриоза. Затруднение естественного оттока крови наблюдается чаще при ретрофлексии, несколько реже при гиперантефлексии матки и атрезии шеечного канала.
Многочисленные данные литературы дают основание считать, что наследственные факторы в возникновении эндометриоза могут играть определенную роль.
Наиболее распространенным является разделение эндометриоза на половой (генитальный) и внеполовой (экстрагенитальный). Половой эндометриоз разделяют на внутренний и наружный. К внутреннему (внутри матки) относится эндометриоз матки и интерстициалыюй части маточных труб. Наружный половой эндометриоз включает эндометриоз яичников, маточных труб (кроме интерстициальной их части), влагалища, наружных половых органов, промежности, влагалищной части шейки матки, круглых маточных связок, ретроцервикальный (эндометриоз дугласова пространства, сводов влагалища, шеечно-прямокишечный).
Экстрагенитальный эндометриоз может локализоваться в кишечнике, аппендиксе, сальнике, диафрагме, мочевом пузыре, почках, мочеточниках, пупке, паховом канале, послеоперационных рубцах, легких, плевре, конечностях, позвоночнике и др. В 92–94% случаев отмечается генитальный эндометриоз.
Эндометриоз может развиваться у лиц различного возраста, но наиболее часто он отмечается в 35–45 лет. Более чем у половины больных эндометриоз поражает матку. Характер поражения матки может быть диффузным или узелковым, первый из них встречается чаще. Независимо от характера заболевания одной из отличительных особенностей его является отсутствие соединительнотканной капсулы. Эндометриоз может возникать в любой части матки, но чаще обнаруживается в задней стенке и у дна, реже – в передней стенке и еще реже – в углах матки или в области внутреннего маточного зева.
Макроскопическая картина эндометриоза на разрезе напоминает изъеденное червями дерево или пчелиные соты. Прорастание эндометриоза в параметрий может симулировать инфильтрат.
Ведущим признаком является нарушение менструаций. У части больных маточные кровотечения принимают характер метрораргий. Иногда отмечаются коричневые выделения в конце регул и спустя несколько дней после них. Особенностью маточных кровотечений при этом заболевании является слишком упорный их характер. Консервативная терапия или неоднократные выскабливания в лучшем случае дают только временный эффект.
В этиологии маточных кровотечений у больных эндометриозом имеют значение следующие факторы: изменение функции яичников увеличение продукции эстрогенов и недостаток прогестерона) и слизистой матки (гиперплазия простая или железисто-кистозная, нередко – полипоз), понижение сократительной способности матки, затруднение оттока крови в результате механического сдавления вен железистыми разрастаниями, увеличение менструирующей поверхности, чрезмерная васкуляризация матки, повышенная ломкость сосудистых стенок.
У многих больных ведущим симптомом является дисменорея. Встречается она приблизительно в половине случаев. Боль появляется за несколько дней до менструации, в начале ее усиливается и затихает после окончания. Боль может быть очень сильной, сопровождаться рвотой, тошнотой, обмороками, головной болью и нетрудоспособностью. Половые сношения могут сопровождаться сильной болью, которая возникает в результате раздражения нервных рецепторов эндометриоидных очагов, увеличения содержания эстрогенов и недостатка прогестерона, спазма шейки матки. Указанные клинические симптомы встречаются в различных вариантах.
Эндометриоз матки может сочетаться с различными заболеваниями половых органов – кистами яичников, хроническим воспалением придатков, карциномой матки, но чаще всего сочетаются с миомой. Сочетание эндометриоза и миомы матки объясняется общностью патогенеза этих заболеваний.
При наружном эндометриозе чаще всего поражаются яичники, причем односторонняя локализация встречается примерно в 2 раза чаще двусторонней. Основное значение в патогенезе этого заболевания имеет имплантация частиц эндометрия в результате ретроградного заноса крови из матки. Нередко целость эндометриоидной кисты нарушается и ее содержимое попадает в брюшную полость, в результате чего образуются спайки и сращения, которые сопровождаются инфильтрацией стенок соседних органов. Исходом нарушения целости стенок кисты («протекания») помимо образования спаек и сращений является возникновение ретроцервикального эндометриоза. Эндометриоз яичника может сочетаться с различными новообразованиями этого органа. Нередко в одном яичнике наряду с «шоколадными» кистами наблюдаются дермоидные, сосочковые или другие кистомы яичника.
Подавляющее большинство больных эндометриозом яичников отмечают ноющую и тянущую боль в нижних отделах живота или пояснично-крестцовой области, причем накануне и во время регул она заметно усиливается. У 66% больных эндометриозом яичников отмечается дисменорея. У части больных, не имеющих болевого синдрома, накануне и во время менструаций появляются тяжесть внизу живота, запоры и вздутие кишечника. Болевой синдром и запор встречаются чаще и сильнее выражены тогда, когда в спаечный процесс вовлечена прямая кишка и развивается ретроцервикальный эндометриоз.
В течение болезни могут наблюдаться периоды сравнительного благополучия, а затем внезапно наступает обострение, как правило, накануне или во время регул, что объясняется «протеканием» кисты.
Клиническая картина разрыва «шоколадных» кист, когда значительное количество содержимого кисты попадает в брюшную полость, напоминает перитонит, появляются симптомы раздражения брюшины. Ретроцервикальный эндометриоз по частоте занимает третье место (после поражения матки и яичников). Ретроцервикальный эндометриоз чаще, чем эндометриоз других локализаций, подвергается малигнизации. Обычно больные жалуются на ноющую боль внизу живота, пояснице, крестце. Встречаются больные как с резко выряженным болевым синдромом, так и с асимптомными формами, что зависит от степени распространения эндометриоза. Боль появляется накануне менструаций, резко усиливается во время ее. Болевой синдром нередко усиливается и при акте дефекации, отхождении газов, движении и т. д. Дисменорея прогрессирует. Большинство больных жалуются на боль при половых сношениях. Одним из симптомов являются запоры накануне и во время регул. Ретроцервикальный эндометриоз может прорастать в задний свод влагалища, прямую кишку, может вызвать сдавление мочеточника. Нередко наблюдается несоответствие между размерами очага поражения и выраженностью боли – небольшие узлы величиной с вишню могут вызвать мучительную боль, в то время как образования с яйцо не сопровождаются болевым синдромом. Особенностью болей внизу живота при ретроцервикальном эндометриозе является их «стреляющий» характер и иррадиация в область прямой кишки.
При ректороманоскопии обнаруживаются гиперемия и отечность слизистой, выбухание стенки кишки внутрь, причем накануне и во время регул эти изменения усиливаются.
Эндометриоз послеоперационного рубца передней брюшной стенки встречается редко. Чаще всего эндометриоз во время беременности наблюдается в матке, преимущественно в задней ее стенке или расположен ретроцервикально.
Обычно эндометриоидные очаги в течение первых 2–3 мес беременности увеличиваются в размерах, затем уменьшаются и размягчаются. Многие авторы поэтому считают беременность и роды средством лечения эндометриоза. Однако заболевание отрицательно сказывается на течении беременности и родов – количество самопроизвольных абортов встречается в 2 раза чаще, оно может быть причиной разрыва матки, роды могут осложниться слабостью родовой деятельности, в ранний послеродовой период может возникнуть атоническое кровотечение.
Диагностика эндометриоза подчас является трудной, но вполне выполнимой задачей. Правильный предоперационный диагноз обычно устанавливается не более чем у 50% больных.
Эндометриоз чаще всего принимают за фибромиому (до 97%). По наблюдениям Bird и Mcelin (1975), в большинстве случаев диагноз устанавливается во время операции по поводу полицоза эндометрия или миомы матки и лишь в 15% случаев до оперативного вмешательства. В. В. Заец (1971) установил, что кровотечения и боли при опухоли матки сравнительно небольшой величины позволяют думать о сочетании миомы и эндометриоза, если нет субмукозного миоматозного узла.
Ретроцервикальный эндометриоз нередко диагностируется как рак, эндометриоз влагалища принимают за рак или хорионэпителиому. Очаги в малом тазу мелкобугристы и отличаются большой плотностью, в связи с чем их принимают за туберкулезное или раковое поражение.
Большое значение имеет хорошо собранный анамнез (перенесенные в прошлом операции, диатермокоагуляция, многократные аборты, диагностические выскабливания, осложненные роды и др.). По данным А. Г. Гайнулиной (1974), симптомы эндометриоза появляются в сроки от 3 до 8 лет после перенесенной операции.
Отличительной особенностью объективных данных при эндометриозе является их изменчивость и зависимость от менструального цикла.
Характер заболевания, по данным различных авторов, удается подтвердить гистологически только в 55–65%. Для гистологического подтверждения диагноза рекомендуется брать больше кусочков для исследования. Одним из методов диагностики является гистерография, при этом обнаруживаются «карманы» и «отростки» за пределами контурной линии полости матки. Гистерографию лучше производить на 3–4-й день посл^менструации или выскабливания, так как отсутствие в это время функционального слоя слизистой оболочки матки не мешает проникновению контрастного раствора в эндометриоидные полости. Ценным диагностическим методом может быть рентгенопельвиография в условиях пневмоперитонеума, которая позволяет судить о степени увеличения матки, состоянии придатков и наличии спаечного процесса.
Для лечения эндометриоза применяются гормональный, хирургический и симптоматический методы. В последнее время чаще применяют гормональный метод, который является не только более безопасным, но и более результативным. Для гормонального лечения эндометриоза в настоящее время широко применяются синтетические прогестины. Оксипрогестерона капронат обладает выраженным прогестероновым действием, направленным на эндометрий. Под влиянием этого гормона наступают секреторные изменения слизистой, задерживается развитие гиперпластических процессов в эндометрии. Поэтому лечение оксипрогестерона капронатом патогенетически обосновано. При всех формах эндометриоза этот препарат назначают по 125 мг внутримышечно 1 раз в неделю (всего 20 инъекций). Лечение инфекундином проводится так же, как и в целях контрацепции, на протяжении 3–12 мес. Инфекундин оказывает тормозящее влияние на гипоталамические центры, благодаря чему снижается продукция гонадотропинов в гипофизе, не наступает овуляция; в эндометрии происходят регрессивные процессы. Эффект в результате лечения синтетическими прогестинами отмечен в 66–100% (Е. В. Кравкова, 1971).
Перед лечением синтетическими прогестинами необходимо исследовать показатели свертывающей системы крови и функцию печени, так как эти медикаменты могут способствовать возникновению тромбофлебита и обостряют заболевания печени.
Оперативное лечение эндометриоза, если оно необходимо, в отличие от других гинекологических заболеваний, производится за 1–2 дня до менструации, так как в этот период очаги поражения лучше выражены.
При обширных поражениях эндометриозом органов малого таза целесообразно назначать предоперационную терапию синтетическими прогестинами, что облегчает выполнение операции. Хирургическое лечение проводится у больных со значительными кровотечениями н болью, с эндометриоидными кистами яичников, а также в случаях сочетания с миомой матки.
Рентгенотерапия, рассчитанная на подавление функции яичников, в настоящее время практически не применяется: этот метод нецелесообразно использовать у молодых женщин, кроме того, он не гарантирует от возникновения рецидивов.
При болевом синдроме или нарушении регул проводится симптоматическое лечение (болеутоляющие и кровоостанавливающие средства).
Профилактика эндометриоза заключается в предотвращении попадания эндометрия из полости матки в другие участки организма: защита брюшной полости от кусочков эндометрия, во время кесарева сечения необходимо избегать проведения лигатур через слизистую матки, тщательное удаление содержимого эндометриоидных кист из брюшной полости, устранение затруднений для естественного оттока менструальной крови, продувание труб под давлением не более 160 мм рт. ст., запрещение занятий спортом во время менструаций.
ginekolog.my1.ru
ТЕМА 5.docЭндометриоз ,заболевания подросткой и детей
ТЕМА 5. ЭНДОМЕТРИОЗ.
ТЕМА №5 эндометриоз.
1. Эндометриоз - определение понятия.
2. Этиология и патогенез эндометриоза.
3. Классификация эндометриоза.
4.Клиника эндометриоза.
5. Аденомиоз - определение понятия. Классификация.
6. Клиника аденомиоза.
7. Методы диагностики аденомиоза.
8. Показатения к хирургическому лечению аденомиоза.
9. Эндометриоз шейки матки.
10. Эндометриоз маточных труб.
11. Эндометриохз яичников. Клиники. Диагностика.
12. Показания к хирургическому лечению эндорметриоза яичников.
13. Позадишеечный (ретроцервикальный) эндометриоз.
14. Клиника позадишеечного эндометриоза.
15. Принципы лечения эндометриоза.
16. Показания к хирургическому лечению эндометриоза.
17. Экстрагенитальный эндометриоз.
Эндометриоз может быть не только генитальным, но и экстрагенитальным, поэтому диагностика сложна. Эндометриоз можно рассматривать как эндометриоидно подобное разрастание, развивающееся за пределами гениталий. Участки эндометриоидной ткани мигрируют в несвойственные ее места, развиваются там, превращаются в опухолевидные разрастания и функционируют почти также, как функционирует эндометрий. Постоянная секреция этих участков приводит к продукции крови, что превращает близлежащие ткани в соединительнотканные рубцы, хронический воспалительный процесс и т.д. Микроскопические и гистологические данные позволяют констатировать, что эта неистинная опухоль, это опухолевидное, гормонозависимое образование. Эндометриоз может быть врожденным, но чаще приобретенный. Возникает в репродуктивный период, и может исчезать в менопаузальном периоде, то есть он непосредственно связан с гормональной функцией. Эндометриоз может быть в любых местах, но чаще всего в области гениталий.
Классификация по локализации:
1. Экстрагенитальный эндометриоз: коньюктивы глаз, эндометриоз пупка, эндометриоз кишки и других органов.
2. Генитальный эндометриоз
· наружный (все что вне матки): эндометриоз яичников (шоколадные кисты яичников), эндометриоз фаллопиевых труб, эндометриоз угла матки, эндометриоз заднего свода влагалища, шейки матки, позадишеечный эндометриоз. Часто бывают эндометриоидные очажки, рассыпанные по брюшине малого таза — могут быть брюшине мочевого пузыря, брыжейке кишечника и т.д.
· внутренний (как правило, эндометриоз тела матки или другое название аденомиоз). Эндометриоз является нетипичной, гормональнозависимой опухолью, и отличается от злокачественных опухолей, тем что не обладает клеточным атипизмом.
Существуют различные теории возникновения эндометриоза. ·
1.Имплантационная — эндометрий может имплантироваться из матки, а также распространяться лимфогенно и гематогенно. Например, при вскрытии эндометриодной кисты яичника. Имплантация эндометрия во время операции, связанных со вскрытием полости матки — кесарево сечение, консервативная миомэктомия, перфорация матки, то есть занос элементов эндометрия в несвойственные ему места.
2.Теория эмбрионального происхождения. Сущность заключается в эмбриобластическом происхождении опухоли из остатков Мюллерова протока. Доказательством этой теории может служить наличие эндометриоза в детском возрасте, сочетание его пороками развития мочевыводящих путей. ·
3.Теория дисфункции иммунной системы: известно, что при эндометриозе существует дисфункция иммунной системы, проявляющаяся Т-клеточным иммунодефицитом (нарушение бластотрансформации лимфоцитов). . Нарушение иммунного гомеостаза при эндометриозе предположили M. Jonesco и C. Popesco в 1975 г. Авторы считали, что клетки эндометрия, попадая в кровь и другие органы, представляют собой аутоантигены. Считается, что такая супрессия обусловленна блокадой Т-клеток иммунными комплексами. Иммунностимулирующая терапия, поэтому применяется в лечении эндометриоза.
4. Миграционная теория. Считается, что клетки эндометрия попадают в кровеносное русло и распространяются в другие органы. Считается что эндометриоз пупка, костей, кишечника является мигрирующим. Таким образом, единой теории нет. Однако существует ряд факторов, играющих роль в развитии заболевания:
5.Гормональные нарушения, которые связаны с нарушением синтеза и содержания стероидных и гонадотропных гормонов. Возникает повышенная продукция ФСГ, гиперэстрогения связанная с этими нарушениями, что приводит к активной функции эндометриоидных клеток.
6. Воспалительный фактор. Любая локализация эндометриоза сопровождается воспалительной реакцией вокруг. Например, шоколадные кисты находятся в очень тесной связи с листками широкой связки, областью дугласового карман, и в силу своей тяжести они опускаются в дуглассов карман и развивается спаечный процесс. Маленький очажок на брюшине также сопровождается зоной инфильтрации, гиперемии вокруг очажка.
7.Наследственные факторы, эндометриоз наследственно детерминирован генами, ассоциированными с определенными антигенами системы HLA, а именно НА, А10, В5, В27
. - в развитии эндометриоза существенную роль играют генетические факторы; - имеется достоверная связь между определенными генетическими факторами и анатомической локализацией эндометриоидных поражений; - на основе экспрессии биохимических генетических маркеров можно установить наличие или отсутствие предрасположенности к эндометриозу или уже развившемуся заболеванию. Также как при миоме имеет значение наследственный фактор (может прослеживаться в трех поколениях).
8.Аномальное положение матки. Ретрофлексированное положение матки способствует забросу менструальной крови в первые дни, когда еще внутренний зев спазмирован. Через маточные трубы менструальная кровь забрасывается в брюшную полость. Атрезия цервикального канала, внутреннего зева — возникают после выскабливания (происходит реактивное воспаление и слипание стенок) ведет в гематометра, и заброс крови. Американские авторы подтвердили, что излитие менструальной крови в брюшную полость ведет к возникновению эндометриозу.
9.Метапластическая теория происхождения эндометриоза Эта теория отражает наиболее спорный вопрос в патогенезе заболевания и предложена Н.Н. Ивановым ( 1897 ), R. Meyer ( 1903 ). Сторонники данной теории считают, что эмбриональные клеточные элементы, расположенные между зрелыми клетками серозного покрова малого таза, могут трансформироваться в эпителий маточно-трубного типа. Другими словами, очаги эндометриоза могут возникать из мультипотентных клеток мезотелия брюшины. В возникновении эндометриоза важное значение имеет так называемый мюллеров потенциал мезотелия, который связан с понятием о “вторичной мюллеровой системе”, предложенным Lauchlan.. Классификация наружного эндометриоза по A. Acosta и соавт. (1973) Малые формы: • одиночные гетеротопии на тазовой брюшине; • одиночные гетеротопии на яичниках без спаек и рубцов.Эндометриоз средней тяжести: • гетеротопии на поверхности одного или обоих яичников с образованием мелких кист; • невыраженный периовариальный или перитубарный спаечный процесс; • гетеротопии расположены на брюшине внематочного пространства с рубцовым процессом и смещением матки без вовлечения в патологический процесс толстого кишечника.Тяжелые формы наружного эндометриоза: • эндометриоз одного или обоих яичников с образованием кист диаметром более 2 см; • поражение яичников с выраженным периовариальным и/или перитубарным спаечным процессом; • поражение маточных труб с деформацией, рубцеванием, нарушением проходимости; • поражение брюшины с облитерацией внематочного пространства; • поражение крестцово-маточных связок и брюшины внематочного пространства; • вовлечение в патологический процесс мочевыводящих путей и/или кишечника.Классификация в зависимости от локализации Эндометриоз тела матки (аденомиоз): I степень – процесс ограничен слизистой оболочкой тела матки; II степень – распространение эндометриоза до середины толщины миометрия; III степень – вовлечение в патологический процесс всей стенки матки; IV степень – вовлечение в патологический процесс париетальной брюшины и соседних органов.Эндометриоз яичников: I степень – небольшие участки эндометриоза на поверхности яичников и на брюшине прямокишечно-маточного углубления; II степень – односторонняя эндометриоидная киста диаметром не более 5-6 см, небольшие участки эндометриоза на брюшине малого таза, спаечный процесс в области придатков; III степень – эндометриоидные кисты обеих яичников диаметром более 5-6 см, участки эндометриоза на серозном покрове матки, маточных труб, брюшине малого таза, выраженный спаечный процесс; IV степень – двусторонние кисты больших размеров с переходом на соседние органы.Ретроцервикальный эндометриоз: I степень – эндометриоидные участки в пределах ректовагинальной клетчатки; II степень – эндометриоидная ткань переходит на шейку матки и стенку влагалища с образованием мелких кист; III степень – процесс распространяется на крестцово-маточные связки и серозный покров прямой кишки; IV степень – процесс распространяется на слизистую оболочку прямой кишки, облитерирует прямокишечно-маточное пространство с возникновением спаечного процесса в области придатков матки.Диагностика Физикальные методы исследования • Опрос: характеристика боли, нарушений менструальной, репродуктивной, сексуальной функций; анамнез: наследственность, перенесенные заболевания и операции, особенности становления менструального цикла, детородной и сексуальной функций. • Общий осмотр: очаги эндометриоза. • Глубокая пальпация живота: болезненность, опухолевидные образования. • Осмотр наружных половых органов: очаги эндометриоза. • Осмотр в зеркалах: очаги эндометриоза. • Бимануальное гинекологическое обследование: подвижность, болезненность, величина, консистенция матки, придатков матки; состояние крестцово-маточных связок; наличие инфильтрации, рубцов, опухолевидных образований. • Ректальное обследование: опухолевидные образования, болезненность в области крестцово-маточных связок, инфильтрации, рубцовые деформации.Лабораторные исследования Обязательные:• определение группы крови и резус-фактора; • общий анализ крови и мочи; • сахар крови; • биохимические показатели крови; • бактериоскопический анализ выделений; • цитологическое исследование; • гормональная кольпоцитология.При наличии показаний:• определение в крови опухолевых маркеров с целью дифференциальной диагностики: • СА (Саnсег аntigen) 19-9 – повышение уровня в среднем до 30 Ед/мл; • СЕА (Саnсег Еmbryonic antigen) – повышение уровня; • СА 125 – повышение уровня в среднем до 28 Ед/мл, в некоторых случаях значительно; • СА 72-41– повышение уровня.Инструментальные методы исследования • Ультразвуковое сканирование (трансабдоминально, трансвагинально, допплерометрия). • Рентгенологическое исследование (гистеросальпингография и биконтрастная гинекография). • Цистоскопия, хромоцистоскопия, радиоизотопная диагностика. • Кольпоскопия. • Лапароскопия. • Ректороманоскопия. • Ядерно-магнитная резонансная томография. • Раздельное диагностическое выскабливание. • Биопсия.Дифференциальная диагностика • Лейомиома матки. • Хронический аднексит. • Опухоли гениталий. • Опухоли кишечника. • Гиперпластические процессы эндометрия. • Внематочная беременность. • Нефроптоз. • Мочекаменная болезнь. • Аппендицит. • Парапроктит, проктит, колит.
Клинические проявления аденомиоза.Встречается чаще диффузный, чем узловой. Различают аденомиоз в зависимости от инвазии в различные слои матки. Небольшое врастание в мышечную ткань — первая степень. Вторая степень — врастание во всю мышечную ткань. Третья степень — прорастание до серозного слоя. Это проявляется отдельно существующих полостей между мышечными волокнами. Эти полости бывают разных размеров, они как правило окружены соединительнотканными оболочками. Между соединительнотканными волокнами и отмечаются полости наполненные черной тягучей жидкостью. Как правило, клинические проявления аденомиоза тяжелы, сопровождаются рядом четких проявлений и симптомов. · В связи с гормональными нарушениями возникают мажущие кровянистые выделения до и после менструации. · Кровотечение во время месячных (обильные меноррагии), в связи с чем нарастает вторичная анемия. · Болевой синдром выражен при любых локализациях, носит циклический характер чем и отличается от кист яичников, миомы матки. Перед менструацией происходит активная секреция в очагах эндометриоза и возникают распирающие боли. Как только начинаются менструации происходит излитие крови, резорбция из этих очагов и боли стихают. Могут поражаться тазовые сплетения. Может быть ощущение тяжести внизу живота, чувство распирания; дизурические явления. Появляются тенезмы , и связанные с ними нарушения дефекации. Эти нарушения также носят циклический характер.
· Кровотечение не уменьшается после диагностического выскабливания полости матки. При исследовании кроме небольшого увеличения матки мы ничего не находим, что говорит о возможно начальной стадии эндометриозе. При бимануальном исследовании: увеличение матки, неровная поверхность, плотная консистенция, болезненность при исследовании. УЗИ: не дает яркой картины. Гистеросальпингография: извилистые ходы в толще миометрия. Больше никаких специальных исследований данных об эндометриозе не дают.
Лечение.Показанием к оперативному лечению является наличие аденомиоза 3 степени, прогрессирующее увеличение матки, сочетание аденомиоза с наружным эндометриозом, прогрессирующая гиперполименорея, отсутствие эффекта от проводимого лечения. Предполагаемый объем операции: целесообразно проводить экстирпацию матки, вопрос о придатках матки решается во время операции ( если женщина молодая, то важно сохранить шейку матки и яичника). Очень важное значение имеет обнаружение эндометриоидных кист яичника — шоколадные кисты. Клинические проявления эндометриоза придатков не всегда имеют место (50%). Уменьшение или увеличение (перед менструацией) размер кисты увеличивается, что позволяет проводить дифференциальную диагностику между с ретенционными кистами, с кистомами. Эти кисты содержат измененную кровь, могут быть единичные, многокамерные и т.д. Капсула обычно плотная, содержимое типа шоколада. Диагностика связана с появляющимися болями, бесплодием, данными УЗИ и т.д. Эндометриоз маточных труб диагностировать очень трудно. При гистеросальпинграфии определяются законтурные тени, то есть от основного контура имеются извилистые ходы.
Эндометриоз брюшины и клетчатки заднего свода— ретроцервикальный эндометриоз (позадишеечный эндометриоз). По началу больные могут не ощущать этого заболевания. Имеется боль при половых контактах, распирающие боли во время менструации, появление тенезмов во время менструаций. Довольно часто запоры, болезненная дефекация. Нередко возникает стенозирование кишки, прорастание кишки, кровотечение из кишки. При ректороманоскопии (является необходимым исследованием при такой локализации) можно выявить втяжение слизистой стенки прямой кишки, иногда очаги эндометриоза. Также закономерна для этой формы цикличность боли. Эндометриоз шейки матки, как правило виден, особенно в предменструальные дни. Связан с травматическим повреждением — диатермокоагуляция, диатермоэксцизия и т.п. На месте неизмененного эпителия видны ярко красные глазки 1-2 мм в диаметре. Эти глазки перед менструацией начинают кровоточить, что можно увидеть при осмотре в зеркалах.
Лечение. В лечении эндометриоза основу составляет гормональная терапия. Хорошо зарекомендовали себя синтетические прогестины — используются в циклическом режиме, чаще всего используются норкалут, регивидон,дюфастон (в режиме 25 через 5, или в режиме поддержания второй фазы цикла с 12 по 17 дни). Применяется в течение 5-6 циклов. Курсы могут длительными или прерывистыми по 5-6 месяцев. Можно сочетать с оксипрогестерон капронатом (по 250 мг) — поддержание второй фазы цикла. Лечение проводится систематически, до получения эффекта. Эндометриоз рецидивирует и поэтому лечение надо постоянно повторять,использование в лечении ингибиторов гипофизарных гормонов (ФСГ, ЛГ) — таназол, золадекс. Эти препараты ингибируют функцию выработку гипофизотропных гормонов, обеспечивающих дисбаланс при эндометриозе. Атрофируются очаги эндометриоза. Эти препараты вызывают медикаментозный кастрационный синдром (золодекс наиболее активен в этом плане). Золодекс действует 28 дней, вводится под кожу живота 1 раз в 28 дней. На курс лечения требуется 6 ампул. П. После оперативного лечения проводят противорецидивную терапию. Позадишеечный эндометриоз гормональному лечению не подвергается. Самая главная задача — снять воспаление (противоспалительная терапия, рассасывающая терапия), так как оно часто способствует формированию стриктурам мочеточников, прямой кишки и т.д. С помощью лапароскопической и эндоскопической техники можно коагулировать мелкие очаги эндометриоза, а далее проводят противорецидивную терапию.
Гинекология детей и подростков.
В гинекологии детей и подростков принято выделять следующие возрастные периоды: внутриутробного развития, новорожденности, период раннего детства, нейтральный (до7лет), препубертатный (от7 лет до года появления менархе), пубертатный (от наступления менархе до 16 лет) и подростковый (от 16 до 18 лет).
Гинекологические заболевания детей и подростков делятся на воспалительные заболевания, дисфункциональные заболевания периода полового созревания, нарушения полового развития, аномалии развития половых органов, опухоли половых органов и травмы.
Воспалительные заболевания гениталий у девочек занимают около 90% в детской практике и 35% в подростковой.
Классификация воспалительных урогенитальных заболеваний у девочек (В.Ф. Коколина, О.В. Зубакова, 1998)
Инфекционные.
Неспецифический бактериальный вульвовагинит.
Специфические:
гонорея;
трихомоноз;
хламидиоз;
бактериальный вагиноз;
уреа-микоплазмоз;
дифтерийный вульвовагинит;
генитальный туберкулёз;
кандидозный вульвовагинит;
вирусный вульвовагинит (цитомегаловирус, кондиломатозный вирус, вирус герпеса).
Первично-инфекционные.
Инородное тело влагалища.
Энтеробиоз. Глистная инвазия.
Онанизм.
Изменение реактивности организма (нарушение обмена веществ, дисметаболическая нефропатия, аллергические заболевания, дисбактериоз кишечника, заболевания мочевыводящих путей, острые вирусные заболевания, детские инфекции).
Классификация воспалительного процесса по локализации заключается в выделении следующих форм: вестибулит, вульвит, вульвовагинит, кольпит (эти формы встречаются наиболее часто), эндоцервицит, эндометрит, сальпингит, оофорит (эти формы встречаются реже), периметрит, параметрит, пельвиоперитонит (очень редко).
Основным проявлением воспалительного процесса половых органов девочки (наиболее часто это вульвовагинит) являются БЕЛИ. Бели – это явление характерное для женщин всех возрастных групп. В детской гинекологической практике бели не всегда носят патологический характер. В период новорожденности бели обусловлены плацентарными и материнскими гормонами, в возрасте 7-8 лет избыточные бели являются признаком начальной гормональной стимуляции, в 13-15 лет – признаком гормональных всплесков. Физиологическими, не требующими лечения белями следует считать светлые, слизистые, без запаха и примесей выделения. В настоящее время многими исследователями вульвовагинит рассматривается не как самостоятельное заболевание, а как проявление различных патологических состояний: кожной патологии, признак иммунодефицита, дисбиотических состояний нарушения обмена веществ и др. Существует также связь между вульвовагинитом в детстве и внутриутробной инфекцией. В тоже время инфицирование, бактерионосительство, вульвовагинит впервые могут возникнуть в момент рождения: пройдя по родовым путям матери, девочка приобретает материнскую микрофлору, которая определяет первичный спектр как нормального, так и патологического биоценоза влагалища девочки.
Факторы, способствующие развитию вульвовагинитов.
Анатомо-морфофункциональные особенности половых органов девочек: тонкая дерма, разрыхленный эпидермис, рН кожи-6,7.
Физиологические затворы гениталий практически не развиты.
Автономные иммунные механизмы: секреторные иммуноглобулины А, лизоцим, система комплимента, фагоцитоз функционально практически не развиты.
Индивидуальные особенности анатомии - отсутствие задней спайки, низкое расположение мочеиспускательного отверстия, неполные или полные синехии, аномалии развития половых органов.
Клиническая картина вульвовагинитов. Типичными жалобами при остром или хроническом в-в являются жалобы на жжение, усиливающийся при мочеиспускании, зуд и бели различной интенсивности, умеренные боли в половых органах. Клинические проявления в зависимости от этиологического фактора имеют незначительные различия. Общее состояние девочки практически не нарушается, (исключение составляет острая гонорея, где могут наблюдаться кратковременные подъемы температуры). Могут наблюдаться дизурия и расстройство стула. В случаях энтеробиозного в-в – боли в животе.
Диагностика в-в. Клиническая диагностика не представляет трудностей. Трудности представляет оценка совокупности этиологических факторов воспаления. Необходимо комплексное обследование ребенка, включая осмотры смежных специалистов и методы лабораторной диагностики. Из специальных методов исследований при рецидивирующем течении вульвовагинитов или при подозрении на инородное тело показана вагиноскопия. Общепринятыми методами лабораторной диагностики в гинекологической практике являются бактериоскопический, бактериологический и цитологический. Иммунофлюорисцентные, иммуноферментные исследования проводятся при подозрении на урогенитальную инфекцию.
Лечение вульвовагинитов комплексное. Первую группу препаратов составляют витамины, адаптогены, иммуностимуляторы (витамин А. Витамин В, витамин Е, настойка овса, эссенциале, иммуналинтерферон, левамизол, кальций хлорид, кальций глюконат и др.). С целью профилактики дисбиоза применяются эубиотики. При длительном, хроническом, торпидном или специфическом процессе назначается этиотропная антибактериальная терапия. Местное лечение состоит из трех последовательных этапов: этиотропное лечение, стимуляция процессов репарации, коррекция микробиоценоза влагалища. Лечение вульвовагинитов гонорейной или туберкулезной этиологии производится в специализированных учреждениях с трехкратным контролем излеченности.
ДИСФУНКЦИОНАЛЬНЫЕ МАТОЧНЫЕ КРОВОТЕЧЕНИЯ периода полового созревания составляют большую часть в структуре гинекологической патологии подросткового возраста. К дисфункциональным маточным кровотечениям относятся такие, которые обусловлены нарушениями ритмической продукции гормонов яичника и не связаны ни с органическими заболеваниями половой системы, ни с заболеваниями других систем организма. Чаще всего дисфункции различных звеньев репродуктивной системы способствуют хронические и острые инфекционные заболевания, гиповитаминозы, различные стрессовые ситуации, соматические заболевания, неблагоприятное течение антенатального периода, психические и эмоциональные перегрузки. Инфекционные заболевания занимают ведущее место среди этиологических факторов дисфункционального маточного кровотечения. Особенно часто в анамнезе отмечались такие заболевания как ангины, хронические пиелонефриты, пневмонии, краснуха, ревматизм, эпидпаротит.
В зависимости от клинико-морфологических особенностей ДМК разделяют на овуляторные и ановуляторные, причем в периоде полового созревания в основном встречаются ановуляторные ациклические кровотечения по типу персистенции или атрезии фолликулов. Во всех случаях ДМК подросткового периода являются следствием нарушения функции системы гипоталамус-гипофиз-яичник-матка.
Клиника. В связи с нередко встречающимися перемежающимся и рецидивирующим характером нарушения менструальной функции отмечается значительная вариабельность клиники. Ановуляторные ДМК характеризуются, как правило, периодом задержки месячных, сменяющихся длительным кровотечением различной интенсивности. В подростковом периоде кровотечения почти всегда безболезненны, но очень часто приводят к анемизации больных.
Диагностика не представляет сложности, а дифференциальная диагностика сложна и требует от врача объемных и многогранных знаний. Маточные кровотечения встречаются при заболеваниях крови (врожденных дефектах гемостаза, геморрагических диатезах, тромбоцитопениях, ангиогемофилии), выраженных нарушениях функции печени, Заболеваниях щитовидной железы, коры надпочечников, диэнцефальной патологии, туберкулезе. Не следует забывать о возможной беременности, опухолях яичников, различных формах рака, эндометриоза, и очень редко – фибромиомы. В ряде случаев кровотечение обуславливается врожденными пороками или аномалиями внутренних половых органов. Лечение ДМК комплексное, этиопатогенетическое и индивидуальное, складывается из общей терапии, применения сокращающих и кровоостанавливающих средств, гормонотерапии, хирургического вмешательства. После остановки кровотечения в течение трех циклов обязательно проведение противорецидивной и поддерживающей терапии. Девушки, страдающие ДМК должны наблюдаться у врача в течение 1 года.
Альгодисменорея – патологическое состояние, характеризующееся сочетанием болезненных месячных с циклически возникающими общесоматическими расстройствами. Альгодисменорею принято разделять на первичную и вторичную. Первичная (конституциональная, эссенциальная) связана с функциональными нарушениями в иммунной, нервной, эндокринной системах, водно-солевого равновесия). Вторичная обусловлена одним из следующих заболеваний: эндометриозом, воспалением внутренних половых органов, аномалиями развития половых органов, опухолями органов таза, половым инфантилизмом. Последняя причина - наиболее частая. Имеются указания на наследственный характер этой патологии. Несмотря на различный этиопатогенез, клиническая картина альгодисменореи одинакова в двух группах. Для альгодисменореи характерны интенсивные боли внизу живота, отклонения в работе ЖКТ, сердца. Боль иногда может носить очень интенсивный характер. Из общих симптомов отмечают также головную боль, тошноту и рвоту, депрессивное состояние, агрессивность, слюнотечение, потливость, ознобы. Для всех симптомов характерны цикличность их возникновения и спонтанное излечение.
Диагностика альгодисменореи имеет комплексный подход с обязательным консультированием девушки у смежных специалистов, проведением УЗИ-диагностики, общеклинических исследований. Особое внимание стоит уделить диагностике полового инфантилизма. В симптомокомплексе полового инфантилизма ведущее место занимает состояние матки, именуемое гипоплазией. Различают три стадии гипоплазии матки. Рудиментарная, или зародышевая. Инфантильная (длина по зонду 3,5-5 см, соотношение тела и шейки 1:3). Гипопластическая (длина по зонду 5-7 см, соотношение тела и шейки правильное).
studfiles.net
MED24INfO
Эндометриоз представляет собой одну из наиболее острых проблем современной эндокринной гинекологии. Актуальность этой проблемы обусловлена, во-первых, увеличением частоты эндометриоза в структуре гинекологической заболеваемости (в течение последнего десятилетия его частота возросла с 12 до 27 % оперированных гинекологических больных); и во-вторых, значением эндометриоза в качестве часто наблюдаемых причин нарушений трудоспособности и репродуктивной функции женщин. Среди всех случаев женского бесплодия на долю эндометриоза приходится около 20 %. Патологические изменения, обозначаемые в настоящее время термином “эндометриоз”, описаны еще в египетском папирусе. Согласно общепризнанному определению, эндометриоз — это патологический процесс, характеризующийся ростом и развитием ткани, идентичной по структуре и функции эндометрию, за пределами слизистой оболочки тела матки. Макроскопически эндометриоз имеет вид мелких изолированных или сливающихся с окружающими тканями очагов (узлов, инфильтратов) или кистозных образований с геморрагическим содержимым. Эндометриоидные очаги (за исключением эндометриоидных кист) лишены капсулы. Они состоят из железистого эндометриоподобного эпителия и цитогенной стромы, но менее подвержены циклическим превращениям, чем слизистая оболочка матки. В ткани эндометриоидных гетеротопий содержание рецепторов эстрогенов и прогестерона меньше, чем в нормальном эндометрии, причем количество рецепторов эстрогенов не изменяется в течение менструального цикла. Содержание рецепторов андрогенов не отличается от такового в ткани нормального эндометрия. Эндометриоз обладает способностью к инфильтрации окружающих тканей с деструкцией последних, а также к распространению по кровеносным и лимфатическим сосудам. Отсутствие капсулы, способность к инфильтрирующему росту и метастазированию сближают эндометриоз с опухолевым процессом. Однако в отличие от истинной опухоли для эндометриоза нехарактерен ни клеточный атипизм, ни прогрессивный автономный рост. Патогенез. Согласно теории ретроградной менструации, формирование очагов эндометриоза происходит в результате ретроградного заброса в брюшную полость жизнеспособных клеток эндометрия, отторгнутых во время менструации, и их имплантации в окружающие органы и брюшину. У больных эндометриозом выявлен ряд условий, способствующих ретроградным менструациям: гипотонус маточно-трубного соединения, своеобразный “стеноз шейки матки”, а также другие аномалии, затрудняющие естественный отток менструальной массы и повышающие давление в полости матки. “Ретроградная менструация” в той или иной степени происходит у каждой женщины и при каждой менструации. Однако эндометриоз формируется только при наличии условий для имплантации и эктопического роста эндометрия. Эти условия создаются, с одной стороны, вследствие нарушения регуляторных связей в системе гипоталамус — гипофиз — яичники — органы-мишени, а с другой, на фоне изменений в иммунной системе (усиленное выделение иммунокомпетентными клетками факторов, способствующих имплантации и пролиферации эндометрия). Разновидностями этой концепции являются теории лимфогенной, гематогенной и ятрогенной диссеминации. Их различает лишь представление о способах переноса клеток эндометрия за пределы его физиологической локализации. Все эти теории можно объединить понятием транспортного генеза эндометриоза. Эмбриональная теория происхождения эндометриоза предполагает развитие его из остатков парамезонефральных (мюллеровых) протоков или зародышевого материала, из которого формируются половые органы, в том числе и ткань эндометрия. Эта теория подтверждается данными о возможности развития эндометриоза у детей и подростков, а также его сочетанием с пороками развития половых органов (особенно с теми, которые создают препятствия нормальному оттоку менструальной крови). В соответствии с гипотезой целомической метаплазии, развитие эндометриоза происходит вследствие перерождения (метаплазии) мезотелия брю шины. Предполагается, что очаги эндометриоза возникают из клеток целомического эпителия, персистирующего в переходной зоне между миометри- ем и эндометрием. Эти клетки появляются в мезотелии, покрывающем яичники, маточные трубы и тазовую брюшину, при воздействии дегенерирующей эндотелиальной ткани во время менструации. Гормональные и/или иммунологические нарушения не являются непосредственной причиной формирования эндометриоидных фокусов. Они играют лишь роль факторов, поддерживающих патологический процесс. Наиболее распространенной является гипотеза о причинной зависимости эндометриоза и функциональной неполноценности системы гипоталамус — гипофиз — яичники. Практически все исследования у больных эндометриозом свидетельствуют о “заинтересованности” иммунной системы в патогенезе заболевания, однако точно локализовать изменения в определенной субпопуляции имму- нокомпетентных клеток не представляется возможным. Имеются сообщения об аутоиммунной природе заболевания. Установлено также изменение активности Т-клеточного звена иммунитета и активности перитонеальных макрофагов. Измененная активность иммунокомпетентных клеток встречается у 92—95 % больных эндометриозом и, вероятно, связана с наличием персис- тирующих вирусов (о чем свидетельствует повышение титров специфических антител). Развитие противовирусного иммунного ответа усиливает активность макрофагов и NK-каеток и способствует выделению ими факторов. стимулирующих имплантацию и пролиферацию жизнеспособных фрагментов эндометрия. Есть основания полагать, что эндометриоз является вирусподдерживаемым заболеванием. КЛАССИФИКАЦИЯ ЭНДОМЕТРИОЗАВ соответствии с локализацией процесса выделяют:
- — внутренний эндометриоз (аденомиоз), развивающийся в мышечной оболочке тела матки, ее перешейке, интерстициальных отделах маточных труб;
| Клинические признаки | Балл | Эндоскопические признаки | Балл |
| Бесплодие: | Типичные | ||
| первичное | 16 | Темные пятна на поверхности брюшины | 2 |
| вторичное | 4 | ||
| Тазовая боль: | Рубцовая ткань, окружающая имплантаты | 2 | |
| легкая | 4 | ||
| средняя | 8 | Желто-коричневые пятна на брюшине | 2 |
| тяжелая | 16 | ||
| Диспареуния | Типичный спаечный процесс в малом тазе | 2 | |
| легкая | 4 | (в том числе подъяичниковые сращения) | |
| средняя | 8 | Эндометриоидные кисты яичников: | |
| тяжелая | 16 | односторонние | 2 |
| Дисменорея: | двусторонние | 2 | |
| легкая | 4 | ||
| средняя | 8 | Нетипичные | |
| тяжелая | 16 | Железистые структуры на брюшине | 1 |
| Болезненность при | Петехиальная брюшина | 1 | |
| влагалищном иссле | |||
| довании: | |||
| легкая | 4 | Белые непрозрачные бляшки, окруженные | 1 |
| рубцовой тканью | |||
| средняя | 8 | ||
| тяжелая | 16 | “Пламеподобные пятна” | 1 |
| Гиперваскулярные зоны | 1 |
стадия I — патологический процесс ограничен (поражена только слизистая оболочка тела матки); стадия II — патологический процесс переходит на мышечные слои (до середины толщи мышечной стенки матки); стадия III — распространение патологического процесса на всю толщу мышечной стенки матки до ее серозного покрова; стадия IV — вовлечение в патологический процесс париетальной брюшины малого таза и соседних органов.
Данная классификация применима лишь к диффузным формам адено- миоза, при которых эндометриоидные имплантаты имеют вид слепых карманов или свищей. Аденомиоз может быть диффузным, очаговым или узловым (рис. 7.6):Рис. 7.5. Стадии внутреннего эндометриоза в зависимости от распространенности процесса.
Рис. 7.6. Формы аденомиоза.
А — диффузная; Б — очаговая; В — узловая. стадия I — мелкие точечные эндометриоидные очаги на поверхности яичников, брюшине прямокишечно-маточного пространства без кистозных полостей; стадия II — эндометриоидная киста одного яичника, диаметром не более 5—6 см, с мелкими эндометриоидными включениями на брюшине малого таза; незначительный спаечный процесс в области придатков матки без вовлечения кишечника; стадия III — эндометриоидные кисты обоих яичников (различной величины диаметром более 5—6 см в одном яичнике и небольшая эндометриома в другом). Эндометриоидные ге- теротопии небольших размеров на серозном покрове матки, маточных труб и на париетальной брюшине малого таза. Выраженный спаечный процесс в области придатков матки с частичным вовлечением кишечника; стадия IV — двусторонние эндометриоидные кисты яичников больших размеров (диаметром более 6 см) с переходом патологического процесса на соседние органы — мочевой пузырь, прямую и сигмовидную кишку. Распространенный спаечный процесс. Такое разделение, однако, является условным, поскольку истинная тяжесть заболевания определяется не размерами образования, а сопутствующим рубцово-спаечным процессом, инфильтрацией тканей вокруг шейки матки, мочеточников, кишечника и крестцово-маточных связок. Эндометриоз ретроцервикальной локализации (рис. 7.7): стадия /—эндометриоидные очаги в пределах ректовагинальной клетчатки; стадия II — прорастание эндометриоидной ткани в шейку матки и стенку влагалища с образованием мелких кист; стадия III — распространение патологического процесса на крестцовоматочные связки и серозный покров прямой кишки; стадия IV — вовлечение в патологический процесс слизистой оболочки прямой кишки, распространение процесса на брюшину прямокишечно-маточного пространства с образованием спаек в области придатков матки.Наиболее тяжелой формой заболевания считают ретроцервикальный эндометриоз с вовлечением в процесс мочевых путей и кишечника. Различают 3 типа очагов этой глубокой инфильтративной формы эндометриоза: при I типе происходит инфильтрация рыхлой соединительной ткани. При
- типе эндометриоидный узел скрывается под кишкой или спайками; инфильтрации тканей не наблюдается; III тип — глубокий эндометриоз характеризуется самыми большими узлами сферической формы, исходящими, по-видимому, из брюшины малого таза.
www.med24info.com